Während alle Klinikmitarbeitenden die Basismaßnahmen zur Wiederbelebung Erwachsener beherrschen müssen, wenden sich die erweiterten Maßnahmen an erfahrene Anwendende. Unser Autor fasst die wichtigen Informationen zum Advanced Life Support gemäß der neuen Leitlinien des European Resuscitation Councils (ERC) zusammen.
Priorisierung. Höchste Priorität haben im Advanced Life Support (ALS) qualitativ hochwertige Thoraxkompressionen mit minimierten Unterbrechungen, frühzeitige Defibrillation sowie die Behandlung potenziell reversibler Ursachen des Kreislaufstillstands. Nur wenn über die gesamte Dauer der Reanimation sehr guter Basic Life Support (BLS) geleistet wird, können die erweiterten Maßnahmen Erfolg versprechend sein.
Prävention. Ein Kreislaufstillstand in der Klinik tritt selten plötzlich und unerwartet auf. Ihm gehen häufig Frühwarnsymptome voraus. Eine Vielzahl von innerklinischen Reanimationen ist vermeidbar, wenn geeignete Maßnahmen zur Früherkennung kritisch kranker Patienten implementiert werden. Neben dem klassischen Reanimationsteam sollten daher Notfallteams gebildet werden, die nicht erst bei Reanimationspflichtigkeit alarmiert werden, sondern schon vorher bei kritisch kranken Patientinnen und Patienten (im Folgenden: Patienten) konsultiert werden. Alle Mitglieder der Notfall- und Reanimationsteams sollten einen international zertifizierten ALS-Kurs absolviert haben.
Das Klinikpersonal muss nicht nur im BLS geschult werden, sondern auch in der Früherkennung kritisch kranker Patienten. Typische frühe Symptome, denen ein Kreislaufstillstand folgen kann, sind Synkopen, Brustschmerzen, Palpitationen, Schwindel und plötzliche Atemnot. Diese gehen zumeist mit Veränderungen von Vitalwerten wie Herzfrequenz und -rhythmus, Blutdruck, Sauerstoffsättigung und Bewusstseinslage einher.
Kliniken sollten Kriterien festlegen, nach denen ein Notfallteam alarmiert wird. Dies kann z. B. ein Scoringsystem sein, in dem für bestimmte Symptome und Vitalwertveränderungen Punkte vergeben werden. Ab dem Erreichen einer definierten Punktezahl wird dann das Notfallteam gerufen. Auch der klinische Eindruck, den erfahrenes Personal von dem betroffenen Patienten hat, sollte eine Alarmierung rechtfertigen können.
Kritisch kranke Patienten müssen in einem Umfeld versorgt werden, das hinsichtlich der Personalstärke und -qualifikation und der technischen und apparativen Ressourcen der Schwere der Erkrankung angemessen ist. Dies kann eine Intermediate-Care-Station, eine Intensivstation oder eine Chest Pain Unit sein.
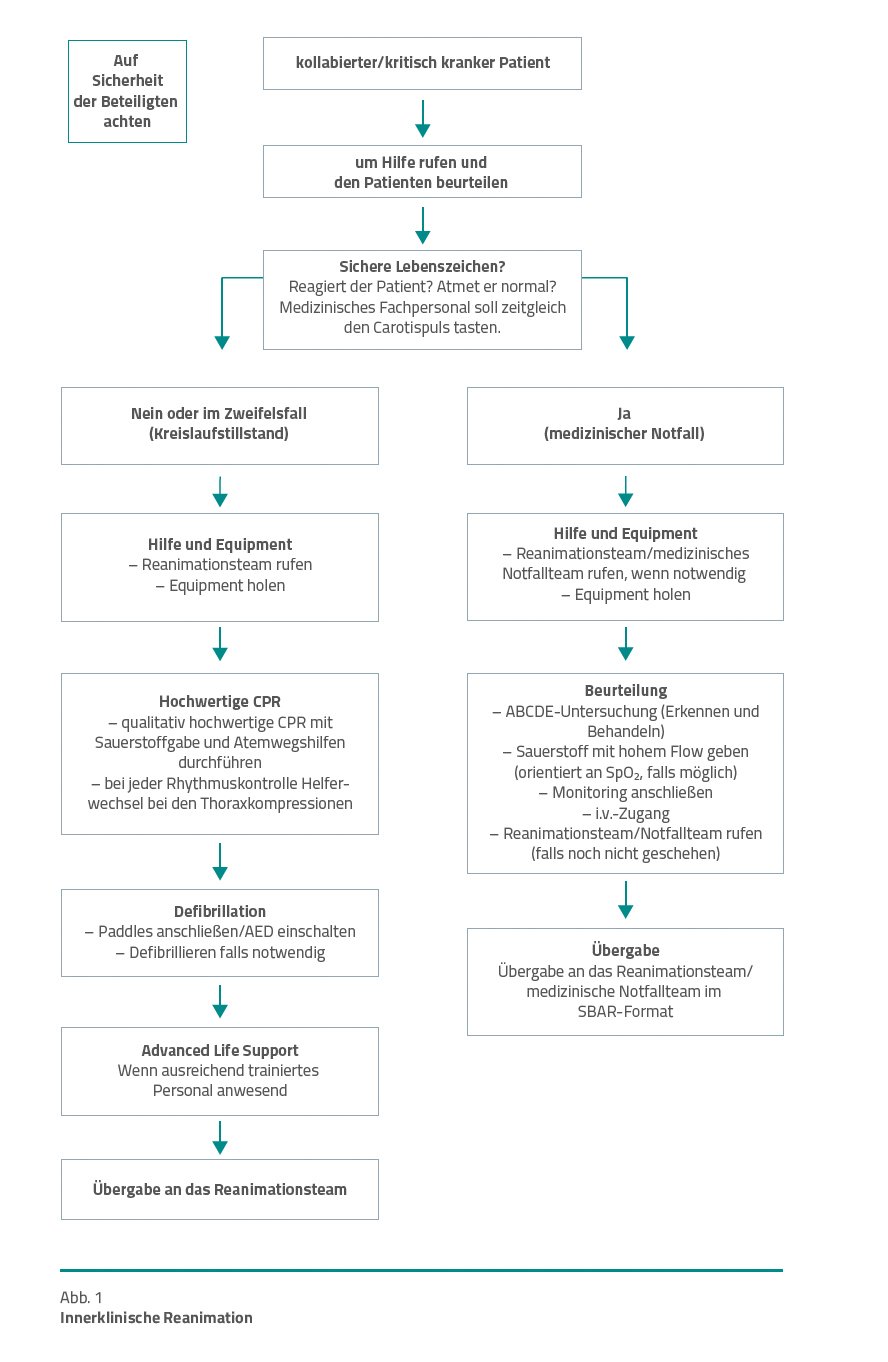
Das Vorgehen bei kritisch kranken Patienten sollte klar definiert sein. Abbildung 1 zeigt einen möglichen Ablauf dieses Vorgehens.
Behandlung des innerklinischen Kreislaufstillstands. Ziel jeder Klinik muss es sein, einen Kreislaufstillstand zu erkennen, das Reanimationsteam zu alarmieren, mit den Maßnahmen zum BLS zu beginnen und den Patienten innerhalb von 3 Minuten mit einem Automatisierten Externen Defibrillator (AED) zu behandeln.
Es muss ein Reanimationsteam vorhanden sein, das bei Alarmierung sofort ausrücken kann. Deren Mitglieder sollen die wichtigsten theoretischen und praktischen Fertigkeiten besitzen, um einen Kreislaufstillstand zu behandeln. Diese beinhalten die manuelle Defibrillation, das erweiterte Atemwegsmanagement, die Anlage eines intravenösen oder intraossären Zugangs sowie das Identifizieren und Behandeln potenziell reversibler Ursachen des Kreislaufstillstands. Das Reanimationsteam sollte sich zu jedem Schichtbeginn treffen, um die Ausrüstung zu überprüfen und Teamrollen festzulegen. Wünschenswert wäre eine international einheitliche Notfalltelefonnummer. Die Ausrüstung der Stationen mit Notfallmaterial sollte einheitlich sein.
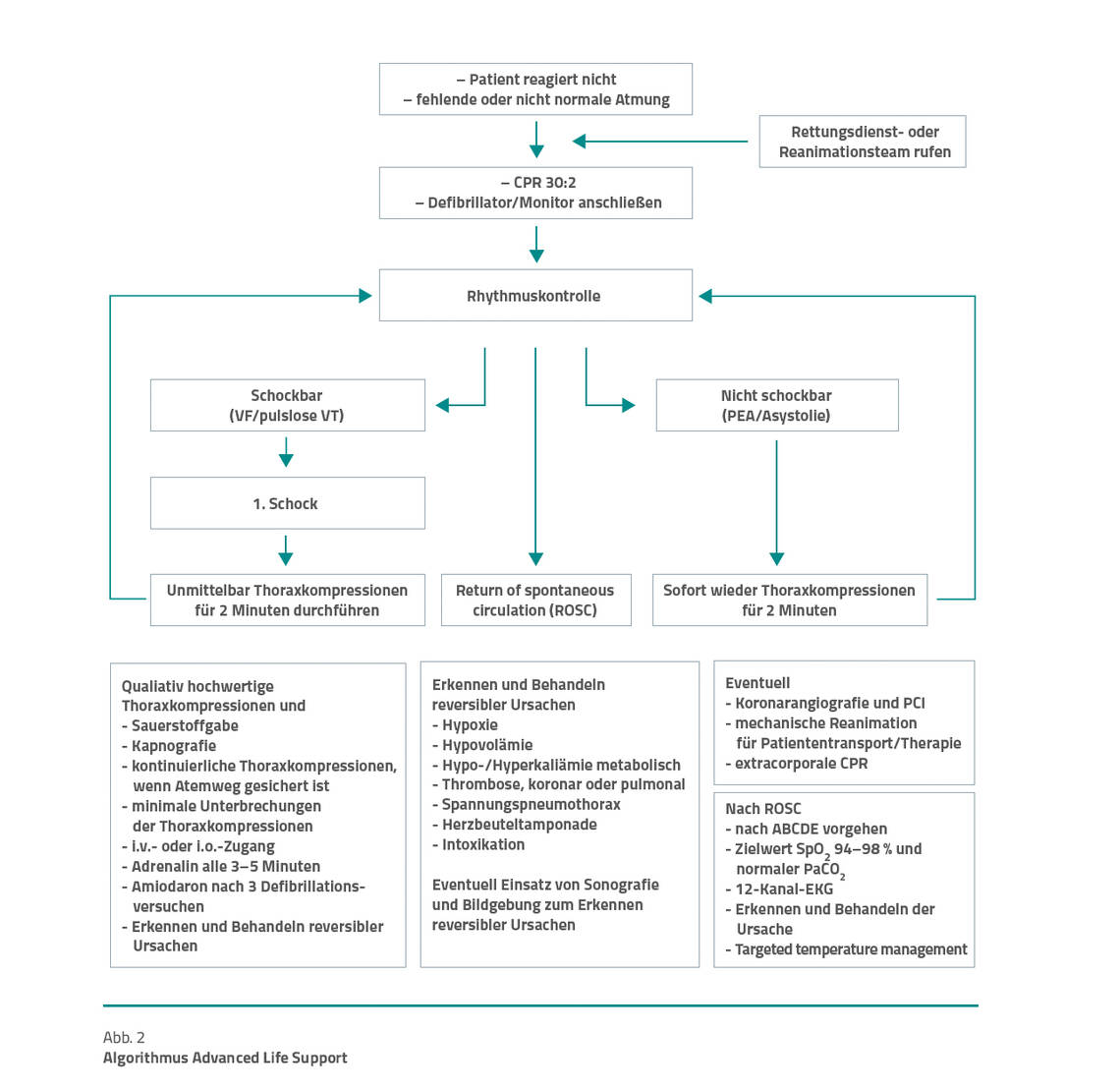
Universeller ALS-Algorithmus. Der universelle ALS-Algorithmus zur Reanimation Erwachsener (Abb. 2) stellt den Masterplan des ALS dar.
Die Startphase sowie der linke (defibrillierbare EKG-Rhythmen) und rechte (nichtdefibrillierbare EKG-Rhythmen) Schenkel des Algorithmus können bereits von den Ersthelfenden im Rahmen des BLS initiiert werden, sofern ein AED verfügbar ist.
Die eigentlichen ALS-Maßnahmen sind in den unteren 4 Feldern des Algorithmus dargestellt. Sie sollen in den 2-minütigen Intervallen zwischen den Rhythmuskontrollen abgearbeitet werden.
Manuelle Defibrillation. Im ALS wird die manuelle Defibrillation der Anwendung eines AED vorgezogen, da eine Person, die in der Analyse des Monitor-EKG geschult ist, schneller als ein AED den vorliegenden EKG-Rhythmus identifizieren kann. Daraus resultiert eine kürzere Thoraxkompressionspause, die sogenannte No-Flow-Zeit.
Defibrillierbar sind das Kammerflimmern (VF) und die pulslose ventrikuläre Tachykardie (PVT); nichtdefibrillierbar sind die Asystolie und die pulslose elektrische Aktivität (PEA). Unter dem Begriff PEA werden alle Rhythmen zusammengefasst, bei denen ein funktionierender Kreislauf vorstellbar ist, der Patient jedoch alle klinischen Kriterien zur Reanimationspflichtigkeit aufweist.
Der Defibrillator muss sofort unabhängig von den laufenden Thoraxkompressionen und Beatmungsversuchen angewendet werden, sobald er einsatzbereit ist.
Eine routinemäßige Phase von Thoraxkompressionen vor dem Schock wird nicht empfohlen.
Das Anbringen der Defibrillationselektroden erfolgt unter laufenden Thoraxkompressionen. Erst zur Rhythmuskontrolle wird das BLS kurz unterbrochen.
Höchste Priorität beim Defibrillationsversuch hat die Sicherheit der Helferin bzw. des Helfers (im Folgenden: Helfer). Der Helfer, der den Defibrillator bedient, muss alle anderen Helfer durch eine deutliche Warnung auf die bevorstehende Schockauslösung hinweisen und sich mit eigenen Augen davon überzeugen, dass niemand den Patienten oder dessen Bett berührt.
Wie Studien ergeben haben, schützen auch Einmalhandschuhe nicht ausreichend vor einer Verletzung der Helfer.
Sauerstoff im offenen System (Beutel-Masken-Beatmung) muss 1 m von der Defibrillationszone entfernt werden, da durch die Schockauslösung bei hoher Sauerstoffkonzentration in der Umgebung ein Brand entstehen kann. Beatmungsgeräte und -beutel am geschlossenen System (Endotrachealtubus, supraglottischer Atemweg) können konnektiert bleiben.
Ziel beim Defibrillationsversuch ist es, die daraus zwangsläufig entstehende No-Flow-Zeit von 5 Sekunden zu unterschreiten. Dies kann nur gelingen, wenn in der Zeit, in der der Defibrillator lädt, Thoraxkompressionen durchgeführt werden, die erst für die Schockabgabe unterbrochen werden. Beatmungen sollen in der Ladephase des Defibrillators nicht mehr verabreicht werden.
Sofort nach dem Defibrillationsversuch müssen die Thoraxkompressionen (und auch die Beatmungen) wieder aufgenommen und bis zur nächsten Rhythmuskontrolle durchgeführt werden – es sei denn, physiologische (arterielle Blutdruckkurve, Kapnografie) und klinische (Aufwachen, gezielte Bewegungen) Zeichen deuten auf einen Spontankreislauf hin. Ist dies der Fall, kann eine vorzeitige Rhythmus- und Pulskontrolle erwogen werden.
In der Regel werden einzelne Schocks, gefolgt von 2-minütigen Kompressionsphasen, abgegeben. Ist ein Defibrillator bereits bei Eintritt des Kreislaufstillstands installiert (z. B. im Herzkatheterlabor), können, wenn nötig, 3 Schocks hintereinander verabreicht werden.
Die Hersteller von Defibrillatoren empfehlen unterschiedliche Anfangsenergien, eskalierend bis zur Maximalenergie beim dritten Schock. Sind der anwendenden Person diese Empfehlungen nicht bekannt, sollte diese bereits beim ersten Schock die maximal mögliche Energiestufe wählen.
Bei defibrillationsrefraktären EKG-Rhythmen kann eine Veränderung der Position der Defibrillationselektroden erwogen werden.
Atemwege und Beatmung. Neben einem (bei supraglottischem Atemweg relativen) Aspirationsschutz ist der eigentliche Vorteil der Sicherung der Atemwege die Möglichkeit, kontinuierliche Thoraxkompressionen ohne Beatmungspausen durchführen zu können.
Obwohl der Endotrachealtubus (ET) den „Goldstandard“ darstellt, sollte die Intubation nur durch erfahrene Mitarbeitende versucht werden. Die Leit-linien definieren erstmals die Intubationserfahrung als eine 95-prozentige Erfolgsrate bei maximal 2 Versuchen.
Bei der Intubation wird eine No-Flow-Zeit von unter 5 Sekunden angestrebt. Das bedeutet, dass die Laryngoskopie unter laufenden Thoraxkompressionen erfolgen muss, die nur für den Moment der Tubuspassage durch die Stimmritze kurz unterbrochen werden.
Wer nicht über Intubationserfahrung verfügt, kann versuchen, unter laufenden Thoraxkompressionen eine Larynxmaske, eine IGEL-Maske oder einen Larynxtubus zu platzieren. Diese sogenannten supraglottischen Atemwegshilfen (SGA) bieten oftmals ebenfalls eine ausreichende Dichtigkeit zur Durchführung kontinuierlicher Thoraxkompression. Sollte dies nicht der Fall sein, muss auf die Thoraxkompressionen und Beatmungsversuche im Rhythmus 30:2 ausgewichen werden.
Die Leitlinie bevorzugt keine der 3 genannten SGA. Der German Resuscitation Council (GRC) hingegen postulierte auf seinem Online-Reanimationsdialog am 27. März 2021 die IGEL-Maske als SGA der ersten Wahl.
Kapnografie. Die grafische Darstellung des endtidalen CO₂ ist im ALS in dreierlei Hinsicht hilfreich: Zum einen beweist sie die korrekte Lage der Atemwegssicherung. Zum anderen gibt sie Aufschluss über die Qualität der Thoraxkompressionen. Zum Dritten sind dauerhafte CO₂-Werte unter 10 mmHg mit einem letalen Ausgang der Reanimation assoziiert. Ein plötzlicher Anstieg auf Werte über 40 mmHg weist auf das Vorhandensein eines Spontankreislaufs hin.
Intravenöser/intraossärer Zugang. Um Medikamente und/oder Infusionen zu verabreichen, wird ein Zugang zum Kreislauf des Patienten benötigt. Galten in früheren Leitlinien intravenöser und intraossärer Zugang als gleichwertig, bevorzugen die aktuellen Leit-linien den intravenösen Zugang als erste Wahl. Misslingt der Versuch der Anlage eines intravenösen Zugangs, kann ein intraossärer Zugang erwogen werden.
Medikamente. Der Einsatz eines Vasopressors und von Antiarrhythmika bei der Reanimation ist wegen des geringen Einfusses auf das Langzeitüberleben und unklarer Effekte auf das neurologische Ergebnis weiterhin mit einer sehr niedrigen Evidenz behaftet. Dennoch wurden diese im ALS belassen.
Adrenalin wirkt alpha- und betamimetisch und soll eine verbesserte Durchblutung von Herz, Lunge und Gehirn unter Thoraxkompressionen bewirken. 1 mg Adrenalin sollte bei nichtdefibrillierbaren EKG-Rhythmen so schnell wie möglich intravenös verabreicht werden. Dieser Empfehlung liegen Metaanalysen zweier placebokontrollierter Studien (PACA und PARAMEDIC2) zugrunde, die ergaben, dass die frühe Applikation von 1 mg Adrenalin die Entstehung eines Spontankreislaufs begünstigt und die Überlebensrate von 3 Monaten nach Krankenhausentlassung verbessert.
Der Einfluss auf das neurologische Outcome ist hingegen unsicher. Die positiven Effekte waren bei defibrillierbaren Rhythmen weniger ausgeprägt. Daher wird die Gabe von 1 mg Adrenalin bei defibrillierbaren Rhythmen erst nach dem dritten Schock empfohlen. Bei beiden Rhythmen soll die Verabreichung von 1 mg Adrenalin alle 3 bis 5 Minuten wiederholt werden.
Antiarrhythmika (Amiodaron und Lidocain) sind ausschließlich bei defibrillierbaren EKG-Rhythmen und Periarrest-Arhythmien indiziert.
Im präklinischen Setting konnten placebokontrollierte Studien zeigen, dass im Vergleich zur Verabreichung eines Placebos mehr Patienten lebend das Krankenhaus erreichten, wenn 300 mg Amiodaron bei defibrillierbaren Rhythmen verabreicht wurden. Keine Verbesserung konnte bei der Krankenhausentlassungsrate und dem neurologischen Outcome gefunden werden.
Eine Subgruppenanalyse zeigte Vorteile für den Einsatz von Amiodaron, wenn der Kreislaufstillstand sich vor Zeugen ereignete, die sofort mit BLS begonnen hatten.
Der ERC empfiehlt die Applikation von 300 mg Amiodaron nach drei Schocks sowie zusätzlich 150 mg Amiodaron nach dem fünften Schock oder bei Wiederauftreten eines defibrillierbaren Rhythmus.
Alternativ können 100 mg Lidocain nach dem dritten Schock verabreicht werden, wenn Amiodaron nicht verfügbar ist oder das lokale Protokoll Lidocain vorschreibt. Nach dem fünften Schock oder bei Wiederauftreten eines defibrillierbaren Rhythmus können zusätzlich 50 mg Lidocain injiziert werden.
Potenziell reversible Ursachen. Hohe Priorität hat im ALS die Suche und Behandlung potenziell reversibler Ursachen der Reanimationspflichtigkeit (Kasten: Potenziell reversible Ursachen des Kreislaufstillstands). Dies verbessert nicht nur die Prognose von nichtdefibrillierbaren EKG-Rhythmen und defibrillationsrefraktären EKG-Rhythmen, sondern kann eine erneut auftretende Reanimationspflichtigkeit nach dem Wiedereinsetzen eines spontanen Kreislaufs (return of spontaneous circulation, ROSC) verhindern.
Es gilt, nach allen naheliegenden, potenziell reversiblen Ursachen zu suchen, denn es können auch mehrere Ursachen vorliegen. Diese Konzentration auf nur eine scheinbar naheliegende Ursache kann in einem Fixierungsfehler mit fatalen Folgen für den Patienten münden.
Hilfreich für die Diagnose einer Herzbeuteltamponade, eines Spannungspneumothorax oder einer Lungenembolie ist eine schnelle Ultraschallunter- suchung des Thorax (Point-of-Care-Ultraschall, POCUS) in einer sehr kurzen (< 5 Sekunden) Thoraxkompressionspause. Diese soll nur von erfahrenen Ultraschallanwendern durchgeführt werden und es darf zu keiner eskalierten Thoraxkompressionspause führen oder eine Defibrillation verzögern.
Eine im Ultraschall gesehene Dilatation des rechten Ventrikels ohne weitere klinische Zeichen oder Hinweise aus der Anamnese rechtfertigt nicht die Diagnose einer Lungenembolie, da der rechte Ventrikel im Kreislaufstillstand regelhaft erweitert ist.
Zu erwägende Prozeduren. Die Datenlage zur Anwendung mechanischer Geräte zur Thoraxkompression ist nach wie vor unklar. Zwar konnte in einer neuen präklinischen Studie nachgewiesen werden, dass die Krankenhausentlassungsrate bei Anwendung mechanischer Geräte zur Thoraxkompression verbessert war. Die hatte jedoch keinen Einfluss auf das neurologische Outcome. Daher rät der ERC vom routinemäßigem Gebrauch mechanischer Geräte zur Thoraxkompression ab.
Dennoch kann deren Einsatz unter bestimmten Umständen sinnvoll sein. Der Transport eines Patienten unter CPR, notwendige lang anhaltende Thoraxkompressionen bei Lungenembolie, Hypothermie oder als Überbrückung bis zum Anschluss an einen extrakorporalen Kreislauf sind solche Indikationen. Auch die Gefährdung der Helfer durch Strahlen bei CT-Untersuchungen und Koronarangiografien rechtfertigen den Gebrauch mechanischer Geräte zur Thoraxkompression.
Die Installation mechanischer Geräte zur Thoraxkompression kann erhebliche No-Flow-Zeiten provozieren und sollte deshalb regelmäßig trainiert werden.
Der Anschluss des Patienten an eine Herz-Lungen-Maschine oder venoarterielle ECMO kann unter bestimmten Bedingungen als Rescue-Therapie erwogen werden:
- sofortiger CPR-Beginn bei Eintritt des Kreislaufstillstands
- junger Patient (nicht älter als 65 bis 70 Jahre) ohne wesentliche Komorbiditäten
- nachgewiesene oder vermutete reversible Ursache, die eine sehr lange CPR erfordert (z. B. schwere Hypothermie oder Intoxikation)
- Anschlussmöglichkeit innerhalb von weniger als einer Stunde durch ein Team mit Expertise, Erfahrung und geeigneter Ausrüstung in einer hygienisch einwandfreien Umgebung
Postreanimationsbehandlung. Die Postreanimationsbehandlung beginnt an dem Ort, an dem ROSC erreicht wurde. Wesentliche Bestandteile der Postreanimationsbehandlung sind eine periphere Sauerstoffsättigung von 94 bis 98 %, Normokapnie, Erstellung eines 12-Kanal-EKG, ein zielgerichtetes Temperaturmanagement (Zieltemperatur: 36 bis 32 °C) sowie das Erkennen und Behandeln der Ursache des Kreislaufstillstands.
Zusammenfassung. Die Kernaussagen der neuen ERC-Leitlinie zum ALS sind:
- Höchste Priorität haben qualitativ hochwertige Thoraxkompressionen mit minimierten Unterbrechungen, frühe Defibrillation und die Behandlung reversibler Ursachen.
- Vor dem Kreislaufstillstand treten oft Frühwarnzeichen auf. Der Kreislaufstillstand ist oft vermeidbar.
- Atmungwegssicherung durch Basis- und erweitertes Atemwegsmanagement. Endotrache-ale Intubation nur durch erfahrene Anwender.
- Frühzeitige Adrenalingabe bei nichtdefibrillier-baren EKG-Rhythmen.
- Erwägung von extrakorporaler CPR bei ausgewählten Patienten und erfolglosem konventionellen ALS als Rescue-Therapie.
[1] Soar J et al. European Resuscitation Council Guidelines 2021: Adult advanced life support. www.erc.edu; Zugriff: 05.04.2021