Die neuen Reanimationsleitlinien setzen für den Advanced Life Support neue Akzente für physiologiebasierte Steuerung, Monitoring und Qualität der lebensrettenden Maßnahmen. Dieser Artikel zeigt auf, was sie für den Klinikalltag bedeuten.
Die im Oktober veröffentlichte Aktualisierung der Reanimationsleitlinien des European Resuscitation Council (ERC) [1] enthält Anpassungen sowohl im Bereich der einfachen lebensrettenden Maßnahmen (Basic Life Support, BLS), die in der vorigen Ausgabe von Die Schwester | Der Pfleger vorgestellt wurden, als auch für die erweiterten lebensrettenden Maßnahmen – das Advanced Life Support (ALS).
Monitoring gewinnt an Bedeutung
Die grundlegenden Prinzipien des ALS bleiben unverändert: Hochwertige Thoraxkompressionen (Herzdruckmassagen) mit minimalen Unterbrechungen, frühzeitige Defibrillation bei schockbarem Rhythmus, Sicherstellung eines gesicherten Atemwegs, die systematische Gabe von Medikamenten im Rahmen des Algorithmus sowie das Suchen und Behandeln potenziell reversibler Ursachen der Reanimationspflichtigkeit des Patienten. Diese Säulen bilden das Fundament, auf dem die neuen Empfehlungen aufbauen.
Physiologiegeleitete Reanimation. Eine bedeutende Neuerung ist die verstärkte Berücksichtigung physiologischer Zielparameter während der Reanimation. So dient das endtidale Kohlendioxid (ETCO₂) nicht nur zur Lagekontrolle der jeweiligen Atemwegshilfe, sondern zunehmend als Trendparameter zur Steuerung der Behandlung – etwa zur Beurteilung der Qualität der Thoraxkompressionen und der Wiederherstellung eines Spontankreislaufs (Return of spontaneous circulation, ROSC). Zielgröße ist ein ETCO₂-Wert von 25 mmHg.
Darüber hinaus stellt die Leitlinie invasive oder weniger invasive hämodynamische Zielgrößen vor – etwa einen diastolischen Blutdruck ≥ 30 mmHg vor und nach ROSC – und erörtert sie als mögliche Orientierungswerte, ohne sie als verbindliche Empfehlung festzulegen.
Diese Entwicklung markiert einen Wandel weg von einem rein algorithmischen Vorgehen hin zu einer wirkorientierten Steuerung der Maßnahmen („quality of CPR“) – sodass nicht mehr nur das „Was“, zum Beispiel Schock und/oder Medikament, zählt, sondern zunehmend das „Wie gut“ oder „Wie wirksam“. In der Praxis bedeutet dies: Monitoring- und Feedbacksysteme gewinnen an Bedeutung; Teams müssen in der Lage sein, Parameter zu interpretieren und gegebenenfalls Reanimationsstrategien anzupassen.
CPR-induziertes Bewusstsein. Cardiopulmonary Resuscitation-Induced Consciousness (CPRIC, auf deutsch: CPR-induziertes Bewusstsein) beschreibt das Vorhandensein eines Bewusstseins ohne ROSC während einer Herz-Lungen-Wiederbelebung. Dieses Phänomen tritt zwar selten auf, ist aber durch zahlreiche Berichte aus Praxis und Literatur als relevantes Phänomen bekannt. Rettende können in Erwägung ziehen, Beruhigungsmittel oder Analgetika (oder beides) in kleinen Dosen zu verwenden, um Schmerzen und Leiden der Betroffenen zu vermeiden, die während der Reanimation bei Bewusstsein sind.
Das Schema der Sedierung und Analgesie während der Reanimation hängt von lokalen Protokollen ab. Die Therapien können auf denen basieren, die bei kritisch kranken Patienten zur Anwendung kommen, zum Beispiel kleine Dosen von Fentanyl, Ketamin und/oder Midazolam.
Defibrillation. Manuelle Defibrillatoren sind Reanimationsteams vorbehalten, die innerhalb von 5 Sekunden einen Kreislaufstillstandsrhythmus sicher identifizieren und bei Bedarf einen sicheren Schock mit weniger als 5 Sekunden Unterbrechung der Thoraxkompressionen abgeben können.
Fortgeschrittene Rettende müssen sowohl mit einem automatisierten externen Defibrillator (AED) als auch mit einem manuellen Defibrillator vertraut sein. Wenn das Reanimationsteam eintrifft und ein AED bereits in Gebrauch ist, sollte es die laufenden Schockanweisungen zunächst befolgen und anschließend – wenn möglich – während eines zweiminütigen Herz-Lungen-Wiederbelebungszyklus auf einen manuellen Defibrillator umsteigen, um kürzere Thoraxkompressionspausen zu erzielen.
Defibrillationsstrategien. Die Leitlinie empfiehlt, die Defibrillationspads nach dem Einschalten des Defibrillators unter laufenden Thoraxkompressionen auf den Thorax des Patienten zu kleben; zunächst in anterolateraler Position. Sobald der Defibrillator einsatzbereit ist, stoppen die Thoraxkompressionen und es erfolgt eine kurze Rhythmusanalyse (kürzer als fünf Sekunden). Während der Ladung der Elektroden sind die Thoraxkompressionen fortzusetzen. Sobald die Elektroden geladen sind, darf niemand den Patienten berühren und es erfolgt der Defibrillationsversuch. Sofort danach sind die Thoraxkompressionen und die Beatmung fortzusetzen. Alle zwei Minuten ist die Rhythmuskontrolle und gegebenenfalls die Defibrillation zu wiederholen.
Bewirken drei Schocks keine Konversion des Kammerflimmerns oder der pulslosen ventrikulären Tachykardie in eine perfundierende Herzaktion, liegt ein refraktärer schockbarer Rhythmus vor. Für diesen Fall empfiehlt die Leitlinie einen Vektorwechsel der Defibrillationselektroden in eine anteriore/posteriore Position. Dabei ist das vordere Pad links vom Sternum zu platzieren und das hintere Pad am Rücken auf gleicher Höhe mittig, direkt medial vom linken Schulterblatt.
Für entsprechend trainierte Teams schlägt der ERC die sogenannte „Precharging“-Strategie vor: Die Elektroden sind bereits unmittelbar vor der Rhythmusanalyse zu laden, um gegebenenfalls sofort defibrillieren zu können, ohne eine weitere Thoraxkompressionspause zum Schocken in Kauf zu nehmen.
Defibrillationsversuche können zu Bränden führen, wenn der Schock in sauerstoffreicher Umgebung erfolgt. Daher sollten Sauerstoffmasken, Sauerstoffnasensonden und Beutel-Masken-Systeme mindestens einen Meter vom Brustkorb des Patienten entfernt liegen. Ein selbstfüllender Beutel oder ein Beatmungsgerät an einem geschlossenen System wie dem Endotrachealtubus oder einer supraglottischen Atemwegshilfe können angeschlossen bleiben.
Atemwegssicherung und Beatmung. Der große Vorteil der Atemwegssicherung mittels Endotrachealtubus oder supraglottischer Atemwegshilfe besteht gegenüber der Beutel-Masken-Beatmung darin, dass neben einer reduzierten Aspirationsgefahr kontinuierliche Thoraxkompressionen ohne Beatmungspausen erfolgen können.
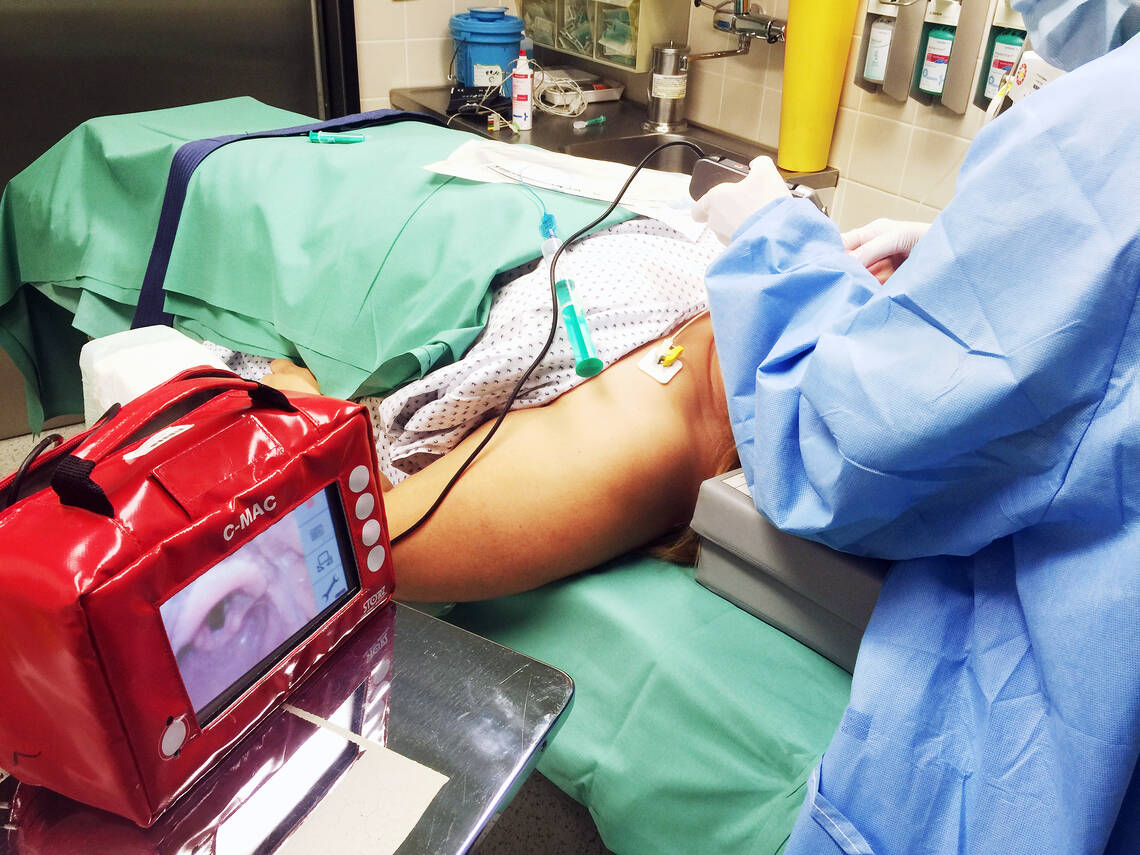
„Goldstandard“ der Atemwegssicherung bleibt die endotracheale Intubation. Die Thoraxkompressionspause für die Intubation darf fünf Sekunden nicht überschreiten. Diese sollten nur in dieser Technik sehr erfahrene Rettende übernehmen, die eine 95-prozentige Erfolgsrate in zwei Versuchen aufweisen. Ist ein Videolaryngoskop verfügbar, ist dieses der direkten Laryngoskopie vorzuziehen. Die Verifikation der korrekten Lage des Endotrachealtubus muss mittels Kapnometrie (ETCO₂) erfolgen.
Ist ein derart erfahrener Rettender nicht verfügbar, ist auf eine supraglottische Atemwegshilfe auszuweichen. Im Gegensatz zur vorherigen Leitlinie, die keine bestimmte supraglottische Atemwegshilfe präferiert hatte, empfiehlt der ERC in der aktuellen Leitlinie die Verwendung des Produkts i-gel®.
Die Beatmung sollte mit maximaler Sauerstoffkonzentration und einer Beatmungsfrequenz von zehn Atemzügen pro Minute erfolgen. Es ist darauf zu achten, den Patienten weder zu hypoventilieren noch zu hyperventilieren. Bei Verwendung eines Beatmungsgeräts soll das Team einen volumenkontrollierten Beatmungsmodus einstellen. Die Parameter sind
- Hubvolumen: 6 bis 8 ml/kg (geschätztes Körpergewicht) oder so viel dass sich der Thorax hebt und senkt,
- Atemfrequenz: 10 Atemzüge pro Minute,
- Inspirationszeit: 1 bis 2 Sekunden,
- positiv endexpiratorischer Druck (PEEP): 0 bis 5 cm H2O
- Spitzendruckbegrenzung: 60 bis 70 cm H2O
- Flow-Trigger: deaktivieren
Intravenöser Zugang. Zwischen der ersten und der zweiten Rhythmusanalyse ist ein intravenöser Zugang zu etablieren, weil die Wirksamkeit der Medikation bei Herzstillstand zeitabhängig ist. Gelingt dies innerhalb von zwei Minuten in zwei Versuchen nicht, ist ein intraossärer Zugang indiziert, der mit einer Bohrmaschine in die proximale oder distale Tibia oder in den proximalen Humerus zu schrauben ist.
Medikamente und Flüssigkeit. Adrenalin ist ein Sympathomimetikum und bewirkt unter anderem eine Vasokonstriktion. Diese Eigenschaft soll den Blutfluss von Herz, Lunge und Gehirn unter Thoraxkompressionen verbessern. 1 mg Adrenalin ist bei defibrillierbaren Rhythmen nach dem dritten Schock zu verabreichen und von da ab alle drei bis fünf Minuten erneut zu injizieren. Bei nichtdefibrillierbaren Rhythmen erfolgt die erste Applikation von 1 mg Adrenalin, sobald ein venöser Zugang verfügbar ist, und ist in der weiteren Folge alle drei bis fünf Minuten zu wiederholen.
Amiodaron ist ein Antiarrhythmikum und nur bei defibrillierbaren Rhythmen indiziert. 300 mg Amiodaron sind einmalig nach dem dritten Schock zu verabreichen. Ist der defibrillierbare Rhythmus nach dem fünften Schock nicht terminiert, sind einmalig 150 mg Amiodaron zu injizieren. Alternativ sind 100 mg Lidocain nach dem dritten Schock und 50 mg Lidocain nach dem fünften Schock zu verabreichen.
Die Leitlinie empfiehlt keine routinemäßige Verabreichung von Calcium und Bikarbonat – mit Ausnahme bestimmter Indikationen (Hyperkaliämie). Dies gilt auch für Glukokortikoide.
Die Verabreichung isotoner Kochsalzlösungen oder balancierter Kristalloidlösungen ist nur indiziert, wenn Hypovolämie den Kreislaufstillstand verursacht hat.
Potenziell reversible Ursachen. Eine zentrale Aufgabe ist das schnellstmögliche Suchen und Behandeln der Ursache der Reanimationspflichtigkeit des Patienten. Es gibt acht potentiell reversible Ursachen; auch „Hs und HITS“ genannt, da die Anfangsbuchstaben der ersten vier Ursachen H ist und die Anfangsbuchstaben der zweiten vier Ursachen das Akronym HITS bilden: Hypoxie, Hypovolämie, Hypo-/Hyperkaliämie, Hypo-/ Hyperthermie, Herzbeuteltamponade, Intoxikationen, Thrombose (Myokardinfarkt/Lungenembolie), Spannungspneumothorax.
Sonografie. Ultraschalluntersuchungen können sehr nützlich bei der Suche nach potenziell reversiblen Ursachen – zum Beispiel Herzbeuteltamponadeoder Spannungspneumothorax – sein. Diese sollen nur sehr erfahrene Untersuchende vornehmen und dürfen keine zusätzlichen oder längeren Unterbrechungen der Thoraxkompressionen verursachen.
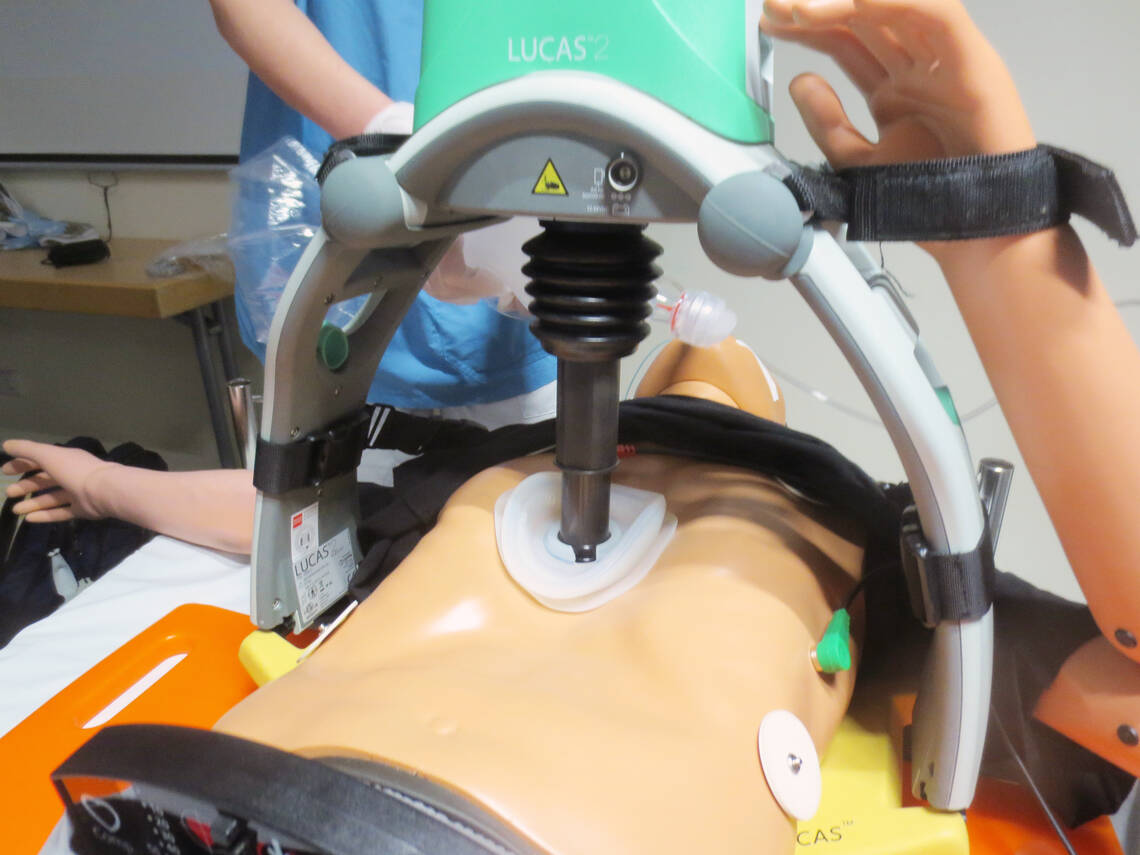
Mechanische Geräte zur Thoraxkompression. Der ERC empfiehlt den Einsatz mechanischer Geräte zur Thoraxkompression nur, wenn hochwertige manuelle Thoraxkompressionen nicht praktikabel sind oder die Sicherheit gefährden. Nur im Umgang mit dem Gerät trainierte Teams sollen mechanische Geräte zur Thoraxkompression benutzen, um längere Unterbrechungen der Thoraxkompressionen zu minimieren.
Extrakorporale Reanimation meint den Anschluss eines Reanimationspatienten an eine Herz-Lungen-Maschine oder Extrakorporale Membranoxigenierung (ECMO), wenn sich mittels konventioneller Reanimation der Kreislauf nicht wiederherstellen lässt und die Voraussetzungen dafür gegeben sind.
Das Potenzial der Leitlinien voll ausschöpfen
Die aktualisierten Reanimationsleitlinien setzen für das ALS klare Schwerpunkte auf Physiologie, Monitoring und Qualität der Reanimation. Sie ist sehr praxisorientiert und berücksichtigt moderne Technik – zum Beispiel ECPR, kontinuierliches Blutdruck- monitoring.
Für die Praxis bedeutet das, dass sich Reanimationsteams auf Training, Implementierung neuer Geräte und Prozesse einstellen müssen, um das Potenzial der neuen Leitlinie voll auszuschöpfen.
In der nächsten Ausgabe von Die Schwester | Der Pfleger werden im dritten Teil der Artikelserie über die neuen Reanimationsleitlinien Neuerungen im Bereich des Paediatric Life Support (PLS) vorgestellt.
[1] Soar J et al. European Resuscitation Council Guidelines 2025. Adult Advanced Life Support. Resuscitation 10/2025. Elsevier; 2025