Die aktuelle S3-Leitlinie „Nierenersatztherapie in der Intensivmedizin“ bietet evidenzbasierte Empfehlungen zur Indikationsstellung, Anwendung und Überwachung der Dialyse bei kritisch kranken Patienten mit akutem Nierenversagen. Sie berücksichtigt neueste Studienergebnisse und praxisrelevante Aspekte, um die Therapiequalität und Patientensicherheit in der Intensivmedizin zu optimieren.
Seit der Veröffentlichung der Kidney Disease: „Improving Global Outcomes“-(KDIGO-)Kriterien im Jahr 2012 [2] wird international und zunehmend auch in der deutschsprachigen Literatur der Anglizismus Acute Kidney Injury (AKI) synonym für die akute Nierenschädigung genutzt.
Daran orientiert sich auch die vorliegende Leitlinie: Eine AKI liegt demnach vor, wenn mindestens eines der drei KDIGO-Kriterien erfüllt ist. Diese umfassen einen Anstieg des Serumkreatinins um mindestens 0,3 mg/dl (26,5 µmol/l) innerhalb von 48 Stunden, einen Anstieg des Serumkreatinins auf mindestens das 1,5-Fache eines bekannten oder angenommenen Ausgangswerts innerhalb von sieben Tagen oder einen Abfall der Urinausscheidung auf weniger als 0,5 ml/kg Körpergewicht/h für mindestens sechs Stunden [2].
Je nach Ausprägung der Serumkreatininkonzentration und der verbleibenden Urinausscheidung lässt sich der Schweregrad der Nierenschädigung zudem in die Grade I bis III unterteilen.
Die Leitlinie
Die S3-Leitlinie „Nierenersatztherapie in der Intensivmedizin“ (QR-Code) der Arbeitsgemeinschaft der wissenschaftlichen medizinischen Fachgesellschaften e. V. (AWMF) ist die erste deutschsprachige evidenz- und konsensbasierte Empfehlungsübersicht für eine qualitativ hochwertige Versorgung kritisch kranker erwachsener Patientinnen und Patienten mit einer akuten Nierenschädigung oder einer extrakorporalen Nierenersatztherapie [1].
Federführend in der Leitlinienerstellung waren die Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin (DIVI), die Deutsche Gesellschaft für Internistische Intensivmedizin und Notfallmedizin (DGIIN) und die Deutsche Gesellschaft für Anästhesie und Intensivmedizin (DGAI). Alle drei Fachgesellschaften sind in der intensivmedizinischen Versorgung erwachsener Patienten national führend und beschäftigen sich im berufspraktischen Arbeitsalltag maßgeblich mit akutem Nierenversagen und Nierenersatzverfahren in der Intensivmedizin. Zur Leitliniengruppe gehören neun weitere Fachgesellschaften und Organisationen aus den Bereichen Pflege, Neurologie und Innere Medizin sowie zwei Vertretende der Patientenperspektive. Auf ins- gesamt 113 Seiten geben die Autorinnen und Autoren 73 Empfehlungen unter Einbeziehung, Bewertung und Diskussion aktuellster wissenschaftlicher Erkenntnisse.
Beginn der Nierenersatztherapie
Die Nierenersatztherapie soll bei Vorliegen lebensbedrohlicher Veränderungen des Flüssigkeits-, Säure-, Basen- oder Elektrolythaushalts unverzüglich begonnen werden. Beispielhaft zeigen sich zu diesem Zeitpunkt etwa Symptome wie eine therapieresistente Hyperkaliämie (>6,0 mmol/l) und eine Volumenüberladung (sichtbar durch eine pulmonalvenöse Stauung oder Ödeme) sowie die ebenfalls therapieresistente und durch das AKI bedingte Azidose (pH <7,2) oder eine Urämie – zum Beispiel in Form von Bewusstseinseinschränkungen. Diese Symptome machen die Entscheidung für die Therapieinitiierung unumstritten (starker Konsens).
Handelt es sich dagegen um nicht lebensbedrohliche Veränderungen oder ist unklar, ob aufgrund der aktuellen klinischen Situation (bisheriger Krankheitsverlauf und/oder bestehende Vorerkrankungen) ein AKI zu erwarten ist, sollten konservative Maßnahmen zur Vermeidung eines Nierenersatzverfahrens unter regelmäßiger Reevaluation erfolgen (starker Konsens, Empfehlung).
Als weitere Möglichkeiten zur Identifikation des passenden Startindikationszeitpunkts beschreibt die Literatur den Furosemid-Stresstest oder neuere renale Biomarker. Diese Tests oder Marker lassen sich jedoch in der aktuellen Leitlinie nicht (renale Biomarker; starker Konsens) oder nicht allein (negativer Furosemid-Stresstest; starker Konsens, Empfehlung) zur Indikationsstellung heranziehen.
Neben den konkreten Kriterien, die die Indikationsstellung für ein Nierenersatzverfahren definieren, ist in der aktuellen Literatur auch der ideale Startzeitpunkt innerhalb des zeitlich dynamischen Krankheitsverlaufs in der Diskussion, also ob ein frühzeitiger Beginn im Vergleich zu einem späteren Einsatz des Nierenersatzverfahrens zu einem verbesserten Patientenoutcome führt.
In den systematischen Übersichtsarbeiten lassen sich zum einen keine einheitlichen Definitionen von „früh“ oder „spät“ finden. Zum anderen nutzen die vorliegenden Studien die seit 2012 gültigen KDIGO-Stadien sehr uneinheitlich. So umfasst die Definition von „früh“ in diesen Arbeiten das KDIGO-Stadium 2 oder 3. Dieses gibt jedoch eher den Grad und weniger den Zeitpunkt an, ab dem eine Nierenersatztherapie starten soll. Aus diesem Grund enthält die S3-Leitlinie dazu keine Empfehlung.
Um jedoch der zeitlichen Dynamik einer lebensbedrohlichen Erkrankung gerecht zu werden, besteht laut den Autoren mittlerweile der Konsens, dass eine alleinige Graduierung als KDIGO 2 oder 3 nicht ausschließlich Anlass zur Initiierung einer Nierenersatztherapie sein sollte, sondern die AKI im Zusammenspiel mit den verschiedenen klinischen Komplikationen zu berücksichtigen ist. So kann bei isoliert erhöhten Serumwerten von Harnstoff oder Kreatinin ohne klinische Symptome mit dem Start eines Nierenersatzverfahrens abgewartet werden (starker Konsens, offene Empfehlung).
Ähnlich verhält es sich bei der schweren Rhabdomyolyse: Auch bei dieser sollte nur bei Vorliegen eines AKI mit der Indikation zur Nierenersatztherapie mit eben jener gestartet werden (starker Konsens, starke Empfehlung).
Dialyse- und Filtrationsverfahren
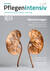
Die Leitlinie unterscheidet zwischen Dialysever- fahren, die die Diffusion als Mechanismus zur Entfernung von Stoffen aus dem Blut nutzen und Filtrationsverfahren, die die Konvektion nutzten (Tab. 1).
Die Dialyseverfahren auf Basis der Diffusion nutzen einen bestehenden Konzentrationsgradienten zwischen dem Blut des Patienten und dem Dialysat. Dadurch lassen sich verschiedene gelöste Stoffe sowie auch optional Wasser über die Membran entfernen (Ultrafiltration). Mit Verzicht auf die Ultrafiltration ermöglicht die damit einhergehende geringe Hämokonzentration auf der Blutseite eine sehr effektive und schnelle Entfernung kleiner Moleküle (0–3 kDa). Deshalb kommen diese Verfahren häufig intermittierend oder auch mit geringen Blut- und Dialysatflussraten kontinuierlich zur Anwendung.
Mit einem Filtrationsverfahren lassen sich hingegen die im Plasma gelösten Stoffe über ein Ultrafiltrat des Blutplasmas entfernen. Im Vergleich zur Diffusion führt die Konvektion zu einer höheren Clearance im Mittelmolekülbereich (2–30 kDa), die von der Molekülgröße, der Porengröße der Membran, der Ultrafiltrationsrate und der Behandlungszeit abhängt.
Um das überschüssig entfernte Wasser oder Stoffe, die nicht entfernt werden sollen (zum Beispiel Magnesium, Natrium, Bikarbonat), zu ersetzen, sind blutseitig entsprechende Substitutionslösungen zu nutzen. Diese lassen sich sowohl vor dem Filter als Prädilution, nach dem Filter als Postdilution oder auch in Kombination mit dem Blut zuführen. Die Leitlinie bewertet beide Dilutionsmöglichkeiten beim konvektiven Verfahren als gleichermaßen geeignet, wenngleich eine Bevorzugung der Prädilution bei vermehrtem Filterclotting erfolgen kann (starker Konsens, offene Empfehlung).
Mit Blick auf die unterschiedlichen Verfahren kommen die Autoren der Leitlinie zu der Schlussfolgerung, dass bei Patienten mit AKI und der vorliegenden Indikation zur Nierenersatztherapie auf der Intensivstation alle drei Verfahrensarten (diffusive Verfahren, konvektive Verfahren sowie Hybridverfahren) gleichermaßen einzusetzen sind (starker Konsens, starke Empfehlung).
So ließen sich etwa in den gesichteten Studien und Übersichtsarbeiten keine Unterschiede in Abhängigkeit des genutzten Verfahrens hinsichtlich verschiedener Outcome-Parameter (zum Beispiel Mortalität oder Erholung der Nierenfunktion) feststellen. Auch bei Patienten mit einer Sepsis und der Indikation zur Nierenersatztherapie sollten alle drei Verfahren gleichermaßen Anwendung finden (starker Konsens, starke Empfehlung).
Anders verhält es sich bei einer schweren, lebensbedrohlichen Hyperkaliämie. Für diese ist, sofern verfügbar, ein diffusives Verfahren mit hohen Dialysatflüssen dem konvektiven Verfahren vorzuziehen (starker Konsens), da insbesondere durch die physikalische Effektivität im Zuge der Diffusion eine rasche Clearance kleiner Moleküle wie Kalium, Laktat oder Harnstoff aus dem Blut erfolgen kann.
Mit einer sehr schnellen Clearance und somit der Entfernung weiterer Osmolyte wie etwa Natrium, Glukose oder auch Harnstoff aus dem Blut geht bei diffusiven Verfahren das potenzielle Risiko eines intrakraniellen Druckanstiegs einher (Dialyse-Dysäquilibrium-Syndrom), vor allem zu Beginn einer Nierenersatztherapie.
Aus pathophysiologischer Sicht ließe sich dies durch eine osmotisch bedingte Entstehung von Hirnödemen erklären, die sich symptomatisch durch Kopfschmerzen, Übelkeit und Erbrechen bis hin zu Bewusstseinseinschränkungen und zerebralen Krampfanfällen bemerkbar macht. Die wenigen im Zuge der Leitlinienerstellung zu diesem Thema gefundenen Arbeiten zeigen keine Unterschiede in der zerebralen Wasserverschiebung bei den unterschiedlichen Verfahrensarten. Somit kann auch die Autorengruppe keine Empfehlung zur Präferenz von Diffusion oder Konvektion in Bezug auf das Risiko eines intrakraniellen Druckanstiegs geben (starker Konsens, offene Empfehlung).
Besteht jedoch bereits ein erhöhter intrakranieller Druck, sollen die Patienten mit einem adaptierten und an die Osmolarität angepassten Nierenersatzverfahren behandelt werden. Damit einher geht die regelmäßige Überwachung der Osmolarität sowie der Osmolyte (Natrium, Harnstoff und Glukose) mit validierten Bestimmungsmethoden (starker Konsens).
Kontinuierliche und intermittierende Nierenersatzverfahren
Für die Nierenersatztherapie lassen sich neben den Verfahrensweisen auch die Behandlungsdauer pro Tag und die Intensität der Blutreinigung pro Zeiteinheit unterscheiden. Die Autoren der Leitlinie ziehen häufig einen Vergleich zwischen der kontinuierlichen Nierenersatztherapie (CRRT) und der intermittierenden Nierenersatztherapie/Hämodialyse (IHD):
- Die CRRT läuft unter idealen Bedingungen über 24 Stunden unterbrechungsfrei.
- Die IHD dauert vier bis sechs Stunden pro Tag.
- Die prolongierte intermittierende Nierenersatztherapie (PIRRT), in Deutschland unter dem Begriff der Sustained Low-Efficient Dialysis (SLED) geläufiger, hat eine Laufzeit zwischen sechs und zwölf Stunden.
Welches Verfahren letztlich zum Einsatz kommt, ist stets unter Berücksichtigung der individuellen klinischen Situation des Patienten zu entscheiden:
- Zur Negativbilanzierung bei Flüssigkeitsüberladung (starker Konsens) oder auch bei Patienten mit Thrombozytopenie (Konsens, offene Empfehlung) kann jedes der drei Verfahren zum Einsatz kommen.
- Für hämodynamisch instabile Patienten eignen sich am ehesten kontinuierliche oder (soweit verfügbar) prolongiert intermittierende Verfahren (Konsens, Empfehlung).
Die Entscheidung für die letztgenannte Vorgehensweise lässt sich mit der besseren hämodynamischen Steuerung und einer geringeren Hypotonierate begründen. So können einzelne Verfahren bevorzugt bei individuellen Symptomkonstellationen zum Einsatz kommen.
Wenngleich die Leitlinie keine Unterschiede zwischen den kontinuierlichen oder intermittierenden Verfahren hinsichtlich des Endpunkts der Nierenfunktionserholung (Konsens, offene Empfehlung) oder der Sicherung des Überlebens des Patienten (starker Konsens, offene Empfehlung) macht, eignen sich beide Verfahren gleichermaßen.
Pflegerische Aspekte
Der Einsatz eines kontinuierlichen Nierenersatzverfahrens mit einliegenden Dialysekathetern und Schläuchen, die die Mobilisierbarkeit des Patienten beeinträchtigen, soll die Frühmobilisation des Patienten nicht verhindern oder verzögern (starker Konsens, starke Empfehlung).
Für die IHD bietet sich eine Mobilisation in den dialysefreien Intervallen an. Um eine sichere Mobilisation des Patienten während der laufenden Nierenersatztherapie zu ermöglichen, sollten prozedurale Anweisungen zum pflegerischen und physiotherapeutischen Umgang mit diesem Patientenklientel vorliegen, die mit dem DIVI-Qualitätsindikator IX (Frühmobilisation) in Einklang stehen, und es sollten multiprofessionelle Schulungen zur fachspezifischen Pflege im Zusammenhang mit der Nierenersatztherapie erfolgen (starker Konsens).
Regionale und systemische Antikoagulation
Eine effektive Antikoagulation des extrakorporalen Kreislaufs gewährleistet eine effiziente extrakorporale Nierenersatztherapie ohne frühzeitige oder ungeplante Therapieunterbrechungen. Für die Antikoagulation stehen zwei Ansätze zur Verfügung, die hinsichtlich der Patienten-Outcomes – Mortalität, Erholung der Nierenfunktion und Transfusionsfrequenz – sowie des Einflusses der regionalen oder systemischen Antikoagulation auf eben diese als gleichwertig anzusehen sind (starker Konsens, Empfehlung).
Eine effektive Antikoagulation des extrakorporalen Kreislaufs kann einerseits über eine systemische Antikoagulation erfolgen, etwa durch unfraktioniertes oder fraktioniertes Heparin. Aufgrund des einfacheren Monitorings und der kürzeren Halbwertszeit empfehlen die Leitlinienautoren jedoch die Verwendung von unfraktioniertem Heparin (starker Konsens, offene Empfehlung).
Bei einer akuten Heparin-induzierten Thrombozytopenie Typ II können Argatroban oder Danaparoid zur systematischen Gerinnungssteuerung zur Anwendung kommen. Eine adäquate Dosierung von Argatroban kann auch allein zur Antikoagulation des Nierenersatzverfahrens dienen, um eine effektive Filterlaufzeit ohne eine erhöhte Blutungsrate zu erreichen (starker Konsens, offene Empfehlung).
Andererseits kann Citrat eine regionale Antikoagulation initiieren und so eine erfolgreiche extrakorporale Therapie ermöglichen, ohne die systemische Hämostase des Patienten zu beeinflussen. Diese Form der Antikoagulation sollte insbesondere bei Patienten mit erhöhtem Blutungsrisiko oder bei solchen, bei denen aufgrund von Kontraindikationen die Anwendung von Heparin nicht indiziert ist, zum Einsatz kommen (starker Konsens, Empfehlung).
Auch kann ein Wechsel auf die Citrat-Antikoagulation erfolgen, wenn eine Behandlung mit systematischer Heparin-Antikoagulation aufgrund verkürzter Filterlaufzeiten nicht wie geplant möglich ist (starker Konsens, Empfehlung).
Beim Einsatz der regionalen Citrat-Antikoagulation bleibt eine regelmäßige Kontrolle der Elektrolyte – insbesondere von Natrium, Gesamt- und ionisiertem Calcium im Serum – sowie der Säure-Base-Parameter (Blut-pH, HCO3 und Laktat) notwendig (Konsens).
Nur so lassen sich frühzeitig optionale Abweichungen erkennen und Schwankungen des Serum-Calciums (Hyper- oder Hypokaliämie) oder des Säure-Basen-Haushalts (metabolische Alkalose oder Azidose) identifizieren. Kommt es im Verlauf zu einer refraktären Akkumulation des Citrats, die sich in Form einer metabolischen Azidose mit erhöhter Anionenlücke sowie einer Hyperkaliämie zeigt, ist die regionale Citrat-Antikoagulation gegebenenfalls auch ohne Antikoagulation auf ein Bikarbonat-gepuffertes Verfahren umzustellen (starker Konsens, starke Empfehlung).
Gerade durch die überwiegende Metabolisierung des Citrats in der Leber sind Patienten mit einer Laktatazidose oder schwerem Leberversagen besonders gefährdet, eine Citrat-Akkumulation zu erleiden. Trotz des erhöhten Risikos stellt die regionale Citrat-Antikoagulation bei diesem Patientenklientel keine absolute Kontraindikation dar, solange das Laktat sowie das ionisierte oder das Gesamtcalcium des Patienten regelmäßig gemonitort werden können (Konsens, offene Empfehlung).
Liegen jedoch eine ausgeprägte, progrediente Laktatazidose im Rahmen eines Schocks sowie ein schweres Leberversagen vor, sollte möglichst keine regionale Antikoagulation mit Citrat erfolgen (starker Konsens, Empfehlung).
Dosis des Nierenersatzverfahrens
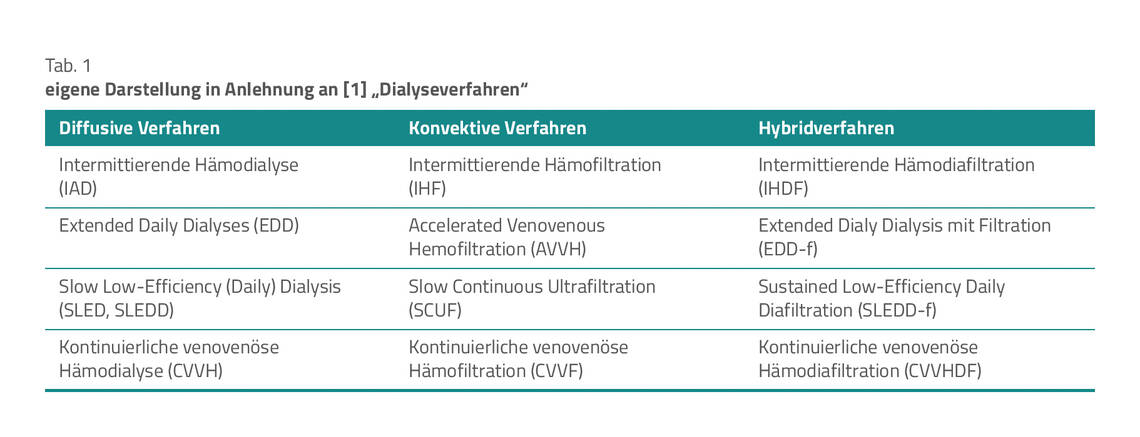
Zur Steuerung der Intensität des Nierenersatzverfahrens lässt sich die applizierte Dialyse- oder Filtrationsdosis heranziehen. Diese ergibt sich aus der Menge des Substituats oder des Dialysats inklusive des Flüssigkeitsentzugs pro Zeiteinheit. Die zugrunde liegende Berechnungsformel für die korrekte Dosis in ml/kg/h variiert je nach Dialyseart (Tab. 2). Je höher die Dosis ausfällt, desto mehr Stoffe können den Filter passieren und somit eliminiert werden. Für ein kontinuierliches Nierenersatzverfahren ist eine Dosis von 20–25 ml/kg/h über die geplante Behandlungsdauer zu verabreichen (starker Konsens, starke Empfehlung).
Die Autoren empfehlen außerdem, die tatsächlich verabreichte mittlere Dosis der Nierenersatztherapie regelmäßig, jedoch mindestens einmal pro Tag, zu protokollieren und die Anpassungen oder die klinische Effektivität der Therapie im Verlauf anhand labordiagnostischer und klinischer Parameter – unter anderem Elektrolyte, Säure-Basen-Haushalt, Harnstoff – zu überprüfen (starker Konsens).
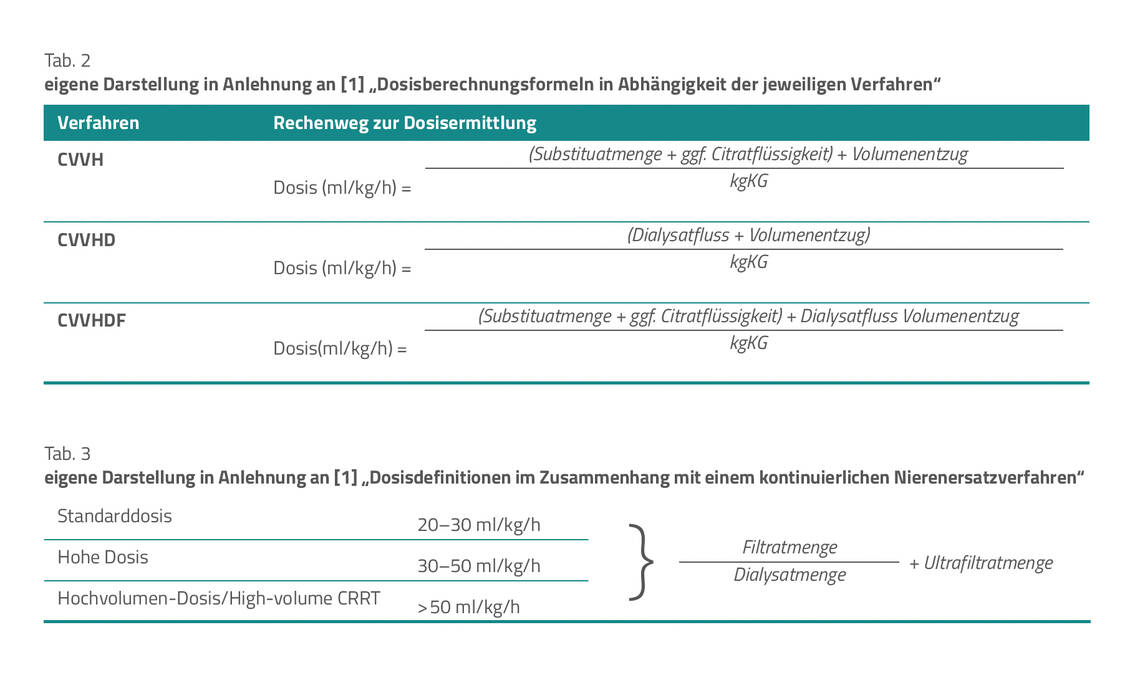
Mit Blick auf die Praxis scheint dies besonders dahingehend bedeutsam, da Unterbrechungen in der Nierenersatztherapie – zum Beispiel durch Transporte, Operationen oder auch den regelhaften Wechsel von Dialysesets oder Filtern – die Kontinuität und somit auch die Effektivität der Behandlung beeinflussen. Um diesen Einflüssen entgegenzuwirken, ist die verschriebene Dosis in der Praxis häufig etwas höher als die berechnete Zieldosis. Dabei können unterschiedliche Definitionen für das kontinuierliche Verfahren zur Anwendung kommen (Tab. 3). Der Einsatz einer kontinuierlichen hochvolumigen (high-volume) Hämofiltration bei Patienten mit einem septischen Schock oder einer Sepsis ist in der Leitlinie nicht empfohlen (starker Konsens, offene Empfehlung).
Für die Festlegung der idealen Dosis bei intermittierenden Verfahren empfehlen die Autoren, dies unter Berücksichtigung der genutzten Dialysator- Membran, des Blutflusses, des Dialysatflusses sowie gegebenenfalls des Filtrationsvolumens bei der Hämofiltration vorzunehmen. In welchen Abständen oder über welchen Behandlungszeitraum das Verfahren zur Anwendung kommt, bestimmen – ähnlich wie bei der kontinuierlichen Nierenersatztherapie – labordiagnostische und klinische Variablen (starker Konsens).
Anders als bei den kontinuierlichen Verfahren kann keine konkrete Dosisempfehlung auf Grundlage der verfügbaren Literatur erfolgen. Die Autoren empfehlen daher insbesondere bei einem dynamischen Krankheitsverlauf eines kritisch kranken Patienten, ein individuelles Dosisziel für jede einzelne Dialysebehandlung festzulegen.
Pharmakotherapie unter Nierenersatztherapie
Wie schnell ein Arzneimittel vom Körper physiologisch verstoffwechselt wird und welche Menge eines Medikaments erforderlich ist, um einen therapeutischen Zielbereich zu erreichen, hängt unter anderem von der Funktion der Organe Nieren, Leber, Gastrointestinaltrakt oder der Lunge ab.
Kommt im Zuge eines akuten Nierenversagens ein entsprechendes Ersatzverfahren hinzu, so errechnet sich die Clearance eines Arzneimittels aus der endogenen und der maschinellen Clearance. Um die medikamentöse Therapie zielgerichtet steuern zu können, empfehlen die Autoren, neben der Erfassung patientenseitiger Faktoren, die die Pharmakokinetik beeinflussen – dazu zählen Größe, Gewicht, Nierenrestfunktion, Proteinstatus und Flüssigkeitsüberladung –, auch die entsprechenden pharmakokinetischen und -dynamischen Eigenschaften des Medikaments bei der Dosisbestimmung zu berücksichtigen (starker Konsens).
So soll sich die Startdosis des Antiinfektivums nach dem aktuellen Verteilungsvolumen im Körper richten, den allgemeinen Dosisempfehlungen entsprechen und nicht in reduziertem Maße verordnet werden (starker Konsens).
Um dann eine schnelle Aufsättigung und eine wirksame Wirkstoffkonzentration zu erreichen, ist die Startdosis als Kurzinfusion zu verabreichen, auch wenn im weiteren Verlauf prolongierte oder kontinuierliche Gaben geplant sind (starker Konsens, starke Empfehlung). Anschließend kann anhand evidenzbasierter, anerkannter Tabellenwerke und eines therapeutischen Drug Monitorings (TDM) eine individuelle Erhaltungsdosis ermittelt werden (starker Konsens, offene Empfehlung).
Insbesondere bei Antibiotika wie ß-Lactamen, Vancomycin und Aminoglykosiden sollte ein TDM erfolgen (starker Konsens, Empfehlung). Über eine Anpassung der Bestimmungszeitpunkte unter Berücksichtigung der verordneten Applikationsform und unter Sicherstellung reproduzierbarer Abnahmeschemata kann eine Einordnung der ausgewählten Parameter in Abgleich mit dem zuvor definierten therapeutischen Zielbereich erfolgen (starker Konsens).
Dabei kann die zuvor erwähnte prolongierte oder kontinuierliche Gabe zeitabhängiger Antiinfektiva in Verbindung mit oder unter Steuerung eines TDM bei Patienten mit einem kontinuierlichen Nierenersatzverfahren zu einem zuverlässigen Erreichen definierter Zielbereiche (Target-Attainment) führen. Daher ist sie einer Kurzinfusion vorzuziehen (starker Konsens, offene Empfehlung).
Im Rahmen der IHD kann jedoch die Gabe eines zeitabhängigen Antiinfektivums als Kurzinfusion oder als prolongierte kontinuierliche Applikation vorgezogen werden (starker Konsens). Ebenso kann auch nach Abschluss der IHD unter Berücksichtigung evidenzbasierter, anerkannter Tabellenwerke eine notwendige Zusatzdosis zur Wiederherstellung eines adäquaten Antiinfektiva-Spiegels erfolgen (starker Konsens).
Elimination von exogenen Substanzen
Vor der Einleitung einer Toxineliminierung mithilfe eines extrakorporalen Verfahrens ist zunächst zu überprüfen, inwiefern die notwendigen Voraussetzungen für den Therapiebeginn vorliegen. Neben der grundsätzlichen Dialysierbarkeit der Substanz sollte zudem eine hinreichende Effizienz absehbar sein. Dazu sollte sich >30 Prozent der im Körper befindlichen Menge der Substanz entfernen lassen oder ein Verhältnis >75 Prozent extrakorporaler Clearance zur Gesamtclearance muss zu erreichen sein. Eine Nierenersatztherapie kann dabei sinnvoll sein, wenn die endogene Clearance – etwa bei Vorliegen einer akuten oder chronischen Nierenerkrankung – nicht ausreicht und eine klinisch relevante maschinelle Clearance gegeben ist (starker Konsens).
Die Effektivität der maschinellen Clearance wird hierbei jedoch maßgeblich von der Größe des Moleküls, seiner Proteinbindung und seinem Verteilungsvolumen im Körper beeinflusst. Daher sollte das Molekül hinreichend klein sein und eine geringe bis moderate aktuelle Proteinbindung aufweisen, um eine Filtermembran passieren zu können. Zudem muss es über ein hinreichendes Verteilungsvolumen verfügen und im Plasmakompartiment erreichbar sein (starker Konsens).
Eine von den Autoren erwähnte Indikation für den Einsatz eines Nierenersatzverfahrens zur Elimination exogener Substanzen (Medikamente/Gifte) besteht bei einer lebensbedrohlichen Lithiumvergiftung oder wenn klinische Indikationen wie Bewusstseinseinschränkungen, Krämpfe oder bedrohliche Herzrhythmusstörungen vorliegen (starker Konsens, starke Empfehlung).
Bei einer Lithiumvergiftung besteht die Indikation für eine extrakorporale Therapie insbesondere dann, wenn die Lithiumkonzentration bei eingeschränkter Nierenfunktion >4 mmol/l liegt (starker Konsens, starke Empfehlung). Ebenso gilt dies, wenn die Lithiumkonzentration 5 mmol/l übersteigt und der Patient aufgrund der Vergiftung verwirrt ist oder wenn er voraussichtlich >36 Stunden benötigt, um einen Lithiumspiegel von <1 mmol/l zu erreichen (starker Konsens, Empfehlung).
Als primäres Verfahren kann dazu die IHD eingesetzt werden. Ist diese nicht verfügbar, kommt alternativ eine SLED in Betracht (starker Konsens, Empfehlung). Fällt der Lithiumspiegel im Behandlungsverlauf <1 mmol/l, verbessert sich die Vigilanz des Patienten klinisch signifikant oder sind sechs Stunden Dialyse verstrichen, kann die Nierenersatztherapie aus Sicht der Autoren enden (starker Konsens, offene Empfehlung). Um im Anschluss einen möglichen Rebound frühzeitig erkennen zu können, ist zwölf Stunden nach Ende der Therapie erneut der Lithiumspiegel zu bestimmen (starker Konsens, starke Empfehlung).
Ist eine erneute Rebound-Therapie notwendig, können dann sowohl intermittierende als auch verlängert intermittierende und kontinuierliche Verfahren Anwendung finden (starker Konsens, offene Empfehlung).
Beendigung des Nierenersatzverfahrens
Die bisherigen Leitlinien können die Frage, wann ein Nierenersatzverfahren beendet werden kann, nicht beantworten, da es an ausreichenden Daten fehlt. Die Autoren dieser Leitlinie versuchen, diese Lücke zu schließen, können jedoch zur Untermauerung ihrer Empfehlungen auch nur auf begrenzte Studienergebnisse zurückgreifen. Dennoch stimmen alle Beteiligten zu, dass ein Zeitraum von sieben Tagen mit stabiler Nierenfunktion als Maßstab für eine primär erfolgreiche Beendigung dienen kann (starker Konsens).
Als ein prädiktiver Marker wird auf die Diuresemenge des Patienten verwiesen (starker Konsens, Empfehlung). Diese ist orientierend mit einer Mindestmenge von 300–600 ml/d angegeben, wobei es sich um ein spontane Diurese ohne Diuretika handelt.
Eine weitere Präzisierung ist aktuell nicht möglich (starker Konsens, offene Empfehlung). Unterstützend können bei der Beendigung der Nierenersatztherapie auch Diuretika zum Einsatz kommen, um die Diuresemenge zu erhöhen (Konsens, offene Empfehlung).
Mit Blick auf die laborchemischen Parameter kommen die Autoren zu dem Ergebnis, dass Kreatinin im Serum nicht als unabhängiger prädiktiver Marker genutzt werden sollte, solange die entsprechende Serumanalyse im unmittelbaren zeitlichen Zusammenhang mit dem Nierenersatzverfahren oder der maschinellen Clearance steht (starker Konsens).
Auch wenn mittlerweile einige Arbeiten verschiedene neue Schädigungs- oder Funktionsmarker als prädiktive Marker für die Beendigung der Nierenersatztherapie untersucht und beschrieben haben, so können die Autoren in dieser Leitlinie keine Empfehlung für oder gegen den Einsatz dieser Marker geben (starker Konsens, offene Empfehlung).
Anders sieht es bei der kinetischen GFR aus, die auf der endogenen Clearance basiert und als prädiktiver Faktor Hinweise zur endogenen Entgiftungsleistung der Niere gibt (starker Konsens, offene Empfehlung).
Ein protokollbasiertes Weaning kann ebenfalls als Methode zum Absetzen der Nierenersatztherapie dienen, wenngleich die Leitlinienautoren aktuell noch keine etablierten Protokolle mit spezifischen Variablen empfehlen können (starker Konsens, offene Empfehlung).
Eine persistierende Hyperkaliämie (>5,5 mmol/l) kann auf ein erhöhtes Risiko für ein Weaningversagen hinweisen. Deshalb sollte sie vor dem Weaningversuch differenzialdiagnostisch untersucht werden (starker Konsens, offene Empfehlung).
Gleiches gilt für eine persistierende metabolische Azidose (pH <7,3), die ebenfalls abgeklärt und vor einem Weaningversuch therapiert werden sollte (starker Konsens, Empfehlung), sowie für die notwendige Korrektur einer bestehenden Flüssigkeitsüberladung (starker Konsens, Empfehlung).
Nachsorge des Patienten
Die Leitlinienautoren erachten eine ambulante ärztliche Nachsorge von Patienten mit überstandenem AKI für zwei bis vier Wochen nach der Entlassung für erforderlich, sofern eine Nierenfunktionseinschränkung mit einer reduzierten GFR vorliegt. Bei Patienten mit guter Erholung nach dem AKI (GFR >60 ml/min) halten sie eine Nachsorge nach etwa drei bis sechs Monaten für angemessen (starker Konsens).
[1] Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin (DIVI), Deutsche Gesellschaft für Internistische Intensivmedizin und Notfallmedizin (DGIIN), Deutsche Gesellschaft für Anästhesie und Intensivmedizin (DGAI). S3-Leitlinie „Nierenersatz in der Intensivmedizin“. Version V1.0 vom 12. März 2025. Im Internet: register.awmf.org/de/leitlinien/detail/040-017; Zugriff: 13. April 2025
[2] Bienholz A, Kribben A. KDIGO-Leitlinien zum akuten Nierenversagen. Deutsche Übersetzung. Der Nephrologe 2013; 8: 247–251. doi: 10.1007/s11560-013-0752-1