Die im Sommer veröffentlichte überarbeitete S1-Leitlinie „Atemwegsmanagement 2023“ ersetzt die Vorgängerversion aus dem Jahr 2015. Der Autor stellt einige der Empfehlungen und Hintergründe vor.
Inhaltlich bezieht sich die Leitlinie (Textkasten: Die Leitlinie) auf anästhesiologisch und intensivmedizinisch betreute erwachsene Patientinnen und Patienten [1].
Die Leitlinie
Im August 2023 veröffentlichte die Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin (DGAI) als federführende Fachgesellschaft die S1-Leitlinie „Atemwegsmanagement 2023“. Die Leitlinie ist ausschließlich als Langversion verfügbar, hat einen Umfang von 86 Seiten und steht auf der Website der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) kostenlos als Download zur Verfügung [1].
Wichtig zu wissen: Für die Sicherung der Atemwege in der Präklinik, Polytrauma-/Schwerverletztenbehandlung sowie Kinderanästhesie wird auf bestehende Handlungsempfehlungen beziehungsweise Leitlinien verwiesen [2, 3, 4].
Adressaten und Patientenzielgruppe. Die Leitlinie richtet sich an Ärztinnen und Ärzte der Anästhesiologie sowie an Fachpflegende aus der Anästhesie und anästhesietechnische Assistentinnen und Assistenten. Die Patientenzielgruppe sind Erwachsene, die im Rahmen ihrer ambulanten oder stationären Behandlung eine anästhesiologische Versorgung mit Sicherung der Atemwege benötigen.
Relevanz. Den Autorinnen und Autoren zufolge ist die Sicherung der Atemwege eine Kernkompetenz von Anästhesiologinnen und Anästhesiologen, Intensiv- und Notfallmedizinerinnen sowie -medizinern, da ohne offene oder gesicherte Atemwege keine Oxygenierung möglich ist. Die Einführung neuer Techniken und die Implementierung von Leitlinien und Strategien zur Versorgung des schwierigen Atemwegs haben Morbidität und Letalität wesentlich gesenkt. Ziel der Leitlinie ist die Gewährleistung einer optimalen Versorgung der anästhesiologisch und intensivmedizinisch betreuten Patienten. Sie soll den Anwenderinnen und Anwendern zur Orientierung sowie als Entscheidungshilfe dienen [1].
Anspruch und Realität klaffen oft deutlich auseinander. Eine Untersuchung der Amerikanischen Gesellschaft für Anästhesiologie (ASA) wertete atemwegsbezogene abgeschlossene Haftpflichtfälle (sogenannte Closed-Claims) aus. Zwei Patientenkollektive wurden dabei verglichen, eines umfasste den Zeitraum 1993– 1999, das andere den Zeitraum 2000–2012. Im jüngeren Zeitraum kam es zu deutlich mehr Todesfällen, bei 73 Prozent davon wurde ein inadäquates Atemwegsmanagement festgestellt [7]. Eine Studie aus Dänemark zeigte, dass bei den Fällen, die eine notfallmäßige chirurgische Atemwegssicherung erforderten, in lediglich 37 Prozent ausreichende nichttechnische Fertigkeiten gegeben waren [8].
Wichtig zu wissen: Laut Europäischem Rat für Wiederbelebung (ERC, European Resuscitation Council) sind die nichttechnischen Fertigkeiten definiert als die kognitiven und zwischenmenschlichen Fertigkeiten, die zur effektiven Arbeitsleistung des Teams beitragen. Sie beinhalten Fertigkeiten wie die Kommunikation, die Fähigkeit, eine Teamleiterin, ein Teamleiter oder -mitglied zu sein, sowie die kognitiven Prozesse der Entscheidungsfindung, situativen Aufmerksamkeit und Aufgabenverteilung. Nach Schätzungen des ERC beruhen 70–80 Prozent der Zwischenfälle im Gesundheitswesen auf einem Mangel an diesen Fertigkeiten [9].
Empfehlungsgrade. Wie auch in anderen AWMF-Leitlinien werden die Formulierungen „soll/soll nicht“, „sollte/sollte nicht“ sowie „kann erwogen werden/kann verzichtet werden/ist unklar“ verwendet (Tab.) [6]. Da es sich bei der hier besprochenen S1- Leitlinie um einen Konsens und daraus abgeleitete Stärken der Empfehlungen durch eine Expertengruppe handelt, ist es nicht möglich, einen Empfehlungsgrad (GoR, Grade of Recommendation) anzugeben.
Aufbau der Leitlinie. Die Leitlinie ist in 14 Abschnitte unterteilt und enthält drei Abbildungen in Form eines Algorithmus.
Wichtig zu wissen: Nach [7] zeigen Algorithmen „... die Lösung für ein Problem auf. In konkreten Einzelschritten wird die Vorgehensweise vorgezeichnet, basierend auf Wenn-Dann-Entscheidungen. Für das Atemwegsmanagement ist ein Algorithmus eine Handlungsanweisung, die im Notfall Sicherheit geben kann.“
Definition schwieriger Atemweg
Die Leitlinie fasst unter dem Begriff „schwieriger Atemweg“ Probleme zusammen, die während der Atemwegssicherung auftreten können. Zur Beurteilung des schwierigen Atemwegs wird als Qualifikation der Facharztstandard Anästhesiologie vorausgesetzt. Alle Empfehlungen der Leitlinie beziehen sich auf den Facharztstandard und ausreichende Erfahrung in der routinemäßigen Anwendung der jeweiligen Technik.
Ebenen der Atemwegssicherung. Der Leitlinie zufolge gibt es vier Ebenen mit möglichen Zugängen für eine Oxygenierung oder Ventilation des Patienten:
- Ebene 1: Spontanatmung, unterstützte oder kontrollierte Beatmung mit einer Gesichtsmaske
- Ebene 2: Verwendung einer supraglottischen Atemwegshilfe
- Ebene 3: Platzierung eines Endotrachealtubus in der Trachea
- Ebene 4: Translaryngealer/transtrachealer Zugang
Basierend auf den vorgenannten Ebenen können folgende Schwierigkeiten auftreten:
- Oxygenierung mithilfe der Gesichtsmaske oder einer supraglottischen Atemwegshilfe (SGA). Wird als schwierig oder unmöglich definiert, wenn aufgrund eines Problems oder mehrerer Probleme das Ausgangsniveau der Sauerstoffsättigung nicht zu erreichen ist.
- Platzieren einer supraglottischen Atemwegshilfe. Gilt laut Leitlinie als schwierig, wenn mehr als zwei Versuche zur korrekten Platzierung notwendig sind.
- Laryngoskopie. Gilt als unmöglich, wenn die Glottis (durch die Stimmlippen gebildete Stimmritze) nicht zu visualisieren ist, was einem Laryngoskopiebefund gemäß Cormack-Lehane-Grad III oder IV entspricht.
- Endotracheale Intubation. Wird als schwierig bezeichnet, wenn mehr als zwei Intubationsversuche notwendig sind.
- „Cannot ventilate, cannot oxygenate“-Situation. Besteht laut Leitlinie, wenn weder eine Ventilation noch eine Oxygenierung möglich ist.
Inzidenzen und Prädiktoren. Den Leitlinienautoren zufolge ist es bisher nicht eindeutig möglich, die Komplikationen und Inzidenzen einer schwierigen Maskenbeatmung, Laryngoskopie oder Intubation zu beziffern, weil in den verschiedenen Studien einerseits die Definition des schwierigen Atemwegs und andererseits auch die zugrunde liegende Situation (zum Beispiel Elektiveinleitung im OP versus Notfallintubation auf einer Intensivstation) sehr unterschiedlich ist.
In etwa 6 Prozent ist die Maskenbeatmung erschwert, in etwa 0,04–0,15 Prozent unmöglich, wobei dies in einer Größenordnung von etwa 90 Prozent unerwartet auftrat [1]. Die Inzidenz der schwierigen direkten Laryngoskopie wird mit 1,5–8,0 Prozent angegeben, die der schwierigen Intubation ist etwas niedriger. Laut Leitlinie ist mit einer Wahrscheinlichkeit von 0,008 Prozent (1:13.000) bis 0,004 Prozent (1:25.000) mit einer unerwarteten „cannot intubate, cannot oxygenate“-Situation zu rechnen.
Die Autoren der Leitlinie weisen darauf hin, dass auch mögliche interindividuelle Unterschiede der praktischen Fertigkeiten der Untersuchenden zu berücksichtigen sind. Da der Facharztstandard die individuelle Kompetenz nur unscharf beschreibt, ist es anzunehmen oder sogar wahrscheinlich, dass verschiedene Arbeitsgruppen bei einem identischen Patientenkollektiv zu unterschiedlichen Ergebnissen gelangen. Der Leitlinie zufolge ist diese Problematik bei der Interpretation klinischer Studien immer mit zu berücksichtigen [1].
Wichtig zu wissen: Da die Humanmedizin eine Erfahrungswissenschaft ist, kann die Expertise von Facharzt zu Facharzt sehr unterschiedlich sein. In Untersuchungen bleiben die sogenannten Menschlichen Faktoren (Human Factors) und das Krisenressourcenmanagement (CRM, Crisis Resource Management) oftmals unberücksichtigt [7].
Ausgewählte Empfehlungen
Mit Unterteilung der Leitlinie in 14 themenbezogene Abschnitte entsteht eine Struktur, die ein rasches Auffinden der benötigten Informationen ermöglicht. Es liegt in der Natur der Sache, dass dementsprechend Informationen und Empfehlungen – beispielhaft sei die Kapnografie genannt – an verschiedenen Stellen der Leitlinie auftauchen. Die Vorstellung und Besprechung ausgewählter Empfehlungen in diesem Beitrag können daher nicht alle Aspekte vollständig beleuchten.
Empfehlung 1: „Im Rahmen der elektiven Aufklärung soll nach anatomischen und physiologischen Hinweisen für eine erschwerte Maskenbeatmung und Intubation gesucht werden: Mundöffnung, Zahnstatus, Protrusion des Unterkiefers, HWS-Beweglichkeit, Pathologien (Hals, Gesicht), bekannter schwieriger Atemweg, ggf. Berücksichtigung Bildgebung und HNO-Befund.“
Empfehlung 2: „Klinikintern soll es einen Algorithmus/Standard geben, der das Vorgehen bei bestehenden Prädiktoren des schwierigen Atemweges definiert. Scores können dabei verwendet werden.“
Die Leitlinie listet folgende „Prädiktoren für eine schwierige oder unmögliche Maskenbeatmung in alphabetischer Reihenfolge“ auf [1]:
- Bestrahlung oder Tumor im Bereich der Halsregion
- Body-Mass-Index >30 kg/m2
- Desolater Zahnstatus, Zahnlosigkeit
- Protrusion (deutlich eingeschränkter Vorschub) des Unterkiefers
- Makroglossie (Vergrößerung der Zunge) und andere pathologische Zungenveränderungen
- Mallampati-Grad III oder IV (Abschätzung des Schwierigkeitsgrads einer endotrachealen Intubation)
- Narben, Tumoren, Entzündungen, Verletzungen von Lippe und Gesicht
- Pathologische Veränderungen von Pharynx, Larynx und Trachea
- Schnarchanamnese beziehungsweise obstruktive Schlafapnoe
- Unzureichende Narkosetiefe
- Verringerter thyreomentaler (von Kinn bis Vorderseite Schildknorpel) Abstand (<6–7 Zentimeter)
- Vollbartträger
Neben den oben aufgeführten Faktoren ist auch die Anamnese des Patienten wichtig. Gab es bereits einmal eine erschwerte Maskenbeatmung oder gibt es Hinweise wie ein Anästhesieprotokoll oder einen Anästhesieausweis? Je mehr der aufgelisteten anatomischen Eigenschaften vorliegen, die auf eine erschwerte Maskenbeatmung hinweisen können, desto wahrscheinlicher ist das Auftreten von Problemen [1].
Der Begriff „schwierige Intubation“ wird oft als Sammelbegriff verwendet, ohne zwischen „Laryngoskopie“ und „endotrachealer Intubation“ zu unterscheiden. Daher sind nach Angabe der Autoren zwei Formen der Laryngoskopie zu differenzieren:
- direkte Laryngoskopie: Bei dieser Form ist diese Unschärfe des Sammelbegriffs von untergeordneter Bedeutung, weil sich anatomische und optische Achse annähern und ein akzeptabler Laryngoskopiebefund auch eine erfolgreiche Tubusplatzierung erwarten lässt.
- indirekte Laryngoskopie: Anders verhält es sich bei der Videolaryngoskopie, da hier die Häufigkeit der schwierigen Laryngoskopie grundsätzlich niedriger ist als die einer schwierigen oder unmöglichen Intubation [1].
Die Leitlinie listet folgende „Prädiktoren für eine schwierige oder unmögliche direkte Laryngoskopie in alphabetischer Reihenfolge“ auf [1]:
- Eingeschränkte Mundöffnung (<3,5 Zentimeter)
- Eingeschränkte Reklination des Kopfes
- Inspiratorischer Stridor (pathologisches Atem- geräusch infolge einer Verengung oder teilweiser Verlegung der Atemwege)
- Kurzer oder umfangreicher Hals
- Makroglossie
- Mallampati-Grad III oder IV
- Mandibulo- und maxillofaziale Dysostosen (Fehlbildungen einzelner Knochen oder Knochengruppen im Mund-Kiefer-Gesichts-Bereich)
- Obstruktive Schlafapnoe
- Pathologischer „Upper-Lip-Bite-Test“
- Progenie (Überbiss der unteren über die oberen Schneidezähne), Dysgnathie (angeborener oder erworbener Fehlbiss)
- Raumfordernde Struma (krankhaft vergrößerte Schilddrüse)
- Schwangerschaft
- Schwierige Intubation in der Anamnese
- Subglottische Stenose, Trachealstenose, Trachealverlagerung
- Tumoren, Abszesse im Kopf-Hals- oder Mediastinalbereich
- Unzureichende Narkosetiefe, fehlende muskuläre Blockade
- Verringerter thyreomentaler Abstand (<6–7 Zentimeter)
- Zustand nach Bestrahlung im Kopf-Hals-Bereich
- Zustand nach Operationen am Larynx/Pharynx
Die Leitlinienautoren weisen darauf hin, dass keiner der beschriebenen Tests oder Scores für sich allein geeignet ist, eine erschwerte Laryngoskopie oder Intubation sicher vorherzusagen. Ähnlich wie bei der schwierigen Maskenbeatmung gilt jedoch auch hier, dass mit zunehmender Anzahl von Prädiktoren die Wahrscheinlichkeit eines schwierigen Atemwegs ansteigt. Es kann jedoch auch ein einziger Prädiktor schon auf Probleme hinweisen, beispielsweise wenn eine sehr kleine Mundöffnung besteht.
Dem „Upper-Lip-Bite-Test“ (ULBT) wird ein wichtiger Stellenwert zugewiesen, da er eine gute Vorhersehbarkeit für die schwierige Intubation hat. Der ULBT beurteilt die Fähigkeit des Patienten, mit der unteren Zahnreihe die Oberlippe zu er- reichen oder vollständig zu bedecken [10]. Im klinischen Alltag sind andere Methoden am weitesten verbreitet, unter anderem der von Samsoon und Young modifizierte Mallampati-Test oder der thyreomentale Abstand nach Patil von weniger als 6–7 Zentimetern [1].
Empfehlung 4: „Der Nachweis einer korrekten Tubuslage kann durch eine Ultraschalluntersuchung der Trachea und beider Hemithoraces erfolgen.“
Empfehlung 5: „Bei bekannt oder erwartet schwierigem Atemweg kann präanästhesiologisch eine Ultraschalluntersuchung der oberen Atemwege mit Darstellung und Markierung der Membrana cricothyreoidea hilfreich sein, um für eine translaryngeale Sicherung der Atemwege vorbereitet zu sein.“
Der Leitlinie zufolge rückt die Untersuchung der Atemwege mittels Ultraschallverfahren zunehmend in den Fokus klinischer Studien, da das Verfahren viele Möglichkeiten bietet. Eine aktuelle Übersichtsarbeit fasst die verfügbare Evidenz für den Einsatz von Point-of-Care-Ultraschall im Umfeld der Atemwegssicherung zusammen [14]. Ultraschall ermöglicht ein schnelles Screening auf eine schwierige Laryngo-skopie und identifiziert die Cricothyreoidmembran für eine potenzielle translaryngeale Sicherung der Atemwege. Wenngleich sich die Cricothyreoidmembran bei den meisten Patienten durch Inspektion und Palpation auffinden lässt, trägt die Unfähigkeit, sie zu identifizieren, wesentlich zur hohen Fehlerquote bei der Cricothyreotomie bei.
Wichtig zu wissen: Die Cricothyreotomie ist ein invasiver Zugang (zum Beispiel mittels Skalpell) zu den Luftwegen unterhalb der Stimmbandebene über die Membrana cricothyroidea, um – nach erfolgloser Atemwegssicherung – in einer lebensbedrohlichen Notfallsituation die Oxygenierung und Ventilation zu sichern. Da die Membrana cricothyroidea früher als Ligamentum conicum bezeichnet wurde, wird das Verfahren auch (Notfall-)Koniotomie genannt. Eine Atemwegsultraschalluntersuchung zur Identifizierung dieser Membran kann die Erfolgsquote verdoppeln. Gemäß Leitlinie können auch in der Atemwegsultraschalltechnik unerfahrene Anästhesistinnen und Anästhesisten die Cricothyroidmembran nach einem kurzen, aber strukturierten Training auch bei schwierigen anatomischen Verhältnissen mittels Ultraschall identifizieren. Dies ist bei Notwendigkeit eines translaryngealen Zugangs hilfreich [1].
Weiter kann Ultraschall ein erhöhtes Aspirationsrisiko feststellen und bietet eine Bestätigung der korrekten Lage des Endotrachealtubus. Da es sich zumeist um Studien mit geringer Fallzahl und niedrigem Evidenzgrad handelt, sind alle Empfehlungen im Abschnitt „Sonographie der Atemwege“ mit der Formulierung „kann erwogen werden“ versehen [1].
Wenngleich sich gemäß Leitlinie die korrekte Tubuslage mit Ultraschall feststellen lässt, ist dies nicht als Ersatz für die Kapnografie anzusehen. Die Autoren der Leitlinie weisen darauf hin, dass es besonders in Hinblick auf nicht spezialisierte Anwender weiterer Untersuchungen bedarf, um die diagnostische Genauigkeit des Ultraschalls zu ermitteln.
Empfehlung 9: „Besteht kein schwieriger Atemweg mit Indikation für eine endotracheale Intubation unter Erhalt der Spontanatmung, soll eine geplante neuromuskuläre Blockade sofort nach Erreichen einer suffizienten Narkosetiefe durchgeführt werden, ohne dass vorher die Möglichkeit der Maskenbeatmung überprüft wurde.“
Die neuromuskuläre Blockade (NMB), also der Einsatz eines Muskelrelaxans, erfolgt oft erst, nachdem getestet wurde, ob eine Maskenbeatmung möglich ist. Dem steht die Erkenntnis gegenüber, dass eine NMB die Maskenbeatmung nie erschwert, sondern in den meisten Fällen erleichtert, höhere Tidalvolumina erzielt und seltener zu Entsättigungen führt [1].
In einem Leitartikel aus 2008 warfen Calder und Yentis die damals recht provokante Frage auf, ob die angenommene „sichere Praxis“, vor der Verabreichung einer NMB eine wirksame Maskenbeatmung nachweisen zu müssen, nicht vielmehr die sichere Praxis gefährdet [11]. Die seither gesammelte Evidenz deutet stark darauf hin, dass dies tatsächlich der Fall ist. Das Überprüfungsgremium des 4. National Audit Project (NAP4) war der Ansicht, dass die verzögerte oder fehlende Verabreichung von NMB bei Atemwegsproblemen zu unerwünschten Ereignissen beitrug [12].
Im NAP4-Bericht heißt es dazu: „Wenn die Gesichtsmasken- oder Larynxmaskenanästhesie durch eine fehlgeschlagene Beatmung und zunehmende Hypoxie erschwert wird, sollte der Anästhesist die frühzeitige Verabreichung eines weiteren Anästhetikums und/oder eines Muskelrelaxans in Betracht ziehen, um einen Laryngospasmus auszuschließen und zu behandeln.“ Und: „Kein Anästhesist sollte zulassen, dass sich eine Atemwegsobstruktion und Hypoxie zu einem Stadium entwickeln, in dem ein chirurgischer Notfallatemweg erforderlich ist, ohne vorher ein Muskelrelaxans verabreicht zu haben.“
Empfehlung 12: „Nach der derzeitigen Evidenzlage kann eine SGA vom LM-Typ nach individueller Nutzen-Risiko-Abwägung alternativ zum Endotrachealtubus bei den erweiterten Indikationen angewendet werden. In diesen Fällen sollte eine SGA vom LM-Typ der zweiten Generation verwendet und über das gastrale Lumen eine Magensonde vorgeschoben werden. Nach Platzierung soll eine Testung von Lage und Dichtigkeit erfolgen.“
Unter erweiterten Indikationen versteht die Leitlinie Eingriffe, die eine höhere Anforderung an die Dichtigkeit zur Beatmung stellen und somit einen verbesserten Schutz vor Luftinsufflation in den Magen bieten, was wiederum die Gefahr einer Regurgitation vermindert. Die Autoren der Leitlinie zählen dazu unter anderem laparoskopische Operationen, Eingriffe an adipösen Patienten und Operationen, die nicht in Rückenlage erfolgen. Voraussetzung ist die Verwendung von Larynxmasken (LM) der sogenannten zweiten Generation. Diese verfügen über einen Kanal („gastrales Lumen“, „Drainagekanal“), der das Einlegen einer Magensonde ermöglicht. Mit diesen SGA ist auch eine sichere Lagekontrolle möglich.
Der Leitlinie zufolge sollen die Tests zur Lagekontrolle erfolgreich bestanden werden, die Anwendung unter acht Stunden bleiben und der Anwender über ausreichend Erfahrung verfügen. Zu den in der Leitlinie aufgeführten Lagetests zählt der Magen-Leckage-Test („Bubble“-Test).
Hierzu wird der Drainagekanal mit einem Tropfen Gel verschlossen. Wurde die Spitze der LM nicht korrekt platziert, entstehen Bläschen (englisch „Bubbles“) am Drainagekanaleinlass, da die Luft retrograd aus dem Kanal entweichen kann. Der positive Jugulum-Test (Supra-Sternal-Notch-Test) kann zusätzlich Hinweise auf die korrekte Lage geben. Der zuvor beschriebene Tropfen Gel am Eingang des Drainagekanals kommt auch hier zum Tragen. Wird mit einem Finger ein leichter Druck auf das Jugulum ausgeübt und bewegt sich das Gel synchron zu dem applizierten Druck, wird dies als Zeichen der korrekten Lage gewertet. Erklären lässt sich dieses Phänomen dadurch, dass der Druck die Spitze der LM komprimiert und die Luftsäulenbewegung eine Bewegung des Gels bewirkt. Eine weitere Lagekontrolle ist die widerstandsfreie Einlage einer Magensonde. Lässt sich eine Magensonde ausreichend tief durch den Drainagekanal einführen, ist es ausgeschlossen, dass die Spitze einer SGA umgeschlagen ist [1, 13].
Empfehlung 16: „Bei erwartet schwieriger direkter Laryngoskopie und bei Notfallpatienten sollte einem Videolaryngoskop gegenüber der direkten Laryngoskopie primär der Vorzug gegeben werden.“
Empfehlung 17: „Ein Videolaryngoskop mit Macintosh Spatel kann in der Anästhesie primär zum Einsatz kommen.“
Empfehlung 18: „Bei der Verwendung von Videolaryngoskopen [mit hyperanguliertem Spatel (Ergänzung des Autors)] soll ein Führungsstab verwendet werden und ausreichend Erfahrung auch außerhalb von Notfallsituationen vorhanden sein. Der Tubus mit Führungsstab sollte so gebogen sein, dass dieser der Form des Spatels zur Spitze folgt.“
Viele Geräte fallen heutzutage unter den Sammelbegriff Videolaryngoskop (VL). Hierbei ist ein Kameramodul in den Laryngoskopspatel integriert. Das Bild dieses Kameramoduls wird in Echtzeit auf einem Videomonitor dargestellt. Teilweise unterscheiden sich diese Module in ihrer Form, Technik und Handhabung grundsätzlich voneinander. Der Leitlinie zufolge ist die Spatelform der VL ein wichtiges Unterscheidungskriterium (Abb. 1).
- Eine Spatelform ähnelt vom Aufbau her dem Macintosh-Spatel. Dieses VL ermöglicht eine „konventionelle“ Intubation, das heißt mit direkter Sicht auf die Stimmritze. Parallel ist das Geschehen auf dem Monitor beobachtbar und somit auch für Ausbildungszwecke günstig.
- Die andere Spatelform ist deutlich stärker gebogen (hyperanguliert), zum Beispiel der D-Blade beim C-MAC. Eine direkte Sicht auf die Stimmritze ist mit diesem Spateltyp nicht mehr möglich. Von Vorteil ist, dass die Reklination des Kopfes und das Anheben des Zungengrunds nicht erforderlich sind.
Die Anwendung eines VL von weniger erfahrenen Anwendern kann zu einem erhöhten, primären Intubationserfolg führen (Abb. 2).
Bei elektiven Patienten im OP zeigte sich, dass die direkte Laryngoskopie gegenüber der VL keine Vorteile bietet und beim ersten Intubationsversuch mit einer signifikant niedrigeren Erfolgsrate einhergeht [1]. Wird ein VL mit hyperanguliertem Spatel verwendet, besteht die Herausforderung darin – trotz optimaler Visualisierung –, den Tubus in die Glottis einzuführen. Hierzu ist der Tubus mit einem Führungsstab optimal an den Spatel anzupassen.
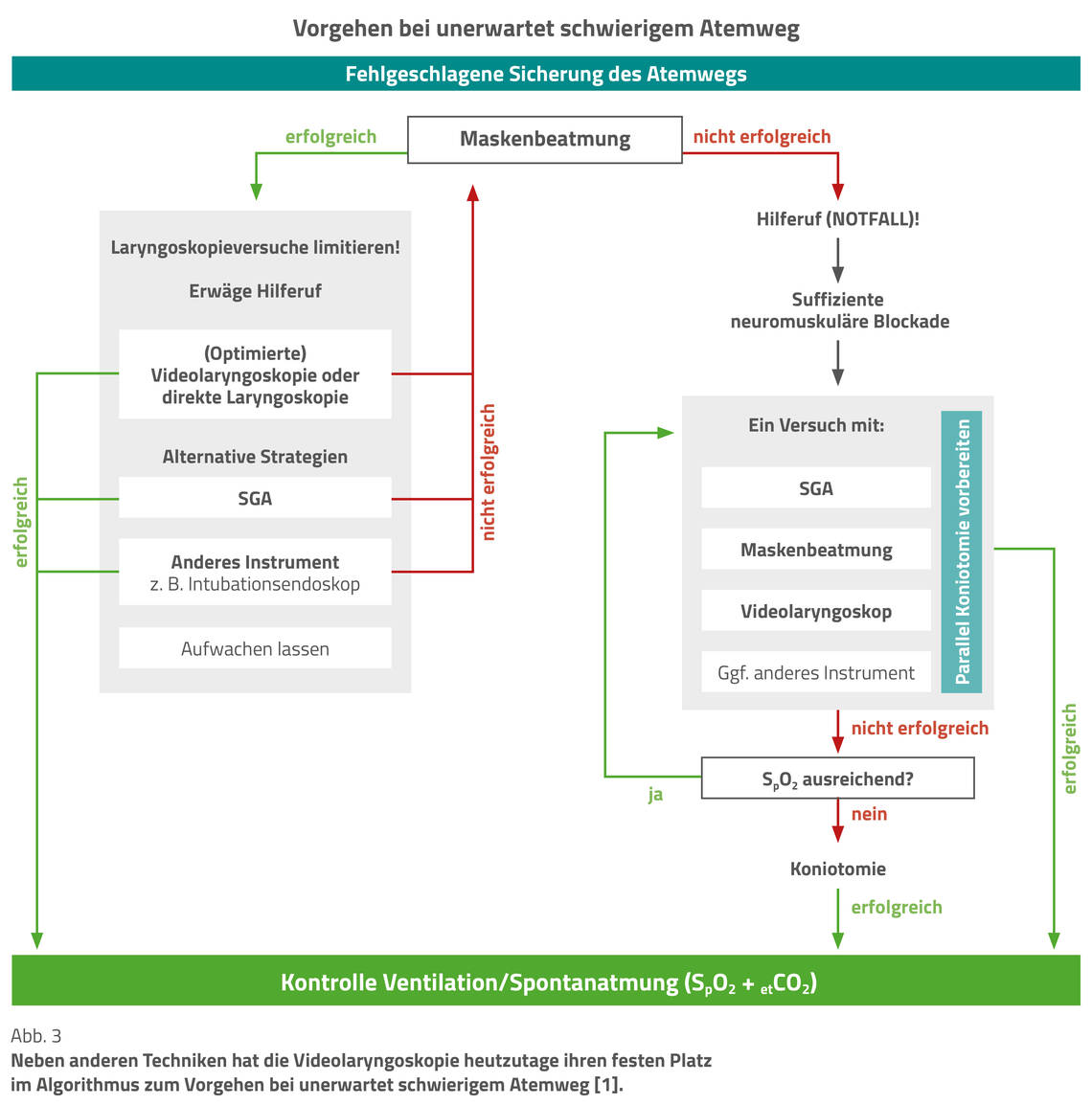
Die Leitlinie hebt hervor, dass das VL heutzutage als die wichtigste Technik zur Beherrschung des unerwartet schwierigen Atemwegs gilt (Abb. 3).
Empfehlung 37: „Ein Videolaryngoskop soll an jedem anästhesiologischen Arbeitsplatz verfügbar sein.“
Empfehlung 93: „Nach erfolgter Atemwegssicherung soll die korrekte Lage des Endotrachealtubus bzw. der SGA mittels Kapnografie verifiziert werden.“
Empfehlung 94: „Zum Ausschluss einer zu tiefen Tubuslage soll die Auskultation des Thorax erfolgen. Im lauten Umfeld oder nicht möglicher Auskultation kann das Pleuragleiten per Sonographie nachgewiesen werden.“
Die Leitlinie betont, dass die Kapnografie bei allen Maßnahmen zur Sicherung der Atemwege einen sehr hohen Stellenwert hat. Sie kann jedoch nicht verhindern, dass ein Endotrachealtubus zu tief eingeführt und nur eine Lungenhälfte ventiliert wird. Aus diesem Grund muss zusätzlich eine Auskultation erfolgen. Die Empfehlung 94 erwähnt die Sonografie der Atemwege, die die Leitlinie in Abschnitt 2 näher beschreibt.
Leitlinie enthält weitere Themen
Da dieser Beitrag lediglich einige ausgewählte Empfehlungen vorstellt, sei allen, die beruflich mit der Atemwegssicherung zu tun haben, ein Blick in die Leitlinie sehr empfohlen. So fehlen in diesem Beitrag beispielsweise die Aspekte der Atemwegssicherung auf der Intensivstation und zwei weitere in der Leitlinie veröffentlichte Algorithmen. Es sei außerdem darauf hingewiesen, dass Expertinnen und Experten stets betonen, dass die nichttechnischen Fertigkeiten bei der Atemwegssicherung eine große Rolle spielen.
[1] Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin. S1-Leitlinie Atemwegsmanagement 2023. (AWMF Registernummer 001 – 028), Zugriff: 4.9.2023
[2] Timmermann A, Byhahn C, Dörges V et al. S1-Leitlinie: Prähospitales Atemwegsmanagement. Anästhesiologie & Intensivmedizin 2019; 60: 316–336
[3] Deutsche Gesellschaft für Unfallchirurgie: S3-Leitlinie Polytrauma/Schwerverletzten-Behandlung (AWMF Registernummer 187–023), Version 4.0 (31.12.2022), verfügbar unter www.awmf.org/leitlinien/detail/ll/187-023.html; Zugriff: 4.9.23
[4] Hoffmann F, Keil J, Urban B. Interdisziplinär konsentierte Stellungnahme: Atemwegsmanagement mit supraglottischen Atemwegshilfen in der Kindernotfallmedizin – Larynxmaske ist State-of-the-art. Anästh Intensivmed 2016; 57: 377–386
[5] Nationale Versorgungsleitlinien. Im Internet: www.leitlinien.de/hintergrund/leitliniengrundlagen; Zugriff: 4.9.2023
[6] Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF). Ständige Kommission Leitlinien. AWMF-Regelwerk „Leitlinien“. 2. Aufl. 2020. Im Internet: www.awmf.org/leitlinien/awmf-regelwerk.html; Zugriff: 4.9.2023
[7] Torossian A. Algorithmen zum Atemwegsmanagement. AINS – Anästhesiologie · Intensivmedizin · Notfallmedizin · Schmerztherapie 2023; 58 (02): 72–81. doi:10.1055/a-1754-5426
[8] Rosenstock C, Hansen E, Kristensen M et al. Qualitative analysis of unanticipated difficult airway management. Acta Anaesthesiol Scand 2006; 50: 290–297
[9] Erweiterte lebensrettende Maßnahmen. ERC-Leitlinien 2015. Anwendermanual 7. Aufl. Hrsg. European Resuscitation Council. ISBN 9789079157839
[10] Cierpka T. Vorhersage der schwierigen Intubation mittels des „Upper-Lip-Bite-Testes“ im Vergleich zur Mallampati-Klassifkation. Philipps-Universität Marburg, 2009. doi.org/10.17192/z2009.0298
[11] Calder I, Yentis SM. Could ‘safe practice’ be compromising safe practice? Should anaesthetists have to demonstrate that face mask ventilation is possible before giving a neuromuscular blocker? Anaesthesia. 2008; 63: 113–115
[12] Royal College of Anaesthetists. 4th National Audit Project (NAP4). Major Complications of Airway Management in the United Kingdom. www.rcoa.ac.uk/nap4; Zugriff: 4.9.23
[13] Dembinski R, Scholtyschik D. Die Larynxmaske – Schritt für Schritt. Pneumologie 2019; 73 (11): 686–691. doi:10.1055/a-0947-3446
[14] Austin DR, Chang MG, Bittner EA. Use of Handheld Point-of-Care Ultrasound in Emergency Airway Management. Chest. 2021 Mar; 159 (3): 1155–1165. doi: 10.1016/j.chest.2020.09.083