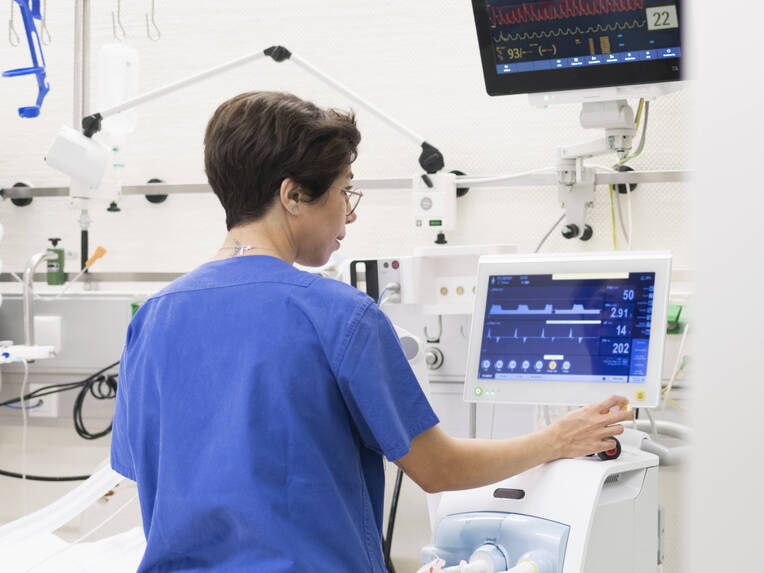
Pflegefachpersonen übernehmen bei der kontinuierlichen Nierenersatztherapie zentrale Aufgaben, um eine sichere und individuell angepasste Behandlung zu gewährleisten. Sie sind verantwortlich für die sorgfältige Vorbereitung und kontinuierliche Überwachung der Patienten sowie das schnelle und fachkundige Reagieren bei Komplikationen und Gerätestörungen.
Die kontinuierliche Nierenersatztherapie (CKRT: „continuous kidney replacement therapy“) ist eine unentbehrliche Komponente der modernen Intensivmedizin und bei der Therapie kritisch kranker Patientinnen und Patienten mit einer akuten Nierenschädigung (AKI) von enormer Bedeutung.
Verfahren, wie die kontinuierliche veno-venöse Hämofiltration (CVVH), die kontinuierliche veno-venöse Hämodialyse (CVVHD) und die kontinuierliche veno-venöse Hämodiafiltration (CVVHDF) zählen zu den kontinuierlichen Behandlungsoptionen bei akuten Nierenschädigungen und ermöglichen eine schonende und individuell anpassbare Elimination von Flüssigkeit und harnpflichtigen Substanzen, was insbesondere bei hämodynamisch instabilen und kritisch kranken Patienten von Vorteil ist. Die einzelnen Verfahren unterscheiden sich in ihren jeweiligen physikalischen Wirkprinzipien, dem Konvektions- und Ultrafiltrationsprinzip, der Diffusion und der Kombination aus allen [1–4].
Für das pflegerische Team ergeben sich daraus besondere Anforderungen: Neben der Überwachung und Sicherstellung eines reibungslosen Ablaufs der Therapie ist ein zielgerichtetes und rasches Eingreifen bei Störungen oder Komplikationen essenziell. Pflegefachpersonen müssen zudem über spezifische Kenntnisse zu den verschiedenen Dialyseverfahren, deren Funktionsprinzipien und den Besonderheiten der Antikoagulation verfügen, um die Therapie optimal an die individuellen Bedürfnisse der Patienten anpassen zu können. Die CKRT beeinflusst zahlreiche physiologische Parameter – darunter den Flüssigkeits-, Elektrolyt- und Säure-Basen-Haushalt sowie Laborwerte – und erfordert daher ein hohes Maß an Fachkompetenz und interdisziplinärer Zusammenarbeit.
Vorbereitung und Therapiestart
Haben die ärztlichen Kolleginnen und Kollegen die Indikation und die Verordnung für eine CKRT bei einem Intensivpatienten gestellt, sind die Vorbereitung und der Therapiestart in vielen Kliniken Aufgaben der intensivpflegerischen Versorgung.
Eine Studie aus dem Jahr 2022 ermittelte mittels eines standardisierten Fragebogens, dass der Aufbau des Nierenersatzverfahrens zu 32,8 Prozent und der Betrieb zu 55,3 Prozent dem Pflegepersonal der Intensivstation obliegen [5]. Zu den pflegerischen Vorbereitungen gehören
- die Überprüfung oder gegebenenfalls die Assistenz bei der Neuanlage eines geeigneten zentralvenösen Dialysezugangs – meist groß- lumige Shaldon-Katheter,
- die Gerätevorbereitung – inklusive Aufbau der Dialysemaschine und Überprüfung der Funktionalität,
- die Auswahl des kontinuierlichen Verfahrens, in interdisziplinärer Absprache – CVVH, CVVHD oder CVVHDF,
- die Bereitstellung der verordneten Antikoagulation – Citratantikoagulation oder Antikoagulation mit Heparin/Argatroban,
- die Einstellung der Parameter gemäß der ärztlichen Anordnung und
- das Anschließen des Patienten an das Dialyse- gerät.
Der Anschluss an das CKRT-Gerät erfolgt unter sterilen Bedingungen, wobei das Pflegefachpersonal die ersten Minuten besonders intensiv beobachtet, um Komplikationen wie Hypotonie oder direkt auftretende Fehlermeldungen am Gerät zu erkennen und entsprechend reagieren zu können.
Überwachung während der Therapie
Mit Abschluss der Vorbereitung und des Anschließens beginnt die eigentliche CKRT. Dabei steht die engmaschige Überwachung der Vitalparameter wie Blutdruck, Herzfrequenz, Temperatur, Sauerstoffsättigung und Bewusstseinslage sowie der Geräteparameter wie Druckverhältnisse, Flussraten und Alarmmeldungen im Mittelpunkt. Veränderungen der Vitalwerte können beispielsweise Hinweise auf Komplikationen wie Volumenverschiebungen, Kreislaufinstabilität oder Elektrolytstörungen geben.
Gerinnungskontrollen. Abhängig vom jeweils gewählten Antikoagulationsverfahren sind die Kontrollen der Gerinnung von enormer Bedeutung. Im Falle einer regionalen Citratantikoagulation unternimmt das intensivpflegerische Team regelmäßig systemische und Postfilter-Calcium-Kontrollen mittels Blutgasanalysen (BGA), um eine optimale Antikoagulation durch Steuerung des Citrats im extrakorporalen Blutkreislauf zu gewährleisten und somit Gerinnungsprozesse im Dialysesystem zu verhindern, indem die Calcium-Konzentration herabgesenkt wird (0,25–0,35 mmol/l im extrakorporalen Blutkreislauf) [1].
Eine systemische Antikoagulation mittels Heparin oder Argatroban erfordert hingegen eine regelmäßige Überprüfung des Laborwerts der aktivierten partiellen Thromboplastinzeit (aPTT) oder der aktivierten Gerinnungszeit (ACT), um die Antikoagulationstherapie während des kontinuierlichen Nierenersatzverfahrens zu steuern. Argatroban kommt dabei als Medikament zur Antikoagulation bei Patienten mit einer heparininduzierten Thrombozytopenie Typ II (HIT II) zum Einsatz.
Bilanzierung. Die Bilanzierung im Zuge der CKRT ist ebenfalls ein zentrales Element des Managements und der Überwachung der kritisch kranken Patienten auf Intensivstationen. Ziel ist es, den Flüssigkeits- und Elektrolythaushalt präzise zu steuern. In der Bilanzierung erfolgt die exakte Erfassung und Gegenüberstellung aller Flüssigkeitszufuhren (zum Beispiel Infusionen, Ernährung, Medikamente) und -verluste (zum Beispiel Urin, Drainagen, CKRT-Ultrafiltrat). Das Bilanzziel, also die gewünschte Nettoflüssigkeitsbilanz, ist individuell für jeden Patienten festzulegen – je nach klinischem Zustand kann dies eine neutrale, positive oder negative Bilanz sein. Die CKRT ermöglicht es, gezielt Flüssigkeit zu entziehen (Ultrafiltration), um das Bilanzziel zu erreichen – die Ultrafiltrationsrate lässt sich individuell anpassen. Dabei können Bilanzierungsprotokolle unterstützend helfen, sofern die Errechnung der Bilanz nicht elektronisch erfolgt.
Laborwerte. Besonders relevante, zu beobachtende Laborwerte unter einer laufenden CKRT sind die sogenannten Retentionsparameter, zu denen vor allem Kreatinin und Harnstoff zählen. Diese Werte geben Auskunft über die Effektivität des Nierenersatzverfahrens. Die dem Pflegeteam obliegenden regelmäßigen BGA zeigen Störungen im Elektrolythaushalt, im Glukosemetabolismus oder im Säure-Basen-Haushalt auf [3]. Die Kontrolle des Säure-Basen-Status, ins- besondere des pH-Werts, des Bicarbonats und der Basenabweichung, ist notwendig, um eine metabolische Azidose oder Alkalose frühzeitig zu erkennen und gegebenenfalls mittels Therapieanpassungen zu behandeln.
Metabolische Störungen infolge einer CKRT sind vielfältig und lassen sich mithilfe von Einstellungen des Blut-Dialysat-Verhältnisses anpassen [2]. Ebenso wichtig ist die Überwachung der Elektrolyte – insbesondere Kalium, Natrium, Calcium, Magnesium und Phosphat –, da Verschiebungen dieser Werte unter einer CKRT auftreten und lebensbedrohlich sein können [7].
Troubleshooting definieren
Bereits im Vorfeld der Therapie sollten Handlungsketten und Problemlösungen festgelegt sein, um auf Komplikationen und Alarmmeldungen während der laufenden Dialysebehandlung adäquat reagieren zu können. Empfehlenswert ist, standardisierte, fachübergreifende Arbeitsanweisungen (Standard Operation Procedures = SOP) zu entwickeln, um transparent die Anforderungen an Qualifikation, Schulung und Verantwortlichkeiten darzulegen [3].
Alarme und Fehlermeldungen. Häufige Gerätealarme während der laufenden CKRT beziehen sich auf Abweichungen des Zugangsdrucks (arterieller Druckalarm) oder des Rückflussdrucks (venöser Druckalarm). Der Zugangsdruck ist aufgrund der Sogwirkung der Blutpumpe immer ein negativer Druck.
Ein zu hoher Ansaugdruck (arterieller Druck ist sehr weit im negativen Bereich) führt jedoch zu einem Alarm am Dialysegerät, da das Gerät den eingestellten Blutfluss nicht bewältigen kann. Ursächlich können beispielsweise verschlossene Klemmen, ein Abknicken von Leitungen oder ein Shaldon-Katheter sein, der an der Gefäßwand anliegt. Bei langen Therapiezeiträumen mit eingestellter Ultrafiltration kann ebenfalls ein intravasaler Volumenmangel zu Ansaugproblemen führen.
Eine vorsichtige Volumengabe in Absprache mit den ärztlichen Kollegen oder die Reduktion des Entzugs kann Abhilfe schaffen. Das Vertauschen oder Umpolen des arteriellen und des venösen Anschlusses sollte nur zur kurzzeitigen Überbrückung dienen, da es dadurch zu einer Rezirkulation innerhalb des Dialysekatheters kommt und dies die Behandlungseffektivität einschränkt [4]. Bei einem plötzlich auftretenden positiven Ansaugdruck ist häufig eine Diskonnektion oder eine Erhöhung des intrathorakalen Drucks, beispielsweise durch Husten, ursächlich für diese Alarmmeldung.
Der Rückflussdruck (venöser Druck) der Dialysemaschine ist stets mit einer positiven Zahl beziffert. Fällt dieser Druck plötzlich ab (Richtung null), ist das System auf Leckagen und auf eine Diskonnektion zu kontrollieren. Abgeknickte Leitungen oder verschlossene Klemmen führen hingegen zum Erreichen des oberen Drucklimits [6].
Neben den Alarmen des Zugangsdrucks (arterieller Druckalarm) und des Rückflussdrucks (venöser Druckalarm) ist eine Überwachung des Filterdrucks (TMP = Transmembrandruck) obligat, um ein mögliches Clotting der Dialyse frühzeitig zu erkennen. Ausschlaggebend hierfür ist die Zeit, in der sich der TMP erhöht, da insbesondere ein sprunghafter Anstieg Hinweise auf ein Gerinnsel gibt [6]. Sollte es dazu kommen, so ist von einer Retransfusion des im CKRT-Gerät befindlichen Blutes abzusehen [7].
Sollten während der laufenden Therapie sogenannte Luft- oder Blut-Leck-Alarme auftreten, ist zumeist das System des kontinuierlichen Nierenersatzgeräts zu wechseln, da es sich dabei meist um nicht behebbare Leckagen im Schlauchsystem, zum Beispiel an Entnahmestellen für Blutproben durch zu große Kanülen, oder um Defekte innerhalb des Kapillarsystems des Filters handelt [6].
Treten technische Probleme mit dem Dialysegerät auf, beispielsweise Pumpenstillstand oder Softwarefehler, sind – nach Ausschluss eines Bedienerfehlers – ein Wechsel des Dialysegeräts und die Kontaktaufnahme mit der herstellenden Firma notwendig, um die Sicherheit der Patienten nicht zu gefährden.
Citratakkumulation. Bei einem CKRT-Verfahren mit einer regionalen Citratantikoagulation ist die Citratakkumulation eine gewichtige Komplikation, die auf eine Störung im Lebermetabolismus bei einem akuten Leberversagen zurückzuführen ist, da die Leber das Citrat in so einem Fall nicht mehr genügend verstoffwechselt [2]. Hinweise dafür sind ein steigendes Verhältnis des Gesamt-Calciums zu ionisiertem Calcium und eine metabolische Azidose, die auf dem inkompletten Abbau der Calcium-Citrat-Komplexe beruht, sodass weniger Bikarbonat in der Leber entsteht [1]. Sind diese Veränderungen bei einem Patienten mit einer Leberinsuffizienz und einer CKRT mit regionaler Citratantikoagulation auffällig, so sollte interdisziplinär ein Wechsel auf eine CKRT mit systemischer Antikoagulation besprochen werden [1]. Dafür eignen sich vor allem Heparin und Argatroban.
Weitere pflegerische Herausforderungen
Temperaturmanagement. Bei Intensivpatienten, die eine CKRT erhalten, stellt das Temperaturmanagement eine besondere pflegerische Herausforderung dar. Aufgrund der extrakorporalen Zirkulation des Blutes und der – meist unzureichend temperierten Substitutions- und Dialysatlösungen – kommt es häufig zu einem ungewollten Abfall der Körperkerntemperatur. Diese ungewollte Hypothermie kann den Kreislauf und den Stoffwechsel der Patienten negativ beeinflussen. Daher ist eine engmaschige und kontinuierliche Überwachung der Körpertemperatur essenziell.
Pflegepersonal muss kontinuierlich die Temperatur messen (zum Beispiel über einen transurethralen Blasenkatheter mit Temperatursonde), Veränderungen dokumentieren und bei Abweichungen frühzeitig intervenieren. Ziel ist es, sofern keine therapeutische Hypothermie indiziert ist, eine Normothermie (36–37 °C) aufrechtzuerhalten. Moderne CKRT-Geräte verfügen deshalb meist über integrierte Heizsysteme, die Substitutions- und Dialysatflüssigkeiten erwärmen, um die Körperkerntemperatur der Patienten auf physiologischem Level zu halten.
Blutwärmer werden am venösen Schenkel eingesetzt, um das Blut vor der Rückführung in den Körper des Patienten wieder auf ein physiologisches Niveau zu erwärmen. Konvektive Temperaturmanagementsysteme, zum Beispiel spezielle Wärmedecken oder -matten, ermöglichen eine gezielte Erwärmung der zu therapierenden Person über die Haut. Zu beachten ist, dass eine CKRT-induzierte Kühlung der zu behandelnden Person möglicherweise zu einer Fieberverschleierung oder einer Fiebermaskierung führt, sodass ein auftretendes Fieber unter Umständen gar nicht bzw. zu spät erkannt wird [7].
Pflege von Dialysekathetern. Ein hygienischer Umgang mit den Dialysezugängen ist essenziell, um die Gefahr einer Sepsis bei den zumeist immungeschwächten Patienten auf einer Intensivstation zu verringern. Die hygienische Händedesinfektion nach den aktuellen Richtlinien des Robert Koch-Instituts stellt hierbei die Basis dar und ist vor und nach jedem Umgang mit einem Dialysezugang obligat. Dem pflegerischen Team obliegt die tägliche Kontrolle der (Dialyse-)Zugänge auf auftretende Entzündungszeichen und Blutungen sowie eine Kontrolle des Verbands auf Verschmutzungen und den korrekten Sitz. Jegliche Veränderung an den Zugängen ist zu dokumentieren und im interdisziplinären Team zu besprechen. Sollte eine Neuanlage eines Dialysezugangs indiziert sein, so ist in jedem Fall ein neues Dialyseset zu verwenden.
Mobilisation. Eine CKRT soll eine Frühmobilisation der betroffenen Patienten nicht einschränken oder vermeiden [3]. Im klinischen Alltag ist jedoch zu beobachten, dass Pflegende Hemmungen haben, Patienten mit einer laufenden CKRT zu mobilisieren – aus Angst vor versehentlicher Dislokation des Shaldon-Katheters [3] oder vor nicht zu behebenden Fehlermeldungen am Dialysegerät insbesondere bei femoral liegenden großlumigen Kathetern.
Tatsächlich stellt eine CKRT keine Kontraindikation für die Mobilisation der Intensivpatienten dar und ist unter Beachtung einiger Sicherheitskriterien gut handhabbar. Zu solchen Sicherheitsvorkehrungen gehören die richtige Fixation der Dialysekatheter, Schulungen und eine interprofessionelle enge Zusammenarbeit von Pflegefachpersonen, Physiotherapeutinnen und -therapeuten, Ärztinnen und Ärzten. Zudem können Mobilisationsprotokolle hilfreich sein, um Unsicherheiten im pflegerischen Team zu minimieren und den Mobilisationsprozess mit einer passenden Mobilisationsart zu begleiten [8]. Auch die S3-Leitlinie Lagerungstherapie und Mobilisation von kritisch Erkrankten auf Intensivstationen aus dem Jahr 2024 empfiehlt eindeutig eine Mobilisation von Menschen mit einer laufenden CKRT auf Intensivstationen und gibt zu dieser Thematik detaillierte Informationen und Empfehlungen [9].
Dokumentation ist unerlässlich
Pflegenden auf der Intensivstation obliegt meist die kontinuierliche Dokumentation des Dialyseverfahrens. Sie dient der Überwachung der Gerinnungseinstellung, dem Erkennen von Komplikationen, zum Beispiel drohendes Clotting, der Bilanzüberwachung und schlussendlich der Sicherheit der Patienten. Auch mögliche Therapieunterbrechungen – etwa wegen Transporten oder Operationen – sind zu dokumentieren [7]. Zusätzlich stellt eine kontinuierliche Dokumentation die Abrechenbarkeit der Leistung sicher und ist somit auch im wirtschaftlichen Sinne von großer Bedeutung. Mithilfe eines Protokolls lassen sich potenzielle Schwierigkeiten während des CKRT-Weaning-Prozesses strukturiert erfassen. Die Auswahl des geeigneten Protokolls sowie der darin genannten Einflussfaktoren ist jedoch bislang nur unzureichend wissenschaftlich belegt [3].
[1] Heise D. Kontinuierliche Nierenersatzverfahren in der Intensivmedizin. Anästh Intensivmed 2024; 65: 603–611. doi: 10.19224/ai2024.603
[2] Bethke N, Khadzhynov D. Kontinuierliche Nierenersatztherapie. Nephrologie aktuell 2024; 28: 214–221. doi: 10.1055/a-2268-3875
[3] Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin (DIVI), Deutsche Gesellschaft für Internistische Intensivmedizin und Notfallmedizin (DGIIN), Deutsche Gesellschaft für Anästhesie und Intensivmedizin (DGAI). S3 Leitlinie Nierenersatztherapie in der Intensivmedizin. Version: V1.0 vom 12.03.2025. Im Internet: register.awmf.org/assets/guidelines/040-017l_S3_Nierenersatztherapie- Intensivmedizin_2025-06.pdf
[4] Kindgen-Milles D. Akutes Nierenversagen – Die Behandlung des akuten Nierenversagens mit kontinuierlichen Nierenersatzverfahren. Fresenius Medical Care Deutschland GmbH 2012
[5] William C, Meersch M et al. Aktueller Stand der Durchführung von Nierenersatztherapien auf deutschen Intensivstationen. Med Klin Intensivmed 2022; 117: 367–373. Im Internet: doi.org/10.1007/ s00063-021-00835-y
[6] Breuch G, Hrsg. Fachpflege Nephrologie und Dialyse, 5. Aufl. Elsevier Urban & Fischer, München, 2014
[7] Steinel M, Schuster S. Pflegerische Versorgung von Dialysepatienten. intensiv 2025; 33: 145–152. doi: 10.1055/a-2537-8793
[8] Stöckelmayer W. Mobilisation von Patienten mit Nierenersatztherapie. intensiv 2025; 33: 153–158. doi: 10.1055/a-2546-4965
[9] Deutsche Gesellschaft für Anästhesie und Intensivmedizin (DGAI). S3-Leitlinie Lagerungstherapie und Mobilisation von kritisch Erkrankten auf Intensivstationen. Version: 3.1 vom 25.07.2023. Im Internet: register.awmf.org/assets/guidelines/001-015l_S3_ Lagerungstherapie-Mobilisation-von-kritisch-Erkrankten-auf- Intensivstationen_2024-09.pdf