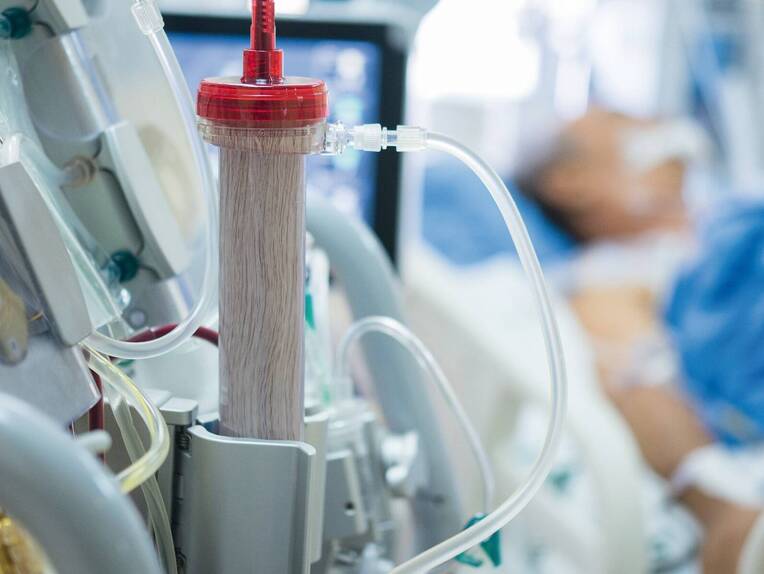
Die Nierenersatztherapie in der Intensivmedizin ist eine komplexe, invasive Maßnahme – zugleich ein Feld, in dem professionelle Pflege den Unterschied macht. Entscheidend sind stringente Prozesse, sicheres Monitoring, Mobilisationskultur im Team und fundiertes Wissen über zentralvenöse Zugänge. Ziel ist die Harmonisierung von Mensch und Technik, um Komplikationen zu vermeiden und Outcomes zu verbessern.
Im deutschsprachigen Raum finden sich verschiedene Bezeichnungen für eine akute Einschränkung der Nierenfunktion, etwa akutes Nierenversagen, akute Nierenschädigung oder akute Nierenfunktionseinschränkung. International hat sich mit Einführung der KDIGO-Klassifikation (Kidney Disease: Improving Global Outcomes, eine internationale Fachorganisation, die Leitlinien für die Diagnose, Klassifikation und Therapie von Nierenerkrankungen erarbeitet) [1] der Begriff Acute Kidney Injury (AKI) durchgesetzt und wird inzwischen auch in der deutschsprachigen Fachliteratur genutzt.
Anzumerken ist bei der Begrifflichkeit, dass die deutsche Nephrologie gern den Begriff akute Nierenfunktionsverschlechterung anstelle akute Nierenschädigung verwenden möchte. Aktuell liegt eine aktuelle, für den deutschsprachigen Raum maßgebliche, überarbeitete Leitlinie vor. Diese wurde in PflegenIntensiv vorgestellt (Version 1.0, März 2025) [2]. In der aktualisierten Version vom 23. Mai 2025 wurden nach der Konsultationsphase der Fachgesellschaften Langfassung und Evidenzbericht angepasst [3, 4].
Anatomie und Funktionen der Niere
Das Gewebe der Nieren stammt aus dem intermediären Mesoderm. Das Mesoderm ist das mittlere Keimblatt der Embryonalentwicklung, aus dem unter anderem Muskeln, Knochen, Herz-Kreislauf- und Urogenitalsystem entstehen. Die entwickelten Nieren des Erwachsenen haben eine Länge von etwa zehn bis zwölf Zentimetern und eine Breite von fünf bis sechs Zentimetern. Das Gewicht variiert ungefähr zwischen 120 und 200 Gramm.
Die Nieren, ein paariges, bohnenförmiges Organ, liegen unterhalb des Zwerchfells zwischen dem zwölften Brust- und dem dritten Lendenwirbel im Retroperitonealraum. Wegen des großen rechten Leberlappens befindet sich die rechte Niere in der Regel etwas tiefer. Jede Niere liegt im sogenannten Nierenlager, das von Musculus quadratus lumborum und Musculus psoas major begrenzt wird.
Äußerlich sind die Nieren von einer festen, wenig dehnbaren Bindegewebskapsel umgeben, die von einem kräftigen Fettpolster (Capsula adiposa renis) und der umschließenden Fascia renalis eingebettet wird.
Die funktionelle Grundeinheit ist das Nephron, das sich aus dem Glomerulum für die Filtration und dem Tubulussystem für Reabsorption und Sekretion zusammensetzt.
Über die Kombination aus glomerulärer Filtration, tubulärer Feinregulation und Sammelrohrmechanismen übernehmen die Nieren zentrale Aufgaben der Homöostase: die Steuerung von Wasser- und Elektrolythaushalt, die Aufrechterhaltung des Säure-Basen-Gleichgewichts, die Regulation des Blutdrucks über das Renin-Angiotensin-Aldosteron-System, die Produktion von Erythropoetin sowie die Aktivierung von Vitamin D zur Knochengesundheit. Darüber hinaus tragen sie zur Entgiftung, zum Metabolismus zahlreicher Substanzen und zur Anpassung an unterschiedliche Belastungssituationen bei [5].
AKI fordert Intensivteams
Eine intensivpflichtige AKI ist meist multifaktoriell. Sepsis ist der häufigste Treiber, gefolgt von Hypovolämie, kardiogenem Schock und Nephrotoxinen. Klassische primäre Nierenerkrankungen sind seltener.
Wichtig ist, dass die Indikationsstellung zur Nierenersatztherapie (NET) nicht alleinig von Laborwerten, sondern von der klinischen Situation abhängig ist. Der Start einer NET bei akuten, lebensbedrohlichen Komplikationen gilt als unstrittig (Tab.). Offen bleibt jedoch, ob ein vorgezogener Beginn mit dem Ziel, solche Komplikationen zu verhindern und eine stabilere metabolische Situation zu sichern, tatsächlich zu einer Senkung der Sterblichkeit führt [6].
Klassische primäre Nierenerkrankungen, die in seltenen Fällen eine kontinuierliche Nierenersatztherapie (CRRT) erfordern, ohne dass zwangsläufig eine Chronifizierung entsteht, sind zum Beispiel:
- Akute Glomerulonephritiden – zum Beispiel Immunglobulin-A-(IgA-)Nephropathie, postinfektiöse Glomerulonephritis (GN), Anti-GBM-Krankheit (Anti-Glomeruläre-Basalmembran-Glomerulonephritis, Goodpasture-Syndrom)
- Rapid-progressive Glomerulonephritis (RPGN) – zum Beispiel im Rahmen einer Vaskulitis (ANCA-assoziiert, antineutrophile zytoplasmatische Antikörper)
- Akute interstitielle Nephritis – zum Beispiel durch Medikamente, Antibiotika, nichtsteroidale Antirheumatika (NSAR)
- Akute Tubulusnekrose nach Intoxikationen – zum Beispiel Ethylenglykol, schwere Myoglobinurie, Hämolyse
- Thrombotische Mikroangiopathien (TMA) – zum Beispiel hämolytisch-urämisches Syndrom (HUS), thrombotisch-thrombozytopenische Purpura (TTP), atypisches HUS
- Akute Kristallnephropathien – zum Beispiel durch Tumorlyse, hoch dosiertes Methotrexat
In der Notfall- und Intensivpflege ist bei der Anamnese die Vormedikation unbedingt zu beachten. Substanzen wie Metformin, NSAR, Protonenpumpeninhibitoren (PPI), Beta-Lactam-Antibiotika, Rifampicin, Sulfonamide und Fluorchinolone können akute Nierenschäden verursachen.
Besonders NSAR und PPI gelten als häufige Auslöser einer akuten interstitiellen Nephritis (AIN), deren Pathomechanismus immunologisch vermittelt ist [7]:
- Pathophysiologie bei NSRA und PPI:
- Beide Substanzgruppen wirken als Haptene: Sie binden an Strukturen im Nierengewebe (vor allem Tubuluszellen) und machen diese für das Immunsystem „fremd“.
- Es kommt zu einer T-Zell-vermittelten Immunreaktion gegen das interstitielle Nierengewebe.
- Folge ist eine entzündliche Infiltration mit Lymphozyten, Plasmazellen und oft Eosinophilen. Dies führt zu einer Schwellung und Schädigung des Interstitiums und der Tubuli.
- Klinisch:
- Verzögerter Beginn: meist Tage bis Wochen nach Beginn der Medikation
- Symptome: unspezifisch, zeigen sich häufig in Fieber, Exanthem, Eosinophilie (die klassische „Trias“ ist aber selten komplett)
- Labor: AKI mit Anstieg von Kreatinin, oft sterile Pyurie, Eosinophilurie
- Besonderheiten:
- NSAR: häufig bei älteren Patienten; AIN kann auch nach längerer Einnahme auftreten
- PPI: heute einer der häufigsten Ursachen; oft schleichender Verlauf, manchmal erst nach Monaten erkennbar
Eine Metformin-Intoxikation hingegen führt typischerweise zu einer schweren metabolischen Azidose mit Laktaterhöhung (MALA, Metformin-associated lactic acidosis). Klinisch oft mit schwerer Hypotonie, Vigilanzminderung und Nierenversagen verknüpft, was die Metformin-Clearance zusätzlich verschlechtert. Pathophysiologisch liegt eine primär metabolische Störung vor, die durch die Beeinträchtigung der mitochondrialen Atmungskette verursacht wird und zu einer vermehrten konsekutiven Laktatproduktion führt [8].
Das klassische Blutgasbild (BGA) ist charakterisiert durch:
- pH: deutlich erniedrigt (<7,20, teils <7,0)
- pCO₂: erniedrigt als Ausdruck der respiratorischen Kompensation (Hyperventilation)
- HCO₃-: stark vermindert (<5 mmol/l, teils <10 mmol/l)
- Basenexzess (BE): deutlich negativ (−10 bis −20 mmol/l oder tiefer)
- Anionenlücke: erhöht (>20 mmol/l), bedingt durch die Laktatakkumulation
- Laktat: deutlich erhöht (meist >5 mmol/l, nicht selten zweistellig), dies gilt als pathognomonisch für MALA
- pO₂: in der Regel normal, da keine primäre Oxygenierungsstörung vorliegt
Wichtig zu wissen:
- Metformin-Intoxikation führt typischerweise zu einer Laktatazidose mit hoher Anionenlücke, sehr niedrigem Bicarbonat und sehr hohem Laktatspiegel.
- NRSA und PPI Akute können eine interstitielle Nephritis auslösen, die in ein akutes Nierenversagen mit Urämie münden kann. Dabei tritt eventuell eine milde Azidose auf, aber nicht das typische Bild der MALA.
Die NET bleibt hier oftmals die einzige Option, um lebensbedrohliche Entgleisungen zu stabilisieren, ohne den Anspruch, die Niere vollständig zu „ersetzen“. Während glomeruläre Prozesse sich technisch teilweise ersatzweise abbilden lassen (Diffusion, Konvektion), bleiben komplexe tubuläre Transportleistungen, endokrine und metabolische Funktionen weitgehend unersetzt – eine wichtige Grenze jeder NET.
NET: Zugang, Steuerung, Sicherheit
Bevorzugt wird die rechte Vena jugularis interna (innere Drosselvene); die Vena subclavia (Schlüsselbeinvene) sollte wegen Shunt-gefährdender Stenoserisiken möglichst gemieden werden. Femorale Zugänge sind valide Alternativen. Die sollte auch bei der Anlage im Schockraum Beachtung finden [9]. Das parallele Einführen eines CRRT-Katheters und eines weiteren zentralen Venenkatheters (ZVK) in dasselbe Gefäß ist zu vermeiden: Medikamente werden „verdünnt“ oder vorzeitig eliminiert, Noradrenalinbedarfe können steigen oder gar Ernährungslösungen die Filterfunktionen beeinträchtigen (Bilder). Günstig ist eine getrennte Lage – etwa jugulär (CRRT) und femoral (ZVK).
Die Etablierung und Durchführung kontinuierlicher wie auch intermittierender Nierenersatzverfahren auf Intensivstationen erfordern ein hohes Maß an technischer Ausstattung, geeignete räumliche Bedingungen sowie klar definierte organisatorische Abläufe. Ebenso entscheidend ist die fachliche Qualifikation aller beteiligten Berufsgruppen.
Neben einem Basismonitoring braucht eine NET eine erweiterte, situationsadaptierte pflegerische Beobachtung und Blutgasanalysen: Kalium, Calcium gesamt und ionisiert bei Citrat-Antikoagulation, Magnesium, Glukose, Hämoglobin/Hämatokrit.
Substitutionen (Kalium, Calcium, Insulin) erfolgen gemäß ärztlich definierten Zielbereichen. Tätigkeiten im Rahmen ärztlicher Anordnungen können auch Pflegefachpersonen mit dreijähriger Ausbildung übernehmen.
Pflegefachpersonen dokumentieren Blutfluss, Ultrafiltration, Dialysatfluss, gegebenenfalls Citrat- und Calciumdosis und passen diese im vorgegebenen Rahmen an. Das große extrakorporale Blutvolumen begünstigt eine Hypothermie, um die Körperkerntemperatur engmaschig zu überwachen. Neben externen Wärmequellen wird die Gerätheizung patientenadaptiert reguliert, um eine Hypothermie zu vermeiden.
Für ein eigenverantwortliches Durchführen solcher Verfahren – im Rahmen der ärztlichen Anordnung und Zielvorgaben – sind neben klinischer Erfahrung und einer regelmäßigen Anwendung unter ärztlicher Anleitung spezialisierte Weiterbildungen erforderlich, etwa in der Fachpflege für Anästhesie- und Intensivpflege oder in der Fachpflege Nephrologie [1].
Eine (Früh-)Mobilisation stellt einen zentralen Bestandteil der intensivmedizinischen Behandlung und Pflege dar [10]. Zwar können großlumige Katheter und die Anbindung an die CRRT die Beweglichkeit theoretisch einschränken, ebenso wie die Sorge vor einer Dislokation der Dialysezugänge eine Barriere für die regelmäßige Umsetzung der Mobilisation darstellen kann.
Dennoch wird der erforderliche Aufwand sowie die praktische Durchführbarkeit je nach Berufsgruppe unterschiedlich eingeschätzt [11]. Interprofessionelle Schulungen und praxisorientierte Trainings auf Grundlage eines standardisierten, von der DGIIN herausgegebenen Curriculums sind daher empfehlenswert [12].
Die Leitliniengruppe (Kidney Disease) empfiehlt, dass Kliniken und Einrichtungen klinikspezifische als auch fachübergreifende standardisierte Arbeitsanweisungen (SOPs) für die Durchführung von Nierenersatzverfahren erstellen, implementieren und konsequent einhalten [1].
Katheter-Check vor CRRT-Start
Bei regionaler Citrat-Antikoagulation ist eine kontinuierliche Calcium-Substitution erforderlich. Erfolgt diese separat (Spritzenpumpe), ist ein dreilumiger CRRT-Katheter sinnvoll. Wenn die Calciuminfusion direkt vor den venösen Zugang der NET gegeben wird, genügt ein zweilumiger Katheter; so bleibt ein Lumen für Medikamente/Parenteralia frei. Eine kontinuierliche periphere Calciumgabe ist kontraindiziert, da Paravasation zu schweren Weichteilnekrosen führt.
Vor Beginn einer CRRT gelten folgende pflegerische Maßnahmen:
- tägliche Inspektion der Einstichstelle, der Katheterlage und möglicher Infektzeichen,
- Überprüfung der Durchgängigkeit beider Lumen per Aspiration (Locklösung/Koagel entfernen),
- Spül- und Funktionstest, zum Beispiel:
- 20 ml 0,9 % NaCl injizieren,
- anschließend 20 ml Blut aspirieren.
- Faustregel: Werden 20 ml in circa 6 s aspiriert, entspricht das einem Fluss von circa 200 ml/min.
Ziel sind ≥200 bis 250 ml/min pro Schenkel. Verzögerter oder asymmetrischer Fluss limitiert die Effektivität der CRRT.
Bei fehlender Aspiration eines Lumens kann das Crossover-Anschließen als Notlösung dienen (distal entnehmen, proximal reinfundieren) – verbunden mit Wirkverlust. Unbedingt dokumentieren und im Team kommunizieren.
Gemeinsam sicher handeln
- Qualitätssicherung: Pflegefachpersonen sichern die Qualität der NET durch kontinuierliches Monitoring, strukturierte Abläufe und die konsequente Umsetzung von SOPs.
- Arzneimittelanamnese: Eine sorgfältige Medikamentenanamnese ist unverzichtbar. NSAR, PPI und Metformin sind häufige Auslöser akuter Nierenschäden und beeinflussen den Verlauf und die Therapieentscheidungen.
- Indikationsstellung: Die Indikationsstellung bleibt klinisch – Laborwerte allein genügen nicht. Die Entscheidung zur NET orientiert sich stets an der klinischen Gesamtsituation des kritisch Kranken.
- Zentralvenöse Zugänge: Die Zugänge richtig wählen und prüfen – Katheterlage, Durchgängigkeit und Flussraten bestimmen maßgeblich die Effektivität und Sicherheit der CRRT.
Professionell Pflegende sehen den ganzen Menschen – auch an der NET. Mit Haltung, klugen Abläufen und interprofessioneller Zusammenarbeit wird aus hochkomplexer Technik eine sichere, personenzentrierte Therapie, die Komplikationen vermeidet und die Genesung fördert.
Literatur:
[1] Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2022 Clinical Practice Guideline for Diabetes Management in Chronic Kidney Disease. Kidney International 2002; 102 (4S): 1–127. Im Internet: kdigo.org/wp-content/uploads/2022/10/KDIGO-2022-Clinical-Practice-Guideline-for-Diabetes- Management-in-CKD.pdf
[2] Bünte M. Kritische Balance wahren: Therapie des akuten Nierenversagens. PflegenIntensiv 2025; 3 (25): 4–11
[3] Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin (DIVI), Deutsche Gesellschaft für Internistische Intensivmedizin und Notfallmedizin (DGIIN), Deutsche Gesellschaft für Anästhesie und Intensivmedizin (DGAI) et al. S3-Leitlinie Nierenersatztherapie in der Intensivmedizin (Version 1.1, 04.04.2025). Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF), Register-Nr. 040–017. Im Internet: register.awmf.org/assets/guidelines/ 040-017l_S3_Nierenersatztherapie-Intensivmedizin_2025-06.pdf
[4] Willam C, Joannidis M, Jörres A et al. 10 Kernaussagen zur S3-Leitlinie zur evidenzbasierten Nierenersatztherapie in der Intensivmedizin [Ten key messages from the S3 guideline for evidence-based renal replacement therapy in intensive care medicine]. Medizinische Klinik, Intensivmedizin und Notfallmedizin 2025; 120 (6): 494–496. Im Internet: doi.org/10.1007/s00063-025-01297-2
[5] Schwegmann H, Huckenbeck Y. Alles unter Kontrolle: Kontinuierliche Nierenersatztherapie auf Intensivstation. PflegenIntensiv 2025; 3 (25): 12–16
[6] Sleziona M. Den optimalen Beginn finden: Einsatz von Nierenersatzverfahren. PflegenIntensiv 2025; 3 (25): 18–23
[7] Kellum JA, Lameire N. Diagnosis, evaluation, and management of acute kidney injury: A KDIGO summary (Chapter 293). In: Jameson JL, Fauci AS, Kasper DL et al. Harrison‘s Principles of Internal Medicine (20th ed.). McGraw-Hill Education 2017. Im Internet: www.ncbi.nlm.nih.gov/books/NBK441896
[8] Taylor BN, Taylor R. Metformin associated lactic acidosis in the setting of acute kidney injury. Journal of Emergency and Critical Care Medicine 2018; 2: 54. Im Internet: jeccm.amegroups.org/article/view/4889
[9] Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin (DGAI), Deutsche Gesellschaft für Interdisziplinäre Notfall- und Akutmedizin (DGINA), Deutsche Gesellschaft für Innere Intensiv- und Notfallmedizin (DGIIN) et al. S1-Leitlinie Gefäßzugänge bei der Erstversorgung von erwachsenen Notfallpatienten im Schockraum (Version 1.0, 11.3.2025). AWMF-Register-Nr. 001–051. Im Internet: register.awmf.org/de/leitlinien/detail/001-051
[10] Hermes C, Nydahl P, Grunow JJ, Schaller SJ. Positioning therapy for intensive care patients. Dtsch Med Wochenschr 2024; 149: 1028–1033
[11] Hermes C, Nydahl P, Blobner M et al. Assessment of mobilization capacity in 10 different ICU scenarios by different professions. PLoS One 2020; 15: e0239853
[12] Eggers D, Hermes C, Esteve H et al. Interprofessional curriculum for early mobilization: Developed by the nursing section of the DGIIN in close cooperation with the German early mobilization network. Med Klin Intensivmed Notfmed 2023; 118: 487–491