Dieser zweite Teil eines Übersichtsbeitrags zu den wichtigsten Inhalten der interdisziplinären und interprofessionellen S3-Leitlinie „Intensivmedizin nach Polytrauma“ befasst sich mit den Inhalten der Kapitel 5 bis 13. Der Autor stellt weitere ausgewählte Behandlungsempfehlungen vor.
Beschäftigte sich der erste Teil des Übersichtsbeitrags zur S3-Leitlinie „Intensivmedizin nach Polytrauma“ vorrangig mit organisatorischen und technischen Aspekten im Zusammenspiel der verschiedenen Professionen, so widmet sich dieser zweite Teil insbesondere den Prozessen und therapeutischen Maßnahmen in der Behandlung polytraumatisierter Patientinnen und Patienten.
Kap. 5: Beatmung
Die Leitlinie verweist bezüglich der nichtinvasiven Beatmung (NIV) im Wesentlichen auf die S2k-Leitlinie der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) „Nichtinvasive Beatmung als Therapie der akuten respiratorischen Insuffizienz“ [1], hebt jedoch hervor, dass der Einsatz der NIV beim Polytrauma nicht als Routine- oder First-Line-Verfahren anzusehen ist [2].
Den Leitlinienautorinnen und -autoren zufolge basiert die Initiierung der invasiven Beatmung nach Polytrauma auf den Empfehlungen der S3-Leitlinie „Invasive Beatmung und Einsatz extrakorporaler Verfahren bei akuter respiratorischer Insuffizienz“ [3]. In Ermangelung gezielter Empfehlungen zur Wahl des Beatmungsverfahrens bei Polytraumapatientinnen und -patienten sind die Leitlinienautoren der Ansicht, dass diese allgemeinen Empfehlungen auch bei der Wahl des Beatmungsverfahrens für dieses Patientenkollektiv hinzuzuziehen sind, wenn eine akute respiratorische Insuffizienz vorliegt.
Empfehlung 5.1 (Empfehlungsgrad: GPP)
Bei der Wahl des Beatmungsverfahrens bei Poly- traumapatienten sollten allgemeine Empfehlungen bei dem Vorliegen einer akuten respiratorischen Insuffizienz berücksichtigt werden [3].
Die vorgenannte Leitlinie geht auch explizit auf die akute respiratorische Insuffizienz beim akuten Atemnotsyndrom (ARDS) sowie die Wahl des Beatmungsverfahrens und der Einstellung der Beatmungsparameter ein [3]. Daher befürworten die Leitlinienautoren, diese Empfehlungen im ARDS nach Polytrauma anzuwenden [2].
Empfehlung 5.2 (Empfehlungsgrad: GPP)
Bei Polytraumapatienten sollten grundlegende Beatmungsprinzipien der ARDS-Therapie in der akuten respiratorischen Insuffizienz berücksichtigt werden [3].
Der Leitlinie zufolge gibt es mehrere Indikationen für eine Tracheotomie bei Polytraumapatienten auf Intensivstationen [2]. Dazu zählen
- die prolongierte mechanische Beatmung,
- das prolongierte Weaning sowie
- die Atemwegssicherung bei Traumata im Kopf- und/oder Gesichtsbereich.
Jedoch ist der optimale Zeitpunkt der Tracheotomie seit Jahrzehnten umstritten. Die Fragestellung, ob eine frühe Tracheotomie im Vergleich zur späten Tracheotomie zu besseren Behandlungsergebnissen für Polytraumapatienten führt, lässt sich anhand der Auswertung der verfügbaren Evidenz derzeit nicht beantworten [2].
Empfehlung 5.3 (Empfehlungsgrad: 0)
Bei Polytraumapatienten kann weder eine Empfehlung für noch gegen eine frühe Tracheotomie gegeben werden.
Weitere für den Abschnitt „Beatmung“ relevante Leitlinien sind die S1-Leitlinien „Atemwegsmanagement“ [4] und „Tracheo-Bronchoskopie“ [5].
Kap. 6: Volumen- und Kreislauftherapie
Aus Sicht der Leitlinienautoren ist der Nutzen einer schnellen, effektiven und zielorientierten Volumentherapie bei Polytraumapatienten unumstritten. Bei den meisten Patienten kann eine adäquat erfolgte Volumentherapie das notwendige Plasmavolumen und infolgedessen eine adäquate kardiale Vorlast erhalten oder wiederherstellen. Dies stellt die Organperfusion und die Mikrozirkulation sicher oder verbessert beides zumindest.
Der Leitlinie zufolge besteht das wichtigste Ziel der Volumentherapie in der Steigerung des Herzzeitvolumens und der Sicherstellung eines ausreichenden Sauerstoffangebots (DO2). Die Leitlinienautoren verweisen auf die S3-Leitlinie „Polytrauma/Schwerverletzten-Behandlung“, die bei schwer verletzten Patienten die Einleitung einer Volumentherapie empfiehlt, die bei unkontrollierbaren Blutungen allerdings in reduzierter Form erfolgen sollte, um den Kreislauf auf einem niedrig stabilen Niveau zu halten und die Blutung nicht zu verstärken [6].
Bei Schädel-Hirn-Trauma-Patienten mit Hypotension sollte die Volumentherapie mit dem Ziel der Normotension erfolgen [6]. Somit umfasst eine optimale Volumentherapie die Indikationsstellung, die Dosisfindung und die Wahl der am besten geeigneten Infusionslösung für den jeweiligen Patienten [2].
Besteht der Verdacht auf einen Volumenmangel, sind Patienten der Leitlinie zufolge zur Klärung der Ursachen für einen Volumenverlust unter Berücksichtigung der Anamnese körperlich zu untersuchen. Besteht eine unklare hämodynamische Instabilität, soll eine Echokardiografie erfolgen.
Diesbezüglich verweisen die Leitlinienautoren auf die S3-Leitlinien „Intravasale Volumentherapie bei Erwachsenen“ [7, 8] und „Polytrauma/Schwerverletzten-Behandlung“ [6], denen zufolge die transthorakale Echokardiografie bei Polytraumapatienten auch zu nutzen ist, um eine Perikardtamponade oder eine Herzbeutelruptur zu diagnostizieren.
Für die polytraumatisierten Patienten mit Begleitverletzungen des Herzens wird auf die S3-Leitlinie „Intensivmedizinische Versorgung herzchirurgischer Patienten – Hämodynamisches Monitoring und Herz- Kreislauf“ verwiesen [9, 10].
Eine Verlaufsbeurteilung zum Beispiel thorakoabdomineller Verletzungen kann mittels bildgebender Verfahren wichtige therapeutische Hinweise liefern, wenn eine kardiale Ursache für einen Volumenmangel auszuschließen ist [2].
Die Leitlinienautoren haben sich mit der Fragestellung befasst, ob eine kristalloide Volumentherapie bei Polytraumapatienten im Vergleich zur kolloidalen Volumentherapie zu besseren Behandlungsergebnissen führt. Kristalloide Lösungen, auch kristalline Lösungen genannt, kennzeichnen unterschiedlichste elektrolythaltige Lösungen, die keine Makromoleküle enthalten. Die Bezeichnung beruht darauf, dass die enthaltenen Ionen die Fähigkeit besitzen, Kristalle zu bilden. Kristalloide Lösungen sind zum Beispiel 0,9%-ige NaCl-, Ringer-, Ringer-Acetat-, Ringer-Laktat-Lösung, Jonosteril®, Sterofundin® und viele mehr. Der Leitlinie zufolge gibt die vorliegende Evidenz jedoch keine klare Empfehlung her [2, 7, 8].
Empfehlung 6.1 (Empfehlungsgrad: 0)
Bei Polytraumapatienten kann weder eine Empfehlung für noch gegen die Gabe von Kristalloiden gegeben werden.
Da obige Empfehlung keine klare Handlungsanweisung beinhaltet, haben die Leitlinienautoren ergänzend noch folgende konsensbasierte Empfehlung hinzugefügt:
Empfehlung 6.2 (Empfehlungsgrad: GPP)
Bei Polytraumapatienten sollten grundlegende Prinzipien der Volumentherapie berücksichtigt werden [7].
Bluttransfusion und Transfusionstrigger. Den Leitlinienautoren zufolge sind Blutungen die häufigste Ursache für einen Schock bei Polytraumapatienten, der zu Sauerstoffmangel in den Zellen und zum Tod führt. In den vergangenen Jahrzehnten beschäftigten sich viele experimentelle und klinische Forschungsarbeiten mit den zellulären Mechanismen und den klinischen Ergebnissen der Notfallversorgung von Patienten mit hypovolämischem Schock.
Dennoch sind die grundlegenden Prinzipien der Wiederherstellung des Kreislaufs laut Leitlinie weitgehend geblieben:
- Eine aggressive Rehydratation zur Korrektur der Gewebehypoperfusion innerhalb von 24 Stunden nach der Verletzung ist mit besseren klinischen Ergebnissen verbunden [2].
- Erster Volumenersatz der Wahl sind kristalloide Lösungen, wobei Blut und Blutprodukte bei hämodynamisch instabilen Patienten mit Blutungen der Klassen III und IV und bei Patienten mit anhaltenden unkontrollierten Blutungen eingesetzt werden [2].
Wichtig zu wissen: Die Schockklassen I–IV entstammen den Kursformaten Advanced Trauma Life Support (ATLS) und Prehospital Trauma Life Support (PHTLS). Dieser Einteilung zufolge entspricht die Schockklasse III einem Blutverlust von 31 bis 40 Prozent und Klasse IV mehr als 40 Prozent [11]. Daten haben mittlerweile gezeigt, dass diese Schockklassen nicht exakt mit dem tatsächlichen Blutverlust eines Patienten korrelieren und die Werte und Beschreibungen der Schockklassen Überlappungen aufweisen.
Der Leitlinie zufolge ist die Inzidenz immunologischer und infektiöser Komplikationen im Zusammenhang mit Bluttransfusionen bei der Kreislaufwiederherstellung von Polytraumapatienten nachweislich nicht höher als in anderen klinischen Situationen. Jedoch sind Massivtransfusionen mit spezifischen Komplikationen wie Hypothermie, Koagulopathie und abdominalem Kompartmentsyndrom verbunden.
Die Leitlinienautoren verweisen außerdem auf die traumainduzierte Koagulopathie als eigenständiges Krankheitsbild, das einen deutlichen Einfluss auf das Überleben hat, sodass Gerinnungsdiagnostik und Therapie spätestens im Schockraum beginnen sollen. Die Leitlinie verweist für Einzelheiten auf die „Querschnitts-Leitlinien zur Therapie mit Blutkomponenten und Plasmaderivaten“ [12].
Wichtig zu wissen: Die traumainduzierte Koagulopathie (TIK, TIC) ist eine akute Störung der Gerinnungsfähigkeit des Körpers, die nach schweren Verletzungen auftritt. Sie kann zu übermäßigen und anhaltenden Blutungen führen, die schwer zu stoppen sind. Die TIK kann eine Unfallverletzung verkomplizieren und ist mit einem höheren Sterberisiko verbunden.
Kap. 7: Definitive chirurgische Versorgung
Die Leitlinienautoren verweisen auf den Jahresbericht des TraumaRegisters® der Deutschen Gesellschaft für Unfallchirurgie, demzufolge Schwerverletzte durchschnittlich sechs Tage auf der Intensivstation verbleiben. Im Wesentlichen bestimmt die Verletzungsschwere die Dauer des Aufenthalts, wobei Patienten mit Kombinationsverletzungen die Intensivstation durchschnittlich nach knapp acht und mit lebensgefährlichen Verletzungen sogar nach über zehn Tagen verlassen. Der Leitlinie zufolge werden Patienten während ihres Krankenhausaufenthalts durchschnittlich 3,4-mal operiert.
Gibt es für die Behandlung in der Präklinik, im Schockraum und während der ersten operativen Phase bereits gut evaluierte Abläufe und Leitlinienempfehlungen, so stehen solche Quellen den Leitlinienautoren zufolge in Bezug auf die Versorgungspriorisierung, die Art und den Umfang der Folgeoperationen sowie den optimalen Zeitpunkt für operative Folgeeingriffe bei schwer verletzten Patienten im Rahmen der intensivmedizinischen Behandlung noch nicht zur Verfügung.
Laut den Leitlinienautoren sind für operative Folgeeingriffe die Heterogenität des Patientenguts, die Komplexität der Verletzungen sowie interdisziplinäre Absprachen zu beachten. Weiterhin spielen individuelle Patientencharakteristika (zum Beispiel Alter, Geschlecht, Vorerkrankungen) sowie pathophysiologische (zum Beispiel Gerinnung, Temperatur, Metabolismus) und immunologische (zum Beispiel Systemisches Entzündungsreaktionssyndrom, SIRS) eine Rolle.
Die Leitlinienautoren verweisen darauf, dass aus der klinischen Erfahrung heraus vor allem das Schädel-Hirn-Trauma und das Thoraxtrauma bestimmende Faktoren für die Operabilität der Patienten zu sein scheinen. Vor allem erhöhte, schwierig zu therapierende oder therapierefraktäre intrakranielle Druckwerte beeinflussen die Operabilität der Patienten, etwa infolge Einschränkungen der notwendigen Lagerung. Daher ist der Nutzen einer operativen Behandlung gegen mögliche intrakranielle Drucksteigerungen interdisziplinär abzuwägen. Auch für Patienten mit Wirbelsäulenverletzungen hängt der Operationszeitpunkt unter anderem von der Instabilität der Wirbelkörperfrakturen und den damit verbundenen Lagerungseinschränkungen für weitere Operationen oder für pflegerischen Maßnahmen auf der Intensivstation ab [2].
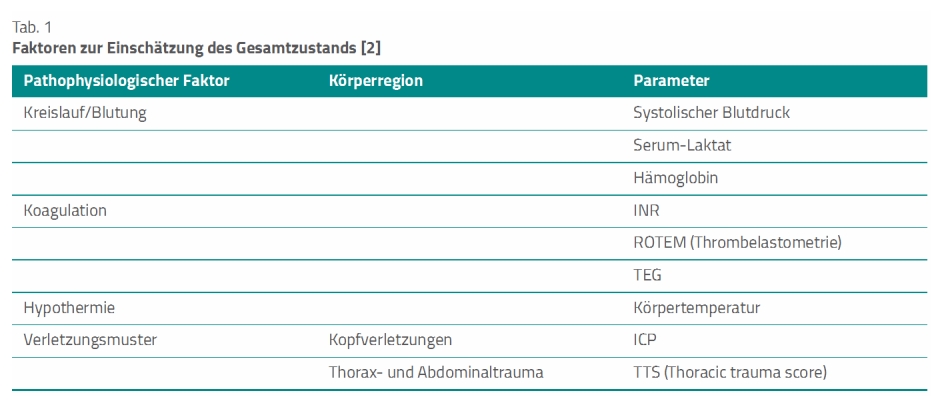
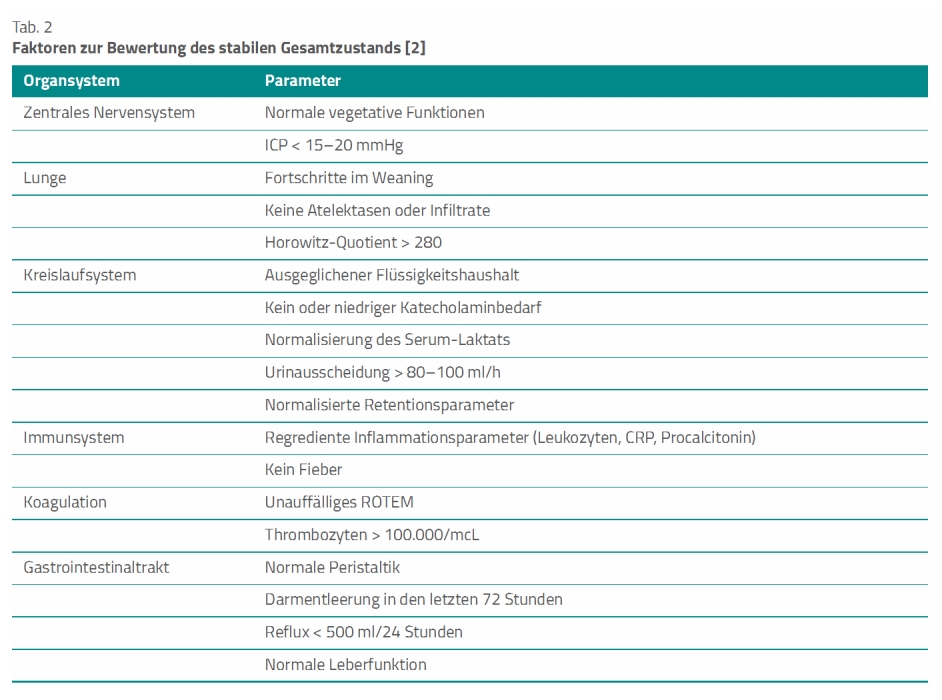
Insgesamt umfasst das Kapitel über 50 Seiten, sodass eine Einzelbetrachtung der Verletzungen beziehungsweise verletzten Organsysteme den Rahmen dieses Beitrags sprengen würde. Die Leitlinienautoren verweisen am Ende des Kapitels darauf, dass sich zur Bestimmung des Zeitpunkts für eine möglichst frühzeitige, definitive chirurgische Frakturversorgung, die den Patienten nicht gefährdet, verschiedene klinische, laborchemische und inflammatorische Parameter verwenden lassen. Die Leitlinie führt dazu aus, dass die Betrachtung einer Kombination mehrerer Parameter bezüglich des optimalen Operationszeitpunkts derzeit am vielversprechendsten erscheint (Tab. 1, 2) [2].
Empfehlung 7.21 (Empfehlungsgrad: GPP)
Ein tägliches Assessment einer Kombination aus klinischen, laborchemischen und inflammatorischen Parametern bei Polytraumapatienten sollte genutzt werden, um einen geeigneten, möglichst frühzeitigen Zeitpunkt zur definitiven operativen Versorgung zu bestimmen.
Kap. 8: Ernährungstherapie
Nach Angaben der Leitlinienautoren kann die medizinische Ernährungstherapie kritisch kranker Patienten aufgrund des vorbestehenden Ernährungsstatus sowie aufgrund des Zeitpunkts des Beginns, der Wahl des Applikationswegs, der Menge und Zusammensetzung der Makro- und Mikronährstoffzufuhr sowie des Monitorings der metabolischen und gastrointestinalen Toleranz individuell variieren [2].
Im Falle vorbestehender Adipositas zeigte sich ein negativer Einfluss auf die Ergebnisse nach einem stumpfen Thoraxtrauma. Adipositas führte zu einer längeren Beatmungsdauer und Verweildauer auf der Intensivstation und im Krankenhaus. Auf der anderen Seite ist auch die vorbestehende Malnutrition ein bedeutendes Problem. Sie ist der Leitlinie zufolge definiert als krankheitsbedingte Gewichtsabnahme, Untergewicht, Verlust an Muskelmasse und verminderter Energie- oder Proteinaufnahme. Malnutrition ist bei kritisch kranken Patienten mit einer höheren Morbidität und Mortalität assoziiert, ihre Prävalenz bei Traumapatienten wird in deutschen Krankenhäusern auf bis zu 40 Prozent geschätzt [2].
Für die Fragestellung, ob sich der Effekt der Ernährungstherapie auf klinische Endpunkte zwischen Polytraumapatienten und „allgemein“ kritisch kranken Patienten (ohne Polytrauma) unterscheidet, war trotz ausführlicher Literaturrecherche keine Evidenz zu finden. Das liegt unter anderem daran, dass keine vergleichenden prospektiven randomisierten kontrollierten Studien oder Metaanalysen zwischen Patienten mit versus ohne Polytrauma hinsichtlich ernährungstherapeutischer Fragestellungen existieren. Die Leitlinienautoren haben daher im Expertenkonsens folgende Empfehlung zur medizinischen Ernährungstherapie von Polytraumapatienten abgestimmt [2]:
Empfehlung 8.1 (Empfehlungsgrad: GPP)
Die Ernährungstherapie bei Polytraumapatienten sollte gemäß den Empfehlungen der aktuellen S2k-Leitlinie „Klinische Ernährung in der Intensivmedizin“ erfolgen [13].
Kap. 9: Lagerung und Physiotherapie
Gemäß den Autoren der Leitlinie unterscheiden sich die Grundprinzipien der Lagerung, der Mobilisation und der Physiotherapie polytraumatisierter Patienten auf der Intensivstation nicht von den Vorgaben für die gleiche Behandlung von aus anderer Ursache kritisch kranken Patienten. Sie werden einerseits prophylaktisch eingesetzt, um sekundäre Schäden oder Komplikationen zu vermeiden, dazu zählen insbesondere [2]:
- Druckulzerationen,
- Atemwegsinfekte,
- Kontrakturen,
- Muskelschwäche und Immobilität,
- Delir.
Andererseits sind mittels Lagerung, Mobilisation und Physiotherapie frühzeitig Verletzungsfolgen und verletzungsbedingte Bewegungseinschränkungen zu therapieren. Die Leitlinie betont die Wichtigkeit einer engen Absprache und Zusammenarbeit im ärztlichen und therapeutischen intensivmedizinischen Behandlungsteam. Absprachen sind sowohl innerhalb des intensivmedizinischen Teams als auch zwischen dem intensivmedizinischen Behandlungsteam und den jeweiligen Operateuren der verletzen Körperregionen zu treffen.
Die Absprachen betreffen unter anderem das tägliche Festlegen der Therapieziele (Tagesziele), die individuelle Nutzen-Risiko-Abwägung für bestimmte Maßnahmen/Empfehlungen, die Belastbarkeit einzelner Körperregionen, die vorliegende Kontraindikation gegen bestimmte Maßnahmen sowie die notwendige Analgesie und Sedierung.
Evidenzbasierte Empfehlungen zum Thema bietet die 2023 aktualisierte S3-Leitlinie „Lagerungstherapie und Mobilisation von kritisch Erkrankten auf Intensivstationen“ [14]. Dort wird empfohlen, die Mobilisation von Intensivpatienten innerhalb von 72 Stunden zu beginnen (starke Empfehlung LoE1).
Die S3-Leitlinie „Intensivmedizin nach Polytrauma“ geht im Einzelnen noch auf die Lagerung von Patienten mit Schädel-Hirn-Trauma, Thoraxtrauma, Wirbelsäulenverletzung, abdominellem Trauma, Beckenverletzung und Bauchlagerung ein [2].
Empfehlung 9.1 (Empfehlungsgrad: GPP)
Die Lagerung, Mobilisation und Physiotherapie von Polytraumapatienten sollte gemäß den Empfehlungen der aktuellen S3-Leitlinie „Lagerungstherapie und Mobilisation von kritisch Erkrankten auf Intensivstationen“ erfolgen [14].
Kap. 10: Multiorganversagen und Organersatztherapie
Die Leitlinienautoren führen aus, dass Polytraumapatienten ein stark erhöhtes Risiko für die Entwicklung eines Multiorganversagens aufweisen. Der Leitlinie zufolge ist das Multiorganversagen (MOV) ein akut lebensbedrohlicher Zustand, der durch die Fehlfunktion zweier oder mehrerer Organe hervorgerufen ist. Oft ist das MOV die Folge einer Sepsis oder einer anderen schweren traumatischen Gewebeschädigung.
Wichtig zu wissen: Die Sepsis ist ein lebensbedrohlicher Zustand, der entsteht, wenn die körpereigenen Abwehrreaktionen gegen eine Infektion die eigenen Gewebe und Organe im Sinne einer Fehlregulation schädigen.
Die Leitlinie behandelt Empfehlungen zu folgenden Organersatzverfahren im Rahmen der Therapie von Polytraumapatienten:
- Nierenersatztherapie (RRT, Renal Replacement Therapy)
- Extrakorporale Membranoxygenierung (ECMO)
Die RRT wird, so die Leitlinie, zur Behandlung der akuten Nierenschädigung (AKI, Acute Kidney Injury) eingesetzt. Die AKI ist eine der häufigen Manifestationen des Multiorganversagens. Zu den Arten der Nierenersatztherapie gehören die kontinuierliche Nierenersatztherapie (CRRT, Continuous Renal Replacement Therapy) und die intermittierende Hämodialyse (IHD). Den Leitlinienautoren zufolge wird die CRRT häufig bei instabilen Patienten bevorzugt, da sie kontinuierlich und schrittweise gelöste Stoffe entfernt und eine Steuerung des Flüssigkeitshaushalts ermöglicht.
Da es für den Einsatz von Nierenersatzverfahren im Rahmen der intensivmedizinischen Behandlung von Polytraumapatienten keine Evidenz aus prospektiv randomisierten Studien gibt, sind die Empfehlungen aus der klinischen Erfahrung abzuleiten.
Wann der ideale Zeitpunkt für den Beginn einer CRRT ist, wird in der Literatur teils widersprüchlich bewertet. Einen eindeutigen Vorteil eines frühen gegenüber eines späten Beginns einer CRRT in Bezug auf die Mortalität konnten die Leitlinienautoren nicht feststellen [2].
Extrakorporale Membranoxygenierung. Die ECMO (Extra Corporeal Membrane Oxygenation) wird bei Polytraumapatienten bei schwerem Atemversagen eingesetzt, die auf die herkömmliche mechanische Beatmung nicht ansprechen. Einzelheiten zu dem Verfahren finden sich beispielsweise in [15].
Wichtig zu wissen: Die ECMO ist ein maschinelles Organersatzverfahren, das die Funktion der Lunge (Oxygenierung und CO2-Elimination), des Herzens oder beider ersetzen kann [16].
Die Indikationen für eine ECMO-Therapie sind demnach zum Beispiel [17]:
- schweres akutes Lungenversagen (ARDS mit lebensbedrohlicher Hypoxämie),
- schweres akutes kardiales Pumpversagen (nach Myokardinfarkt, Lungenembolie),
- kardiopulmonale Reanimation.
Empfehlung 10.1 (Empfehlungsgrad: GPP)
Für den Einsatz der extrakorporalen Membranoxygenierung sollten die Empfehlungen der S3-Leitlinie „Extrakorporale Zirkulation (ECLS/ECMO), Einsatz bei Herz- und Kreislaufversagen“ sowie der S3-Leitlinie „Invasive Beatmung und Einsatz extrakorporaler Verfahren bei akuter respiratorischer Insuffizienz“ angewendet werden [3, 18].
Kap. 11: Wundmanagement
Dazu führt die Leitlinie aus, dass der chirurgische Wundverschluss bettseitig auf der Intensivstation erfolgen muss, sofern dies noch nicht im Schockraum oder im Rahmen der ersten operativen Versorgungsphase geschehen ist. Die Leitlinienautoren empfehlen in Abhängigkeit vom Verletzungsmuster und der Wundbeschaffenheit auch aus forensischen Gründen eine Fotodokumentation der Wunden.
Der Fortschritt der Wundheilung ist insbesondere bei chronischen Wunden und Dekubiti mittels regelmäßiger Wunddokumentation festzuhalten. Die periphere Durchblutung, Motorik und Sensibilität werden grundsätzlich vor jeder chirurgischen Wundversorgung überprüft und dokumentiert. Auch bettseitig ist auf streng aseptische Bedingungen zu achten.
Der Leitlinie zufolge ist zu prüfen, ob bei der vorliegenden Wunde ein primärer Wundverschluss möglich ist oder ob aufgrund der Entität und Beschaffenheit oder des Kontaminationsgrads der Wunde eine sekundär offene Wundbehandlung zu präferieren ist [2].
Wichtig zu wissen: Primäre Wundheilung heißt, dass die Wundränder direkt über die Ausbildung schmaler Narben zusammenwachsen. Eine Naht oder Klammern kann diese Wundheilung unterstützen. Für großflächige, klaffende Wunden mit großem Gewebeverlust ist hingegen die sekundäre Wundheilung oft der empfohlene Weg. Dabei wachsen die Wundränder nicht direkt zusammen. Stattdessen wird die Wunde vom Wundgrund aus mit Granulationsgewebe aufgefüllt [19].
Das Kapitel geht außerdem auf den Verbandwechsel und die Wundkontrolle, offene Wundbehandlung und Wundauflagen, Vakuumverbände (eine Sonderform des feuchten Wundverbands mit luftdichter Abdeckung), thermische Verletzungen, Wundversorgung bei Patienten mit anliegendem Fixateur externe oder Extensionsvorrichtungen und patientenindividuelle Einflussfaktoren ein [2].
Kap. 12: Antikoagulation und Thromboseprophylaxe
In diesem Kapitel widmen sich die Leitlinienautoren den Fragestellungen
- ob eine frühe Einleitung einer Antikoagulanzientherapie bei Polytraumapatienten im Vergleich zu einer späten Einleitung zu einer Verbesserung der klinischen Behandlungsergebnisse führt,
- ob der Verzicht einer (pharmakologischen) antithrombotischen Therapie bei Polytraumapatienten im Vergleich zur Standardbehandlung (pharmakologische antithrombotische Therapie) zu einer Verbesserung der klinischen Behandlungsergebnisse führt und
- ob die frühe Einleitung einer Thrombozytenaggregationshemmungstherapie bei Polytraumapatienten im Vergleich zu einer späten Einleitung zu einer Verbesserung der klinischen Behandlungsergebnisse führt.
Für alle Fragen erfolgte eine ausführliche Literaturrecherche. Die Leitlinienautoren kommen zu der Schlussfolgerung, dass zu keiner der genannten Fragestellungen eine Evidenz zu identifizieren war, die die Formulierung evidenzbasierter Empfehlungen ermöglichen würde. Lediglich zur Thromboseprophylaxe formulieren die Leitlinienautoren im Expertenkonsens folgende Empfehlung:
Empfehlung 12.1 (Empfehlungsgrad: GPP)
Die Thromboseprophylaxe soll sich an den Empfehlungen der aktuellen Fassung der S3-Leitlinie „Prophylaxe der venösen Thromboembolie (VTE)“ orientieren [20].
Kap. 13: Ethische Aspekte
Während des gesamten Behandlungspfads nach Polytrauma ergeben sich in Abhängigkeit der individuellen Gegebenheiten regelmäßig ethische Fragestellungen. Daher reichen die Inhalte des Kapitels 13 von der ethischen Betrachtung der frühen intensivmedizinischen Versorgung und hier insbesondere dahingehend, ob eine Situation existiert, in der keine Behandlung erfolgen soll oder die bestehende Behandlung gar abzubrechen ist, bis hin zur Prognoseabschätzung, die im Rahmen der Beratung der Betroffenen oder deren Angehörigen eine wichtige Position einnimmt, sowie zu den Implikationen für die Organspende [2].
Empfehlungen auf einem hohen Evidenzlevel können die Leitlinienautoren nicht aussprechen. Daher beinhaltet die Leitlinie Ausführungen gebietsbezogener Perspektiven von Experten sowie Auszüge aus der vorhandenen Literatur. Sie gibt damit Hilfestellungen für den Behandlungsprozess sowie Impulse für eine speziell auf das Polytrauma zugeschnittene Forschung [2].
Empfehlung 13.1 (Empfehlungsgrad: GPP)
Eine ausreichend sichere Aussage zur Langzeitprognose des Polytraumas im engeren Sinne ist aufgrund der vorhandenen Datenlage nicht möglich. Daher ist weitere Forschung notwendig, um den Langzeitverlauf nach stattgehabtem Polytrauma besser zu charakterisieren. Dabei sind neben der Sterblichkeit vor allem Faktoren wie die Lebensqualität der Betroffenen zu berücksichtigen und der Schwerpunkt der Erfassung auf die Perspektive der Betroffenen zu legen.
Viel Fachwissen erforderlich
Teil 1 und 2 über die Leitlinie „Intensivmedizin nach Polytrauma“ machen deutlich, dass die Versorgung dieser Patienten äußerst anspruchsvoll ist. Für das erforderliche umfassende Fachwissen bedarf es der Kenntnis zahlreicher anderer Leitlinien und nicht zuletzt ist eine umfassende Zusammenarbeit inklusive enger Absprachen zwischen den unterschiedlichen beteiligten Berufsgruppen essenziell.
Dieser Beitrag möchte dazu anregen, die unterschiedlichen Facetten der Patientenversorgung in den Blick zu nehmen. Das fängt an mit der Kommunikation und endet bei ethischen Aspekten.
[1] Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin. S2k-Leitlinie „Nichtinvasive Beatmung als Therapie der akuten respiratorischen Insuffizienz“. AWMF-Registernummer 020–004. Version 3.3 (redakt. überarb. Fassung v. 24.01.2024). Im Internet: register.awmf.org/de/leitlinien/detail/020-004; Zugriff: 30.08.2024
[2] Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin: S3-Leitlinie „Intensivmedizin nach Polytrauma“. AWMF-Registernummer 040–014. Version 1.0 (30.01.2024). Im Internet: register.awmf.org/de/leitlinien/detail/040-014; Zugriff: 30.08.2024
[3] DGAI. S3-Leitlinie „Invasive Beatmung und Einsatz extrakorporaler Verfahren bei akuter respiratorischer Insuffizienz“. AWMF-Registernummer 001–021. Im Internet: register.awmf.org/de/leitlinien/detail/001-021; Zugriff: 30.08.2024
[4] DGAI. S1-Leitlinie „Atemwegsmanagement“. Version 2.0 (Stand 21.08.2023). Im Internet: register.awmf.org/de/leitlinien/ detail/001-028; Zugriff: 30.08.2024
[5] Deutsche Gesellschaft für Hals-Nasen-Ohren-Heilkunde, Kopf- und Hals-Chirurgie. S1-Leitlinie „Tracheo-Bronchoskopie“. AWMF- Registernummer 017–061. Version 4.0 (Stand 06.07.2015, zurzeit in Überarbeitung). Im Internet: register.awmf.org/de/leitlinien/ detail/017-061; Zugriff: 30.08.2024
[6] Deutsche Gesellschaft für Unfallchirurgie. S3-Leitlinie „Polytrauma/Schwerverletzten-Behandlung“. AWMF-Registernummer 187–023. Version 4.0 (31.12.2022). Im Internet: www.awmf.org/leitlinien/detail/ll/187-023.html; Zugriff: 30.08.2024
[7] Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin (DGAI). S3-Leitlinie „Intravasale Volumentherapie bei Erwachsenen“. AWMF-Registernummer 001–020. Version 2.0 (21.07.2020). Im Internet: register.awmf.org/assets/guidelines/001-020l_ S3_Intravasale-Volumentherapie-Erwachsene_2020-10.pdf; Zugriff: 30.08.2024
[8] Dönitz S. Infusionslösungen für den Flüssigkeitshaushalt. Aktualisierte S3-Leitlinie zur intravasalen Volumentherapie. PflegenIntensiv 2022 (1): 55–61
[9] DGAI. S3-Leitlinie „Intensivmedizinische Versorgung herzchirurgischer Patienten – Hämodynamisches Monitoring und Herz-Kreislauf“. AWMF-Registernummer 001–016. Version 3.1 (01.12.2017, zurzeit in Überarbeitung). Im Internet: register.awmf.org/assets/ guidelines/001-016l_S3_Intensivmedizinische_Versorgung- Haemodynamisches-Monitoring_2018-06-abgelaufen.pdf; Zugriff: 30.08.2024
[10] Dönitz S. S3-Leitlinie „Intensivmedizinische Versorgung herzchirurgischer Patienten – Hämodynamisches Monitoring und Herz-Kreislauf“. Viel Wissenswertes auf 328 Seiten. PflegenIntensiv 2018 (4): 33–36
[11] American College of Surgeons. Advanced Trauma Life Support® Student Course Manual. Tenth Edition 2018. ISBN 78–0–9968262–3–5
[12] Bundesärztekammer. Querschnitts-Leitlinien zur Therapie mit Blutkomponenten und Plasmaderivaten – Gesamtnovelle 2020. Im Internet: www.wbbaek.de/fileadmin/user_upload/_old-files/downloads/pdf-Ordner/MuE/Querschnitts-Leitlinien_BAEK_zur_ Therapie_mit_Blutkomponenten_und_Plasmaderivaten- Gesamtnovelle_2020.pdf; Zugriff: 30.08.2024
[13] Deutsche Gesellschaft für Ernährungsmedizin (Hrsg.). S2k-Leitlinie Klinische Ernährung in der Intensivmedizin. AWMF-Registernummer 073–004. Version 2.0 (Stand 30.06.2018). Aktuel Ernahrungsmed 2018; 43: 341–408. doi: doi.org/10.1055/a-0713-8179. Im Internet: register.awmf.org/de/leitlinien/detail/073-004; Zugriff: 30.08.2024
[14] DGAI. S3-Leitlinie „Lagerungstherapie und Mobilisation von kritisch Erkrankten auf Intensivstationen“. AWMF-Registernummer 001–015. Version 3.0 (Stand 25.07.2023). Im Internet: register.awmf.org/de/leitlinien/detail/001-015; Zugriff: 30.08.2024
[15] Dönitz S. S3-Leitlinie „Einsatz der extrakorporalen Zirkulation (ECLS/ECMO) bei Herz- und Kreislaufversagen. Organersatz für Herz und Lunge“. PflegenIntensiv 2021 (2): 23–27
[16] Lotz G. Organersatzverfahren: Update Herzersatz- und -unterstützungsverfahren. Anästhesiol Intensivmed Notfallmed Schmerz- ther 2020; 55: 150–164
[17] Oczenski W, Hrsg. Atmen – Atemhilfen. 11., überarb. Aufl. Stuttgart: Thieme; 2023
[18] Deutsche Gesellschaft für Thorax-, Herz- und Gefäßchirurgie. S3-Leitlinie „Einsatz der extrakorporalen Zirkulation (ECLS/ECMO) bei Herz- und Kreislaufversagen“. AWMF-Registernummer 011–021. Version 1.0 (Stand 20.08.2020). Im Internet: www.awmf.org leitlinien/detail/ll/011-021.html; Zugriff: 30.08.2024
[19] mediset.de/wundheilungsstoerung
[20] AWMF. S3-Leitlinie „Prophylaxe der venösen Thromboembolie (VTE)“. AWMF-Registernummer 003–001. Version 3.0 (Stand 15.10.2015, zurzeit in Überarbeitung). Im Internet: register.awmf.org/de/leitlinien/detail/003-001; Zugriff: 30.08.2024