Der US-amerikanische Intensivmediziner Marin Kollef ist einer der führenden Wissenschaftler, die neue Konzepte gegen nosokomiale Infektionen entwickeln und in klinischen Studien prüfen. Er veröffentlichte jetzt eine ausführliche Übersicht über den aktuellen Stand wissenschaftlich begründeter Präventionsmaßnahmen.
Das Autorenteam um Marin Kollef führte als Grundlage seiner Arbeit eine Literaturrecherche in medizinischen Datenbanken durch. Suchworte waren Intensivmedizin, Antibiotikaresistenz, nosokomiale Infektionen, Erfassung, Prävention und intestinales Mikrobiom. Die Ergebnisse der Recherche werden aufgrund eigener, langjähriger Erfahrungen gewichtet. Es handelte sich insgesamt um eine narrative Übersichtsarbeit [1].
Erhebungen zur Prävalenz. Die erste Prävalenzstudie zur Häufigkeit nosokomialer Infektionen auf Intensivstationen wurde 1995 von Vincent und Mitarbeitern auf europäischen Intensivstationen initiiert. Die Studie ging als EPIC-Studie (European Prevalence of Infection in Intensive Care) in die Literatur ein und wurde in der Folge vielfach zitiert. Im Ergebnis zeigte sie, dass von 10.038 Patientinnen und Patienten (im Folgenden: Patienten), die in einer einzigen Woche auf den Intensivstationen zahlreicher Teilnehmerländer lagen, 2.064 (20,6 %) an einer auf eben dieser Intensivstation erworbenen Infektion litten. Häufigstes Problem war dabei mit 46,9 % eine nosokomiale Pneumonie, gefolgt von Harnwegs- (17,6 %) und Blutstrominfektionen (12,0 %).
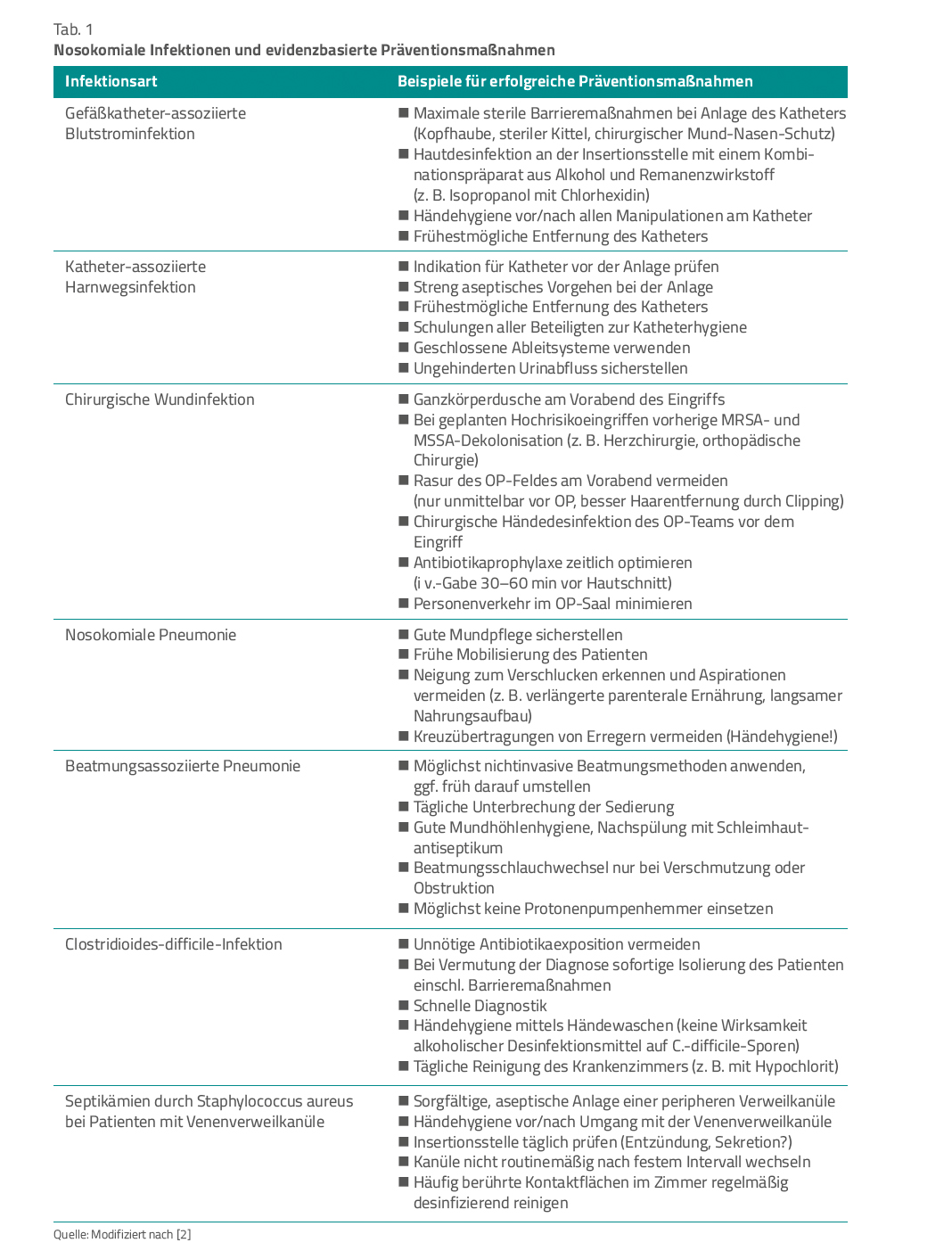
Eine zweite von Vincent durchgeführte Prävalenzstudie im Jahr 2009 (EPIC II) ergänzte diese Daten und zeigte, dass 71 % von 13.796 Intensivpatienten in der Studienwoche Antibiotika erhielten. Eine im Jahr 2017 durchgeführte dritte Studie mit ähnlicher Methodik (EPIC III) zeigte eine immer noch vergleichbare Häufigkeit und Verteilung der Infektionsdiagnosen auf europäischen Intensivstationen. Durch die inzwischen in vielen Zentren etablierten Hygiene- und Präventionsmaßnahmen (Tab. 1) war somit immer noch keine wesentliche Reduktion der Häufigkeit von Infektionen auf Intensivstationen erreicht worden.
Erregerspektrum. Die Autoren stellen das während dieser drei Untersuchungsphasen ermittelte Erregerspektrum dar. Besonders zu erwähnen sind hierbei die zunehmende Bedeutung von Acinetobacter species bei Device-assoziierten Infektionen, aber auch die kontinuierliche Rolle von Koagulase-negativen Staphylokokken, Cutibakterien und Staphylococcus aureus.
Neben der in den Industrienationen etwas rückläufigen Bedeutung von Methicillin-resistenten Staphylococcus-aureus-Stämmen (MRSA) spielen vermehrt (multi)resistente gramnegative Infektionserreger wie multiresistente E.-coli- oder Klebsiella-Stämme eine Rolle.
In den USA wurden in den vergangenen Jahren vermehrt Häufungen von nosokomialen Infektionen durch Carbapenemase-bildende Klebsiella-pneumoniae-Stämme beobachtet, deren Behandlung mit Reserveantibiotika wie Tigecyclin oder in schweren Fällen Colistin relativ unbefriedigend ist. In den drei EPIC-Studien stieg der Prozentsatz problematischer gramnegativer Erreger von 62,2 % im Jahr 2007 auf 67,1 % im Jahr 2017 an, während Infektionen unter Beteiligung von MRSA von 10,2 % auf 4,6 % abnahmen. Letzteres dürfte eine Folge intensiver Hygieneprogramme sein, die sich auf diesen Erreger fokussiert haben. Zuletzt spielen auch Vancomycin-resistente Enterokokken (VRE) eine zunehmende Rolle.
Die Rolle des Darmmikrobioms. Die Bedeutung der patienteneigenen Kolonisationsflora als Abwehrschild gegen das Eindringen von nosokomialen Erregern ist erst im letzten Jahrzehnt in den Fokus der Wissenschaft gerückt. Die Zerstörung oder zumindest Zurückdrängung der protektiv wirkenden eigenen Flora erfolgt vor allem bei beatmeten Intensivpatienten durch die Gabe von Antibiotika, die fehlende oder reduzierte Darmmotorik, eine Durchblutungsminderung der Darmschleimhaut und das Fehlen der gewohnten natürlichen Ernährung. Der Forschung zur Erhaltung der protektiven Flora oder deren Unterstützung durch oral verabreichte Probiotika dürfte in den kommenden Jahren eine mindestens ebenso große Bedeutung zukommen wie der Entwicklung neuer Antiinfektiva.
Neue Antibiotika in der Entwicklung. Obwohl sich die Entwicklung und Markteinführung neuer Substanzen im letzten Jahrzehnt deutlich verlangsamt hat, kamen in den vergangenen Jahren einige Neuentwicklungen auf den Markt.
Bei den gegen grampositive Keime wirkenden Antibiotika handelt es sich um die Vancomycin-ähnlichen Substanzen Dalbavancin und Oritavancin sowie das bereits seit 2015 in Europa zugelassene Oxazolidinon Tedizolid. Letzteres stellt eine Weiterentwicklung des seit 2000 verfügbaren Linezolid dar. Tedozolid hat eine auf Gewichtsbasis stärkere MRSA-Wirksamkeit und kann daher niedriger dosiert werden als Linezolid. Letzteres war das erste klinisch zugelassene Antibiotikum aus der Gruppe der Oxazolidinone, das inzwischen einen breiten Einsatz in der Klinik gefunden hat, insbesondere bei Infektionen durch MRSA und Vancomycin-resistente Enterokokken (VRE).
Dalbavacin ist seit 2016 in Deutschland für die Behandlung schwerer bakterieller Haut- und Weichteilinfektionen verfügbar. Ob es bezüglich der Verträglichkeit tatsächlich Vorteile gegenüber Vancomycin besitzt, ist noch unklar. Aufgrund der sehr langen Halbwertszeit braucht diese Substanz nur einmal wöchentlich verabreicht zu werden.
Eine bedeutsame Neuerung stellen die beiden Cephalosporine in Kombination mit b-Lactamase-Inhibitoren Ceftazidim/Avibactam und Ceftolozan/Tazobactam dar. In der Kombination Ceftazidim/Avibactam wurde das bewährte Pseudomonas-wirksame Drittgenerations-Cephalosporin Ceftazidim mit dem Inhibitor Avibactam kombiniert.
Dieser hemmt wirksam die enzymatische Inaktivierung von Ceftazidim durch Breitspektrum-Cephalosporinasen und einige Carbapenemasen. Die Wirkung gegen resistente Pseudomonas-aeruginosa-Stämme wird ebenfalls verbessert. Zugelassen ist die Substanzkombination für komplizierte Harnwegsinfekte, nosokomiale Pneumonien, Beatmungspneumonien sowie lokalisationsunabhängig für schwere Infektionen mit schwer therapierbaren gramnegativen Erregern.
Die Kombination von Ceftolozan mit Tazobactam hat ein vergleichbares Indikationsspektrum. Damit stellen die Wirkstoffkombinationen angesichts der fortschreitenden Resistenzentwicklung mit multiresistenten gramnegativen Erregern eine Behandlungsoption dar.
Neues zur Prävention. Die Autoren gehen abschließend auf zu erwartende Neuerungen in der Prävention nosokomialer Infektionen ein. Hier erschließt sich möglicherweise das größte Innovationspotenzial. Aktuell wird in den USA intensiv an Vakzinen gegen die Toxine von Clostridioides difficile und gegen die Endotoxine gramnegativer Stäbchenbakterien geforscht. Ein monoklonaler Antikörper gegen das Toxin B von Clostridium difficile wurde bereits klinisch eingeführt (Präparat Bezlotoxumab).
Große Hoffnungen werden in die seit 1915 bekannten Bakteriophagen (bakterienzerstörende, für den Menschen apathogene Viren) gesetzt. Die einzelnen Phagen können spezifisch für bestimmte problematische Bakterien gezüchtet und als Cocktail gegen eine Reihe von Problembakterien eingesetzt werden. Klinische Heilungen bei verzweifelten Fällen von Infektionen, bei denen kein verfügbares Antibiotikum mehr wirksam war, sind bereits beschrieben worden.
Auf dem Gebiet der Desinfektion werden Fortschritte durch antimikrobielle Oberflächen und Werkstoffe, Weiterentwicklung von nonmanuellen Desinfektionsmethoden wie UV-Lichtsäulen, Wasserperoxid-Verneblungsgeräte und photoaktivierbare Oberflächen erwartet. Ein Beispiel für diese Entwicklungen sind kupferhaltige (und dadurch antibakteriell wirksame) Türklinken, die bereits in Deutschland für medizinische Einrichtungen angeboten werden.
Die konventionellen Reinigungsmethoden durch manuelle Wischdesinfektion sollten dadurch aber keinesfalls ersetzt werden. Durch die antibakteriellen Materialien und Oberflächen kann jedoch eine zusätzliche Inaktivierung von Erregern an schwer erreichbaren Lokalisationen oder im Intervall zwischen den Reinigungsmaßnahmen erreicht werden.
Kommentar
Die neuen Aspekte dieser Analyse liegen in der Tat auf dem Gebiet der Impfungen gegen nosokomiale Erreger. Patienten, bei denen größere operative Eingriffe mit flankierendem Antibiotikaeinsatz bevorstehen, könnten möglicherweise davon profitieren, dass sie zuvor aktiv gegen das Toxin B von Clostridioides difficile geimpft werden. Meist geht derartigen Eingriffen eine längere Planungsphase voraus, sodass die Chance besteht, den Aufbau einer Immunität gegen diesen Erreger abzuwarten. Eine pharmazeutische Firma in den USA hat die Entwicklung einer Clostridium-difficile-Vakzine in ihr Forschungsprogramm aufgenommen.
Die Phagentherapie hat ebenfalls neue Aufmerksamkeit erfahren und wird an verschiedenen Zentren intensiv beforscht. Einzelfälle, bei denen es gelang, Infektionen mit hochgradig resistenten Erregern durch Phagenanwendung allein oder in Kombination mit partiell wirksamen Antibiotika zu heilen, wurden mehrfach beschrieben.
Ein Fallbericht aus Shanghai schilderte das therapeutische Vorgehen bei einer 63-jährigen Diabetikerin, die an einer chronischen Harnwegsinfektion durch einen multiresistenten Klebsiella-pneumoniae-Stamm litt. Mehrere antibiotische Therapiezyklen mit Reserveantibiotika hatten keinen Erfolg, führten jedoch zu erheblichen Nebenwirkungen.
Über sieben Monate traten immer wieder symptomatische Harnwegsinfektionen auf, die die Patientin belasteten. Die Phagenspezialisten entwickelten einen individualisierten Cocktail von fünf Klebsiella-spezifischen Phagen, den sie retrograd in die Blase der Patienten instillierten.
In der dritten Therapiephase wurden die Phagen mit dem Antibiotikum Trimethoprim/Sulfamethoxazol kombiniert, obwohl dieses resistent getestet war. In Kombination mit dem Phagencocktail wurde der Erreger jedoch wieder sensibel und die Patientin konnte erfolgreich geheilt werden, was durch negative Urinproben bewiesen wurde [3].
Eine Erfolg versprechende Applikationsform ist auch die lokale Aufbringung von spezifischen Phagensuspensionen auf infizierte Wunden, beispielsweise Brandwunden, die mit Pseudomonas aeruginosa infiziert sind [4]. Weitere Forschungen auf diesem Gebiet werden angesichts zunehmender Antibiotikaresistenzen sehnlich erwartet.
In den Industrieländern sind die Raten von MRSA rückläufig, während die Drittgenerations-Cephalosporin-resistenten Enterobakterien und Vancomycin-resistenten Enterokokken ein wachsendes Problem darstellen. Die Ausbreitung multiresistenter Erreger ist nicht nur durch Maßnahmen der Krankenhaushygiene, wie zum Beispiel Händedesinfektion, Screening und Isolation, zu verhindern.
Viele der Infektionen stehen in engem Zusammenhang mit der Schwere der Grunderkrankung und der Anzahl der Begleiterkrankungen – Faktoren, die sich nicht allein durch Prävention beeinflussen lassen. Die Patienten werden immer älter und kränker und die Medizin ermöglicht immer invasivere diagnostische und therapeutische Maßnahmen.
Ein Faktor für den hohen Antibiotikaverbrauch ist, dass häufig empirisch behandelt wird, ohne den Erreger und seine Resistenzsituation zu kennen. Damit kann eine optimierte Diagnostik mit schnellerer Erregeridentifikation eine zielgerichtete Therapie mit möglicherweise weniger breit wirksamen Antibiotika ermöglichen, sodass der Selektionsdruck auf Bakterien durch Breitspektrumantibiotika abnimmt.
Des Weiteren ist die konsequente Umsetzung von Maßnahmen erforderlich, die die Qualität der Antiinfektiva-Behandlung bezüglich Auswahl, Dosierung, Applikation und Anwendungsdauer sichern, um das beste klinische Behandlungsergebnis zu erreichen.
Die zunehmende Antibiotikaresistenz macht eine rationale Antiinfektiva-Verordnung (Antibiotic Stewardship, ABS) notwendig. Nur so kann mit hoher Wahrscheinlichkeit eine Reduktion der Inzidenz multiresistenter Erreger erzielt und die Wirksamkeit der vorhandenen Antiinfektiva gesichert werden.
[1] Kollef MH et al. Nosocomial infection. Crit Care Med 2021; 49: 169–186
[2] Fernando SA, Gray TJ, Gottlieb T. Healthcare-acquired infections: prevention strategies. Internal Medicine Journal 2017; 47: 1341–1351
[3] Baoa J et al. Non-active antibiotic and bacteriophage synergism to successfully treat recurrent urinary tract infection caused by extensively drug-resistant Klebsiella pneumoniae. Emerging Microbes and Infection 2020; 9: 771–774
[4] Jault P et al. Efficacy and tolerability of a cocktail of bacteriophages to treat burn wounds infected by Pseudomonas aeruginosa (PhagoBurn): a randomized, controlled, double-blind phase 1/2 trial. Lancet Infect Dis 2019; 19: 35–45