Jährlich wird mehreren Millionen Krankenhauspatienten Sauerstoff verabreicht. Allerdings kann die Gabe des Medikaments Sauerstoff in bestimmten Fällen nicht nur ohne Nutzen sein, sondern sogar zu erhöhter Sterblichkeit führen. Eine neue Leitlinie zur Sauerstofftherapie in der Akutbehandlung im Krankenhaus und im Rettungsdienst zielt auf eine Erhöhung der Patientensicherheit.
Die Erstellerinnen und Ersteller (im Folgenden: Ersteller) der S3-Leitlinie „Sauerstoff in der Akuttherapie beim Erwachsenen“ (Textkasten: Die Leitlinie) sind der Ansicht, dass Sauerstoff in der Akutmedizin in Deutschland häufig unkritisch zum Einsatz kommt, nicht zuletzt weil bislang eine Leitlinie fehlte. Den Erstellern zufolge kann medizinisches Fachpersonal die Relevanz einer Hypoxämie kaum einschätzen und hat auch kein Bewusstsein für eine Hyperoxämie. Zudem würden Ärztinnen und Ärzte eine Sauerstofftherapie in den meisten Fällen weder ausreichend schriftlich verordnen noch dokumentieren [1].
Die Leitlinie
Im Juni 2021 veröffentlichte die Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin e. V. (DGP) als federführende Gesellschaft die S3-Leitlinie „Sauerstoff in der Akuttherapie beim Erwachsenen“. Zahlreiche weitere Fachgesellschaften und Verbände haben an der Erstellung mitgewirkt. Die Leitlinie hat einen Umfang von 119 Seiten und steht auf der Website der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) kostenlos zum Download bereit [1].
Die Leitlinie verfolgt daher die Ziele [1],
- lokale Standards der Sauerstofftherapie in stationären und präklinischen Einrichtungen zu fördern,
- Indikationen für die Sauerstofftherapie in der Akutmedizin festzulegen – möglichst krankheitsunabhängig,
- Orientierungswerte der Sauerstoffsättigung unter Sauerstofftherapie vorzuschlagen,
- Risiken und unerwünschte Arzneimittelwirkungen von Sauerstoff aufzuzeigen und Hyperoxämie zu vermeiden,
- schriftliche Verordnungen der Sauerstofftherapie zu fördern,
- praktische Empfehlungen zur Sauerstofftherapie (Verordnung, Überwachung, Dokumentation, Beendigung) zu geben.
Zielgruppe. Die Leitlinie richtet sich an Ärztinnen und Ärzte (insbesondere der beteiligten Fachgesellschaften), an Pflegepersonal im stationären Bereich, Pflegefachpersonal der Intensivstationen sowie Rettungsfachpersonal (Rettungssanitäterinnen und -sanitäter, Rettungsassistentinnen und -assistenten, Notfallsanitäterinnen und -sanitäter).
Physiologische Grundlagen
Wesentliche physiologische Grundlagen dienen dem Verständnis der Leitlinien-Empfehlungen.
Blutgase. Körperzellen benötigen Sauerstoff, um Energie erzeugen zu können. Aufgabe der Lunge ist die Abgabe von Sauerstoff an das Blut und die Aufnahme von Kohlendioxid aus dem Blut, das in die Umgebung abgeatmet wird. Dabei lässt sich das respiratorische System grob in zwei Bereiche unterteilen [1]:
- die Lunge als gasaustauschendes Organ (Diffusion)
- der An- und Abtransport der Gase über die Atempumpe (Ventilation)
Zu unterscheiden sind zwei Typen des Atemversagens:
- Typ 1 – pulmonale Insuffizienz: Die Aufnahme von Sauerstoff ist gestört, Kohlendioxid wird jedoch noch abgegeben [3].
- Typ 2 – ventilatorische Insuffizienz: Die Aufnahme von Sauerstoff und die Abgabe von Kohlendioxid sind gestört [1, 3].
Sauerstofftransport. Im Blut erfolgt der Sauerstofftransport hauptsächlich durch Bindung der Sauerstoffmoleküle an das Hämoglobin der Erythrozyten. Zur Bestimmung der Sauerstoffmenge im Blut dient entweder die Sauerstoffsättigung des Hämoglobins (SO2) oder der arterielle Sauerstoffpartialdruck (PaO2):
- SO2 sagt aus, zu wie viel Prozent das Hämoglobin zum Zeitpunkt der Messung mit Sauerstoff gesättigt ist. Der Wert wird entweder fotometrisch oder (ungenauer) aus dem Sauerstoffpartialdruck im arteriellen Blut (SaO2) nach verschiedenen Formeln ermittelt. Zudem lässt er sich auch nichtinvasiv mittels Pulsoxymeter (periphere kapillare Sauerstoffsättigung, SpO2) feststellen.
- PaO2 ist mittels Blutgasanalyse (BGA) zu bestimmen und zur Beurteilung von Gasaustauschstörungen der Lunge genauer, aber aufwendiger (arterielle Punktion erforderlich).
Zur Berechnung des arteriellen Sauerstoffgehalts (CaO2, C = Content) eignet sich – vereinfacht dargestellt – folgende Formel:
CaO2 = Hb x SO2
Sie verdeutlicht das bereits Besprochene. Hämoglobin fungiert als Transporter für den Sauerstoff. Je mehr die Transporter beladen sind, umso mehr Sauerstoff wird transportiert. Im Wesentlichen sind also die Hämoglobinkonzentration (Hb) – gemessen in Gramm pro Deziliter: g/dl – und die Sauerstoffsättigung maßgeblich für den Sauerstoffgehalt des Bluts.
Es könnte der Eindruck entstehen, dass bei einer weitgehend im Normbereich liegenden Hämoglobinkonzentration nur noch die Sauerstoffsättigung herangezogen zu werden braucht, um das Sauerstoffangebot für die Körpergewebe abzuschätzen. Das stimmt insoweit, dass ein Sauerstoffmangel im Blut natürlich auch zu Sauerstoffmangel im Gewebe führen kann. Aber auch bei völlig normalem Sauerstoffgehalt des Bluts kann das Gewebe unzureichend mit Sauerstoff versorgt werden. Diese Situation kann auftreten, wenn die Herzfrequenz und/oder das Schlagvolumen so niedrig sind, dass das Gewebe trotz des ausreichend vorhandenen Sauerstoffs/Hämoglobins nicht adäquat versorgt werden kann.
Wichtig zu wissen: Die Versorgung der Organe und Gewebe mit O2 wird häufig als Gewebeoxygenierung bezeichnet. Sowohl SO2 als auch SaO2 sind nicht geeignet, um die Gewebeoxygenierung abzuschätzen [1]. Zu deren Berechnung bzw. zur Ermittlung des Sauerstoffangebots (DO2, D = Delivery) ist das Herzzeitvolumen (HZV: Herzfrequenz x Schlagvolumen) hinzuzuziehen. Dabei gilt folgende Formel:
DO2 = HZV x CaO2
Beide Formeln verdeutlichen, dass die Sauerstoffversorgung des Gewebes (DO2) v. a. von Hb und HZV abhängen. PaO2 und SO2 bilden DO2 hingegen nur unzureichend ab [1]!
Hypoxie und Hypoxämie. Die Begriffe Hypoxie und Hypoxämie sollten nicht verwechselt werden, obwohl sie oft gleichgesetzt sind. Bei einer Hypoxämie ist der Leitlinie zufolge der Sauerstoffpartialdruck oder der Sauerstoffgehalt im arteriellen Blut erniedrigt.
Eine Hypoxie bezeichnet dagegen die Unterversorgung von Organen und Gewebe mit Sauerstoff. Laut Leitlinie wird bei Erwachsenen die Hypoxämie meist für einen PaO2 < 60 Millimeter-Quecksilbersäule (mmHg) und eine SaO2 < 90 % definiert [1].
Wichtig zu wissen: Somit kann eine Gewebehypoxie z. B. auf Diffusionsstörungen in der Lunge, Aufenthalt in großer Höhe, aber auch auf einer Anämie beruhen.
Wichtige Empfehlungen
Von den insg. 34 Empfehlungen der Leitlinie – inklusive Praxistipps – sind nachfolgend sechs näher beschrieben.
EMPFEHLUNG: Behandlung einer Hypoxämie (S. 26 f.) – „Die zugrundeliegenden Ursachen einer Hypoxämie sollen festgestellt und behandelt werden. Sauerstoff soll verabreicht werden, um eine Hypoxämie und nicht um Atemnot zu behandeln“ (Empfehlungsgrad: A).
Verschiedene Studien haben die Rolle von Sauerstoff zur Linderung von Atemnot bei COPD und Krebserkrankungen untersucht. Dabei wurde der Effekt von Sauerstoff mit dem der Verabreichung von Druckluft verglichen. Andere Studien ließen die Patientinnen und Patienten (im Folgenden: Patienten) die eigene Atemnot anhand unterschiedlicher Skalen einschätzen. Insgesamt zeigte sich, dass Sauerstoff zur Linderung von Atemnot nicht effektiver als Druckluft ist. Daher sollte Sauerstoff nur verabreicht werden, um eine Hypoxämie zu behandeln. Die Leitlinie räumt jedoch ein, dass in Situationen, in denen kein verwertbares Signal aus der Pulsoxymetrie ableitbar ist – etwa im Rettungsdienst –, die Gabe von Sauerstoff an Patienten mit Atemnot vertretbar ist. Im stationären Bereich hingegen sollte in solch einer Situation eine arterielle (hilfsweise auch eine kapilläre) BGA erfolgen. Für die Praxis betont die Leitlinie außerdem den Stellenwert von Allgemeinmaßnahmen wie der Lagerung.
Bei manchen Patienten lässt sich mit einer aufrechten Oberkörperhochlagerung die Oxygenierung verbessern. Zudem kann die Flachlagerung bei morbid adipösen Patienten (BMI > 50 kg/m2) zu akutem Atemversagen führen. Schwangere mit Hypoxämie sollen zur Prophylaxe eines Vena-cava-Kompressionssyndroms eine Linksseitenlage einnehmen. Zu Atemnot ohne Hypoxämie ist der Einsatz von Opioiden gut untersucht und nachgewiesen wirksam [1].
Wichtig zu wissen: Ein nicht ableitbares Pulsoxymeter wird in einer Akutsituation so gewertet, als hätte man keines.
Behandlungsbedürftigkeit einer Hypoxämie. Der Leitlinie zufolge sollen Anwenderinnen und Anwender zur Behandlungsbedürftigkeit einer Hypoxämie vier Fragen beantworten [1]:
1. Hat der Patient Beschwerden und ist er klinisch stabil? Grundsätzlich stellt sich die Frage, ob jemand behandlungsbedürftig ist, wenn es ihm klinisch gut geht. Gemäß Leitlinie ist deshalb die Angabe von Atemnot ein wichtiger Aspekt. Weiterhin sind die Vitalzeichen zu erheben, v. a. die Bewusstseinslage (inklusive Verwirrung) und die Atemfrequenz. Eine Objektivierung ist mittels BGA möglich.
2. Wie ausgeprägt ist die Hypoxämie und ist diese anhaltend? Tritt eine Hypoxämie nur vorübergehend und selbstlimitierend auf, etwa unter Belastung oder Hustenattacken oder infolge einer im Rahmen einer Endoskopie auftretenden Hypoventilation (Nebenwirkung der Sedierung), sind sogar schwere Hypoxämien von z. B. < 1 min Dauer in der Regel unkritisch. Selbst eine mittelschwere Hypoxämie mit einer Sauerstoffsättigung zwischen 85 % und 89 % ist vermutlich auch langfristig wenig problematisch.
3. Ist der Patient an die Hypoxämie adaptiert? In bestimmten Situationen besteht eine chronische Hypoxämie, die oft über viele Wochen anhält. Abgesehen von Menschen, die in großer Höhe leben, ist dies häufig bei Patienten mit chronischer Hypoventilation, angeborenen Herzfehlern und generell auch bei Patienten mit Hyperkapnie-Risiko zu beobachten.
4. Liegen Begleiterkrankungen vor? Bei bestimmten Patienten ist die Toleranz einer Gewebehypoxie vermutlich geringer. Die Leitlinie nennt hier als Beispiele Patienten mit koronarer Herzkrankheit oder anderen Herz-Kreislauf-Erkrankungen.
Wichtig zu wissen: Hyperkapnie bedeutet, der Kohlendioxidgehalt im Blut (PaCO2) ist zu hoch. Krankheitsbilder, die häufig zu ventilatorischer Insuffizienz bis hin zu Hyperkapnie führen, sind Thorax- oder Wirbelsäulendeformitäten, strukturelle/obstruktive Lungenerkrankungen (z. B. COPD), neuromuskuläre Erkrankungen (NME), das Obesitas-Hypoventilations-Syndrom (OHS) und zentrale Atemregulationsstörungen [3].
Hyperoxämie. Genau wie die Hypoxämie ist die Hyperoxämie der Leitlinie zufolge nicht exakt definiert. Auf Meereshöhe liegt der Normalwert der Sauerstoffsättigung der Bevölkerung bei 96 %. Bei bestimmten Patientengruppen (akutes Koronarsyndrom, Schlaganfall, intraoperativ) wurden infolge einer großzügigen Sauerstoffgabe Sättigungswerte > 96 % gemessen. Die Leitlinie führt eine große Zahl Argumente gegen Hyperoxie und Hyperoxämie als Therapieziel auf [1]:
- Bei einigen Patienten führte die unnötige Verabreichung von Sauerstoff einerseits zur Austrocknung der Schleimhaut und Heiserkeit und andererseits zu Beeinträchtigungen bei Mobilisation, Nahrungsaufnahme, Trinken und Kommunikation.
- Eine Metaanalyse, die über 16.000 Patienten mit unterschiedlichen akuten Erkrankungen (u. a. Sepsis, Schlaganfall, Trauma, Herzinfarkt, Kreislaufstillstand) umfasste, zeigte mit hoher Evidenz ein erhöhtes relatives Sterberisiko.
- In einer Studie mit Sepsispatienten wurde die Hyperoxämie-Gruppe für 24 Stunden mit 100 % Sauerstoff versorgt. Laut Leitlinie war die Zahl der Patienten, die an Critical-Illness-Polyneuropathie und Myopathie litten, in der Hyperoxämie-Gruppe fast verdoppelt.
- Selbst bei Gesunden können hohe Sauerstoffkonzentrationen eine Entzündungsreaktion der Atemwege hervorrufen.
- Die vermehrte Bildung von sog. freien Sauerstoffradikalen kann zu einer Zellschädigung führen.
- Unter COPD-Patienten war die Krankenhaussterblichkeit höher (2 % versus 9 %).
- Eine Studie zeigte, dass die routinemäßige Sauerstoffgabe die Sterblichkeit nach einem Herzinfarkt nicht verbessert. Eine andere Studie zeigte hingegen, dass sich die Rate erneuter Koronarereignisse unter Sauerstoffgabe – verglichen mit Druckluft – mehr als fünffach erhöhte.
- 21 Studien mit über 7.500 Patienten ergaben, dass eine intra- und postoperative Hyperoxie die Wundheilung nicht verbesserte.
EMPFEHLUNG: Klinische Beurteilung von Hypoxämie und Hyperkapnie (S. 32 f.) – „Bei der Einschätzung von Patienten mit Atemnot sollen neben der Sauerstoffsättigung auch Atemfrequenz, Pulsfrequenz, Blutdruck, Temperatur und Bewusstseinslage bestimmt werden“ (Empfehlungsgrad: Expertenkonsens).
Laut Leitlinie existieren derzeit keine randomisiert kontrollierten Studien, die verschiedene klinische Einschätzungssysteme bei akut kranken Patienten verglichen haben. Daher beruht diese Empfehlung auf Expertenmeinungen. Die Bestimmung der Sauerstoffsättigung ist nur einer von mehreren Parametern, die problemlos bettseitig auch pflegerisches oder Rettungsfachpersonal erheben kann. Die Erhebung von 1,15 Mio. Vitalwerten bei knapp 28.000 stationären Patienten erlaubte die Festlegung kritischer Werte, bei deren Unter- oder Überschreitung eine Krankenhaussterblichkeit von ≥ 5 % zu beobachten war. Gemäß Leitlinie ließen sich dabei folgende kritische Grenzwerte identifizieren [1]:
- systolischer Blutdruck < 85 mmHg
- Herzfrequenz > 120/min
- Körpertemperatur < 35° C oder > 38,9° C
- Sauerstoffsättigung < 91 %
- Atemfrequenz ≤ 12/min bzw. ≥ 24/min
- eingeschränkte Bewusstseinslage
Wichtig zu wissen: Nicht zwingend ruft eine arterielle Hypoxämie eine Veränderung der Vitalzeichen hervor. Häufig ist allerdings eine Tachykardie zu beobachten. Die Messung der Atemfrequenz hat gemäß Leitlinie eine herausgehobene Bedeutung, ein Wert zwischen 12/min und 20/min ist normal.
EMPFEHLUNG: Pulsoxymetrie (S. 34 f.) – „Die Pulsoxymetrie soll in allen klinischen Situationen verfügbar sein, in denen Sauerstoff medizinisch verwendet wird, und zur Überwachung der Sauerstofftherapie regelmäßig eingesetzt werden“ (Empfehlungsgrad: A).
Die Pulsoxymetrie misst die Hämoglobinsättigung mittels zweier unterschiedlicher Wellenlängen. Das Verfahren beruht darauf, dass oxygeniertes Hämoglobin einen anderen Absorptionsverlauf aufweist als desoxygeniertes Hämoglobin (HHb). Das Verhältnis der beiden Absorptionen zueinander ermöglicht die Berechnung der Sättigung (SpO2). Sie lässt sich mittels Pulsoxymetrie einfach, schnell und nichtinvasiv einschätzen.
Wichtig zu wissen: Die Pulsoxymetrie ist weniger genau als die arterielle Messung der Sauerstoffsättigung mittels BGA, v. a. im Bereich unter 80 %. Im klinisch relevanten Bereich zwischen 80 % und 100 % ist die Korrelation zwischen SaO2 und SpO2 gemäß Leitlinie akzeptabel [1].
Als Praxistipp empfiehlt die Leitlinie die Verwendung von Pulsoxymetern mit Darstellung der Pulskurve (Plethysmografie) oder Signalqualitätsanzeige. Bei allen Patienten, die Sauerstoff erhalten, ist die SpO2 regelmäßig zu messen. Bei Patienten mit dunkler Hautfarbe besteht die potenzielle Gefahr, die Sauerstoffsättigung zu überschätzen! Die Schwelle für eine BGA ist daher bei Patienten mit dunkler Hautfarbe gemäß Leitlinie niedriger anzusetzen [1].
Sauerstoffquellen. Im Krankenhaus kommt der Sauerstoff entweder aus einem sechskantigen Wandanschluss (zentrale Gasversorgung) oder wird aus entsprechenden Sauerstoffflaschen entnommen. Für die Verwendung von Sauerstoffflaschen ist sicherzustellen, dass die Flasche ausreichend gefüllt ist. Der Flascheninhalt lässt sich einfach berechnen nach der Formel Flaschenvolumen x Flaschendruck in bar.
Beispiel: Eine 10 l Sauerstoffflasche weist einen Flaschendruck von 40 bar auf. Somit enthält die Flasche 400 l Sauerstoff.
Um abzuschätzen, wie lange der Inhalt der Flasche reicht, ist maßgeblich, wie viele Liter Sauerstoff pro Minute verabreicht werden. Nehmen wir an, es sollen 4 l Sauerstoff pro Minute verabreicht werden und in der Flasche sind noch 200 l Sauerstoff. Dann wäre die Flasche nach 50 Minuten leer.
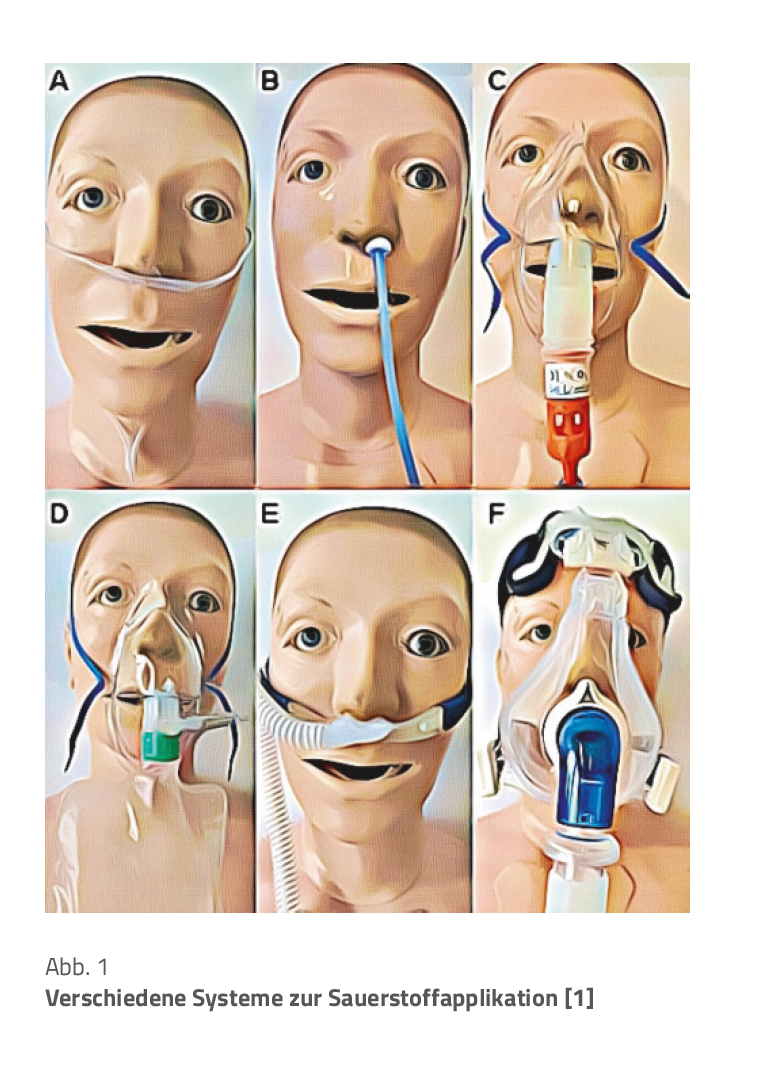
Sauerstoffapplikationssysteme. Die Möglichkeiten, Sauerstoff zu verabreichen, sind vielfältig. Sie umfassen Nasenbrillen (A in Abb. 1), Nasensonden (B), einfache Gesichtsmasken, Venturi-Masken (C), Reservoirmasken (D), High-Flow-Kanülen = HFNC (E) und Masken für non-invasive Ventilation, NIV-Masken (F).
Alle Sauerstoffapplikationssysteme haben Vor- und Nachteile, sodass Anwenderinnen und Anwender sich mit den verfügbaren Systemen vertraut machen sollten. Einfach gesagt gilt, dass Nasenbrillen und -sonden niedrige bis mittlere Sauerstoffkonzentrationen in der Größenordnung 36 % bis 54 % bereitstellen können. Abhängig von der Flussrate können einfache Gesichtsmasken etwa 40 % bis 60 % Sauerstoff liefern.
Wichtig zu wissen: Gesichtsmasken sollten nicht mit einem Sauerstofffluss < 5 l/min betrieben werden [1].
Venturi-Masken leiten Sauerstoff nach dem Bernoulli-Prinzip durch eine sich verjüngende Düse. Der Patient bekommt über die Maske ein Luft-Sauerstoff-Gemisch angeboten. Je nach Beschaffenheit ermöglichen Venturi-Masken eine kontrollierte Sauerstoffgabe zwischen 24 % und 60 %. Hohe Sauerstoffkonzentrationen lassen sich mithilfe einer Reservoirmaske oder einer HFNC erreichen.
Wichtig zu wissen: Reservoirmasken sind gemäß Leitlinie für Patienten mit Hyperkapnie-Risiko ungeeignet [1].
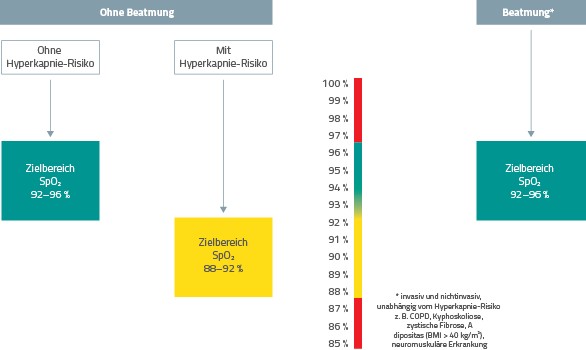
Anwendung von Sauerstoff. Die Leitlinie definiert Zielbereiche für die Sauerstoffsättigung. Dabei war die Überlegung maßgeblich, wann sowohl Hypoxämie als auch Hyperoxämie wahrscheinlich gefährdend für akut Erkrankte sind und in welchem Bereich die Sauerstofftherapie keinen Schaden anrichtet und somit als sicher angesehen werden kann [1]. Außerdem spielt eine Rolle, ob der Patient beatmet ist oder nicht und ob er ein Risiko für eine Hyperkapnie aufweist oder nicht (Abb. 2).
Für die Sauerstofftherapie ergeben sich somit drei Patientengruppen:
- In der Gruppe ohne Beatmung und ohne Hyperkapnie-Risiko wird eine Sättigung von 92 % bis 96 % angestrebt (Empfehlungsgrad: A).
- In der Gruppe ohne Beatmung mit Hyperkapnie-Risiko beträgt der Zielbereich 88 % bis 92 % (Empfehlungsgrad: A). Dieser Empfehlung liegt zugrunde, dass die Sauerstoffgabe bei manchen Patienten eine Zunahme der Hyperkapnie auslösen kann [4].
- Bei beatmeten Patienten wird generell ein Zielbereich von 92 % bis 96 % angestrebt (Empfehlungsgrad: A).
Wichtig zu wissen: Die Zielwerte beziehen sich auf Patienten in Ruhe. Unter Belastung oder bei Husten sind gemäß Leitlinie kurzfristig auch Werte unterhalb des Zielbereichs tolerabel, sofern die Sauerstoffsättigung anschließend (normalerweise < 1 min) wieder in den Zielbereich zurückkehrt [1].
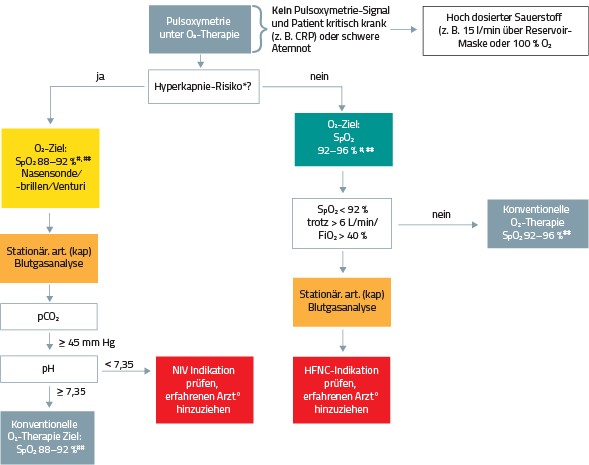
Ein Pulsoxymeter sollte frühzeitig zum Einsatz kommen (Abb. 3).
Lässt sich kein adäquates Signal ableiten und wirkt der Patient kritisch krank, kommt eine Sauerstoffmaske mit Reservoir und 15 l/min Sauerstofffluss zum Einsatz bzw. eine Beatmung mit 100 % Sauerstoff (Reanimation).
*z. B. COPD, BMI > 40 kg/m2, zystische Fibrose, Erwachsene mit neuromuskulären o. Thoraxwanderkrankungen.
# O2 unter SpO2 88 % bzw. 92 % nicht beginnen,
## O2 über 92 % bzw. 96 % beenden oder reduzieren
° erfahrener Arzt in der Diagnostik und Behandlung von Patienten mit Versagen der Atmung oder kritisch kranker Patienten CPR – kardiopulmonale Reanimation, SpO2 – pulsoximetrische Sauerstoffsättigung, O2– Sauerstoff, NIV – nicht-invasive Beatmung, HFNC – High-Flow-Sauerstoff, BMI- Body- Mass-Index, art. –arteriell, kap – kapillär, pCO2 – Kohlendioxidpartialdruck
Sauerstoffverabreichung an prähospitale Notfallpatienten
Für das Rettungsfachpersonal wird eine liberalere Vorgehensweise propagiert: Beim unbekannten Notfallpatienten „entscheiden der Ersteindruck und das klinische Bild über die Dosierung des Sauerstoffs, bis Pulsoxymeter-Werte zur Dosierungsanpassung zur Verfügung stehen. Im Zweifel gehen wir bis zum Beweis des Gegenteils auch weiterhin von lebensbedrohlichen Zuständen aus und verfolgen das Konzept, dass zunächst Sauerstoff – wenn es in die Situation passt, auch hoch dosiert – appliziert wird und im weiteren Verlauf dann an die Situation angepasst bzw. reduziert wird. Die Ableitung eines Pulsoxymeter-Wertes vor Beginn der O2-Therapie kann sinnvoll sein und wird in Abhängigkeit des Ersteindrucks abgewartet oder nicht (klinische Entscheidung!)“ [2].
Diese Vorgehensweise ist möglicherweise auch in der innerklinischen Umgebung zu empfehlen, wenn z. B. Notfallteams ausrücken, um Patienten akut in potenziell kritischem Zustand zu versorgen. Darauf geht die LL jedoch nicht ein.
Wie beschrieben, richtet sich die weitere Vorgehensweise danach, ob ein Hyperkapnie-Risiko besteht oder nicht. Daraus ergeben sich unterschiedliche Zielbereiche für die Sauerstoffsättigung. Im weiteren Verlauf ist eine arterielle BGA (hilfsweise eine kapilläre BGA) zur Therapiesteuerung anzuwenden. Die Leitlinie weist darauf hin, dass eine Sättigung oberhalb des Zielbereichs eine Reduktion oder Beendigung der Sauerstofftherapie nach sich ziehen sollte. Bleibt die Sauerstofftherapie erfolglos, ist eine erfahrene Ärztin bzw. ein erfahrener Arzt hinzuzuziehen, die bzw. der den Patienten einschätzt.
EMPFEHLUNG: Therapierefraktäre Hypoxämie (S. 68 f.)
„Patienten, die trotz Flussraten von mehr als 6 L/min Sauerstoff eine SpO2 von 92 % nicht erreichen, sollen unverzüglich durch einen erfahrenen Arzt in der Diagnostik und Behandlung von Patienten mit akutem Atemversagen oder kritisch-kranker Patienten eingeschätzt werden“ (Empfehlungsgrad: Expertenkonsens).
Im klinischen Alltag ziehen Sauerstoffflussraten > 6 l/ min oftmals den Einsatz einer O2-Reservoirmaske oder der sog. High-Flow-Sauerstofftherapie (HFNC, High-Flow Nasal Cannula) nach sich. Laut Leitlinie zeigt die klinische Erfahrung, dass Patienten mit anhaltender Hypoxämie trotz Sauerstoffgabe > 6 l/min häufig auf Intensivstationen behandelt werden müssen.
EMPFEHLUNG: Therapierefraktäre Hypoxämie (S. 69 f.)
„Eine nichtinvasive Beatmung soll primär bei Patienten mit hyperkapnischem Atemversagen mit konsekutiver Hypoxämie, besonders bei COPD mit Exazerbation und kardialem Lungenödem eingesetzt werden, bei denen der pH-Wert < 7,35 beträgt. Bei hypoxämischen und moderat hyperkapnischen Patienten kann HFNC alternativ eingesetzt werden“ (Empfehlungsgrad: A).
Wie die Leitlinie beschreibt, führt eine hoch dosierte Sauerstoffgabe an Patienten mit Risiko eines hyperkapnischen Atemversagens vielfach zu Todesfällen [1]. Bei diesem speziellen Patientenkollektiv ist die alleinige Sauerstoffgabe oft nur unzureichend – primär ist eine NIV einzusetzen. In einer Studie hatten die Patienten zunächst eine mittlere SpO2 von 84 % bis 87 %. Die bei solchen Werten oft reflexartige Verabreichung hoch dosierten Sauerstoffs sollte bei diesen Patienten unbedingt vermieden werden. Denn unter hoch dosierter Sauerstofftherapie kam es bei 22 % bis 34 % der Risikopatienten (u. a. COPD und Adipositas) zu einem signifikanten Anstieg des transkutan gemessenen Kohlendioxidpartialdrucks. Somit war das Risiko eines hyperkapnischen Atemversagens gegenüber der konservativen Sauerstofftherapie um das Drei- bis Fünffache erhöht. Eine Einschätzung seitens erfahrener Ärztinnen bzw. Ärzte ermöglicht den frühzeitigen Einsatz der NIV [1].
EMPFEHLUNG: Sauerstoff bei Verfahren mit Sedierung (S. 86 f.) – „Bei allen Verfahren mit Sedierung mit dem Ziel der erhaltenen Spontanatmung soll vor und während des Eingriffs und in der Aufwachphase die Sauerstoffsättigung kontinuierlich pulsoxymetrisch überwacht werden“ (Empfehlungsgrad: Expertenkonsens).
Für Eingriffe mit Sedierung wird häufig Propofol verwendet. In Verbindung damit treten Hypoxämien in einer Häufigkeit von 25 % bis 44 % auf. Bei bis zu zwei Dritteln der Studienteilnehmenden wurden während des Eingriffs Apnoen bzw. Hypopnoen (Verringerung der Atmungstiefe um 50 % über einen Zeitraum von wenigstens 10 Sekunden [5]) registriert. Die Leitlinien-Ersteller schließen daraus, dass die meisten Hypoxämien vermutlich auf Episoden von Hypoventilation beruhen. Daher sehen sie eine klare Indikation zur kontinuierlichen Registrierung der Pulsoxymetrie vor, während und nach solchen Eingriffen.
Wichtig zu wissen: Bei Hypoxämien unter Sedierung ist die alleinige Sauerstoffverabreichung häufig nur unzureichend wirksam, sodass zusätzliche Maßnahmen zur Behebung notwendig sind [1].
Sauerstoff nicht unkritisch verabreichen
Sauerstoff ist ein Medikament, seine unkritische Verabreichung kann gravierende Nebenwirkungen hervorrufen. Ein nicht ableitbares Pulsoxymeter wird in einer Akutsituation so gewertet, als läge keines vor. Sauerstoff sollte nur verabreicht werden, um eine Hypoxämie zu behandeln. Für die klinische Einschätzung ist die Atemfrequenz einer der wichtigsten Parameter.
Die neue Leitlinie definiert Zielbereiche der Sauerstoffsättigung, die bei spontanatmenden Patienten 92 % bis 96 % und bei Hyperkapnie-Risiko-Patienten 88 % bis 92 % umfasst. Die Leitlinie empfiehlt, unterhalb dieser Werte keine Sauerstofftherapie zu beginnen, sie oberhalb davon zu beendet oder zu reduzieren.
Für beatmete Patienten beträgt der SpO2- bzw. SaO2-Zielbereich außerhalb der Reanimation 92 % bis 96 %. Neben der Pulsoxymetrie spielt die arterielle (hilfsweise die kapilläre) BGA eine wichtige Rolle. Manche Patienten profitieren eher von einer nichtinvasiven Beatmung (NIV) anstelle einer herkömmlichen Sauerstofftherapie. Für andere ist zu prüfen, ob eine High-Flow-O2-Anwendung (HFNC) als Eskalationsstufe einzusetzen ist. Erfahrene Ärztinnen und Ärzte sind zur Einschätzung der Patienten frühzeitig einzubeziehen, um die geeignete Therapie festzulegen.
[1] Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin e. V. „S3-Leitlinie: Sauerstoff in der Akuttherapie beim Erwachsenen“. Langversion 1.0, Stand 06/2021. AWMF-Registernummer: 020 – 021. Im Internet: www.awmf.org/uploads/tx_szleitlinien/020–021l_ S3_Sauerstoff-in-der-Akuttherapie-beim-Erwachsenen_2021–06.pdf
[2] AMLS (Advanced Medical Life Support) Deutschland. Stellungnahme zur S3 Leitlinie „Sauerstoff in der Akuttherapie beim Erwachsenen“ für Instruktorinnen und Instruktoren. Stand Juni 2021
[3] Weigand M, Hecker A, Mayer K, Michalski D (Hrsg.). Intensivmedizin compact. 1. Aufl. Stuttgart: Thieme; 2021
[4] Suttorp N, Möckel M, Siegmund B, Dietel M (Hrsg.). Harrisons Innere Medizin. 20. Aufl. Berlin: ABW Wissenschaftsverlag; 2020
[5] DocCheck Flexikon. Im Internet: flexikon.doccheck.com/de/Hypopnoe