Nach sechs Jahren liegt die erste Aktualisierung der Leitlinie zur Analgesie, zur Sedierung und zum Delirmanagement in der Intensivmedizin vor. Viele Empfehlungen der Ursprungsversion sind erhalten geblieben. Dennoch enthält die überarbeitete Leitlinie einige Änderungen, die die Arbeit auf den Intensivstationen nachhaltig beeinflussen können.
Die Veröffentlichung der S3-Leitlinie „Analgesie, Sedierung und Delirmanagement in der Intensivmedizin“ im Jahr 2015 bedeutete für die Intensivmedizin und -pflege in Deutschland einen Paradigmenwechsel: Das Ziel wacher, aufmerksamer, schmerz-, angst- und delirfreier intensivmedizinisch behandelter Patientinnen und Patienten (im Folgenden: Patienten), die aktiv an ihrem Genesungs- und Behandlungsprozess teilnehmen, hielt nicht nur vermehrt Einzug in die Therapiepläne der Intensivstationen, sondern fand zunehmend auch Beachtung in wissenschaftlichen Untersuchungen der nachfolgenden Jahre.
Die sich hieraus ergebende veränderte Evidenz in den Bereichen der Analgesie, der Sedierung und des Delirmanagements machte die Überarbeitung der Leitlinie nötig. Die aktualisierte Fassung [1] wurde unter Federführung der Deutschen Gesellschaft für Anästhesiologie und Intensivmedizin (DGAI) und der Deutschen Interdisziplinären Vereinigung für Intensiv- und Notfallmedizin (DIVI) entwickelt und kürzlich auf der Website der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) veröffentlicht. 15 weitere medizinische und pflegerische Organisationen, darunter etwa die Deutsche Gesellschaft für Fachkrankenpflege und Funktionsdienste (DGF) und die Deutsche Gesellschaft für Internistische Intensivmedizin und Notfallmedizin (DGIIN) haben an der Überarbeitung mitgewirkt.
Zwar sind viele Empfehlungen der ursprünglichen Leitlinie erhalten geblieben, doch gibt es auch diverse Änderungen, die die Arbeit auf den Intensivstationen nachhaltig beeinflussen können. Diese Änderungen werden im Folgenden näher erläutert. Dabei ist zu beachten, dass für die Aktualisierung die Literatursuche nur neue, wegweisende Publikationen ab Mai 2019 einbezogen wurden.
Die überarbeitete Leitlinie ist in Form und Struktur wie die vorherige aufgebaut. Sie unterteilt sich im Wesentlichen in einen allgemeinen Teil, der sich mit der Analgesie, der Sedierung und dem Delirmanagement erwachsener Patienten befasst, und einen Teil mit Besonderheiten spezieller Patientengruppen. Ein weiterer Teil ist der Analgesie, Sedierung und dem Delirmanagement von Kindern sowie den Besonderheiten älterer Patienten gewidmet. Abschließend beschreibt die Leitlinie ökonomische Aspekte sowie Möglichkeiten ihrer Implementierung und Umsetzung.
Delirprävention: Nichtpharmakologische Maßnahmen gewinnen an Bedeutung
Als Risikofaktoren in der Intensivmedizin berücksichtigt die neue Leitlinie neben bestehenden Komorbiditäten, kognitivem Defizit, Immobilität, chronischen Schmerzen und der Schwere der Erkrankung auch seit Längerem eingesetzte Assessments wie den ASA-Status (Scoring-System der American Society of Anesthesiologists zur Einteilung von Patienten nach ihrem körperlichen Zustand) und den APACHE-Score (Acute Physiology And Chronic Health Evaluation: Verfahren zur Vorhersage der Überlebenswahrscheinlichkeit von Patienten einer Intensivstation). Auch ein höheres Lebensalter ist nun als Risikofaktor definiert.
Präventiv wird in der neuen Leitlinie nochmals größerer Wert auf nichtpharmakologische Maßnahmen gelegt. Als einer der größten Risikofaktoren für die Entwicklung eines Delirs ist eine Sedierung – insbesondere eine Übersedierung – zu vermeiden. Große Bedeutung für die Delirprävention bei allen Patientengruppen hat zudem ein geordneter Tag-Nacht-Rhythmus.
Zu wichtigen aktivierenden Maßnahmen, die tagsüber erfolgen sollten, zählen insbesondere eine frühe Mobilisation und eine zeitliche Reorientierung. Diese sollten durch einen frühestmöglichen und wenn möglich ständigen Einsatz patienteneigener Hilfsmittel wie Sehhilfen und Hörgeräte sowie eine intensive Kommunikation erfolgen. Alternative Kontaktmöglichkeiten isolierter Patienten sind auszuschöpfen, um auch die Angehörigen in den Genesungsprozess einbinden zu können. Dieser Punkt gewinnt gerade vor dem Hintergrund der sich abspielenden pandemischen Lage an Aktualität, da es zunehmend Hinweise gibt, dass COVID-19-erkrankte Patienten häufig ein Delir erleiden, sodass ein entsprechendes Monitoring sowie eine leitliniengerechte Prävention erfolgen sollten.
Neben den bereits empfohlenen schlaffördernden Maßnahmen, z. B. mittels Ohrstöpseln und Schlafbrillen sowie Lärmreduktion und Lichtanpassung, sollte auch eine nächtliche Betreuung im Patientenzimmer auf ein absolut notwendiges Maß beschränkt sein. Routinemaßnahmen, z. B. das Wechseln von Beatmungsschläuchen, sollten möglichst tagsüber bzw. vor Beginn der Nachtruhe erfolgen. Für ältere Patienten bietet sich präventiv eine nächtliche Melatoningabe an.
Kommunikation fördern
Patienten, die einen längeren Aufenthalt auf der Intensivstation hatten, sind bekanntermaßen gefährdet, eine Posttraumatische Belastungsstörung (PTSD) zu entwickeln. Als Risikofaktoren besonders hervorzuheben sind neben einer längeren Sedierung das Entwickeln eines Delirs, der Einsatz von Benzodiazepinen sowie empfundene Angst.
Neu als Spätfolge eines belastenden Intensivaufenthalts definiert wurde in der Leitlinie die Entwicklung eines Post Intensive Care Syndrome (PICS), das neben den psychischen Faktoren der PTSD auch die physischen und kognitiven Folgen der intensivbehandlungsspezifischen Umstände berücksichtigt. Zur zentralen Präventionsstrategie von Spätfolgen der Intensivbehandlung gehört eine angemessene Kommunikation. Sie verringert zum einen das Risiko einer potenziellen Traumatisierung und wirkt zum anderen der Entstehung von Folgeschäden entgegen, indem traumasensible Kommunikation behandlungsbedingte Stressoren reduziert. Dies betrifft insbesondere belastende Erlebnisse im Zuge fehlender Realitätsorientierung.
Um diese Form der Kommunikation zu ermöglichen, ist bei allen intensivmedizinisch behandelten Patienten die Kommunikationsfähigkeit systematisch zu erfassen. Darauf basierend sind ihnen unterstützende oder alternative Kommunikationsmethoden anzubieten. Die geläufigsten Kommunikationsmethoden wie Lippenlesen, Kopfbewegungen und Gesten sind sehr zeitaufwendig und dennoch meist unzureichend, um alle Kommunikationsbedürfnisse der Patienten zu erfüllen. Dies wiederum kann zu Frust und weiteren Belastungen führen.
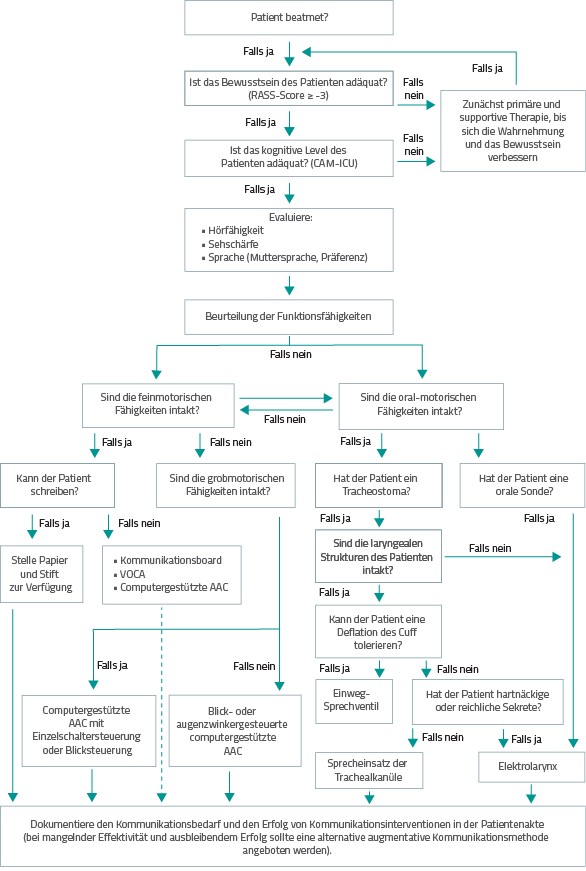
Zur Verbesserung der Kommunikation empfiehlt die Leitlinie die Verwendung eines Kommunikationsalgorithmus, um den Ansatz der Auswahl verschiedener augmentativer und alternativer Kommunikationsmethoden (AAC) zu standardisieren (Abb. 1).
Der Einsatz von Kommunikationsinterventionstypen, ob Sprechventil, Elektropharynx oder Hightechgeräte, zieht eine deutliche Verbesserung der Kommunikationsfähigkeit der Patienten nach sich und ist – soweit möglich – auch in Kombination anzuwenden. Für die Auswahl einer passende Intervention sollten Intensivstationen mit verschiedenen AAC ausgestattet und das Personal im Umgang mit diesen geschult sein.
Gezieltes Monitoring erforderlich
Um frühzeitig auf unerwünschte Ereignisse im Zusammenhang mit der Intensivtherapie reagieren zu können, bedarf es eines regelmäßigen, gezielten Monitorings von Analgesie, Sedierung, Angst und Delir mittels valider Scoringsysteme oder apparativer Messverfahren. Eine besondere Bedeutung kommt in diesem Zusammenhang künftig auch EEG-basierten Messverfahren an tief sedierten oder neuromuskulär blockierten Patienten zu. So lassen sich z. B. Übersedation oder stille epileptische Episoden erkennen und behandeln.
Darüber hinaus kann zur Differenzierung eines Delirs bzw. einer akuten Enzephalopathie eine Diagnostik mittels bettseitigem 1-Kanal-EEG beitragen. Zum Zeitpunkt der Leitlinienerstellung war dieses EEG-basierte Instrument zum Monitoring und zur Diagnose eines Delirs/einer akuten Enzephalopathie noch in der Entwicklung, ist aber mittlerweile validiert und zugelassen. Hierbei spielt die Erkennung sog. polymorpher Deltawellen eine große Rolle [2].
Ungeachtet des technischen Fortschritts sollte jedoch auch weiterhin das bereits erprobte und implementierte Screening mit Delir-, Schmerz- und Sedations-Agitations-Scores regelmäßig – mindestens alle acht Stunden – erfolgen und dokumentiert werden. Auch in Bezug auf Stress, Angst und Schlaf sollte ein regelmäßiges Testverfahren zum Einsatz kommen. Neben apparativen Systemen zum Schlafmonitoring stehen hier auch Selbsteinschätzungsmethoden zur Verfügung.
Sedierung speziellen Indikationen vorbehalten
In der Therapie des Delirs sowie für die Reduktion von Schmerz und Angst stehen nichtpharmakologische Maßnahmen im Fokus. Interessant ist, dass die Leitlinie für die Alpha-2-Agonisten-Gabe daher ein Downgrading empfiehlt – verbunden mit dem Hinweis, die Ursachen zu beheben und primär nichtpharmakologische Ansätze zu nutzen. Diese Empfehlung gilt allerdings nicht für die Therapie eines Delirs. Dazu sollte tatsächlich eine kontinuierliche Alpha-2-Agonisten-Gabe erfolgen. Zusätzlich sind auch hier die Ursachen des Delirs zu suchen und zu beheben.
Neben der großen Bedeutung eines geordneten Tag-Nacht-Rhythmus können reorientierende Maßnahmen wie die Nutzung patienteneigener Hilfsmittel sowie von Datums- und Zeitanzeigen, Frühmobilisation und eine angemessene kognitive Stimulation mittels angepasster Kommunikation wirkungsvoll sein.
Die bisherige Empfehlung für die pharmakologische Schmerztherapie hat sich in der neuen Leitlinie nicht geändert. Die Empfehlung zur Sedierung von Patienten hingegen deutlich. So soll eine Sedierung speziellen, dokumentierten Indikationen vorbehalten sein, die regelmäßig zu überprüfen sind.
Zu den primären Sedierungsindikationen zählen Situationen, die eine Reduktion des Metabolismus bzw. Sauerstoffverbrauchs im Gehirn erfordern, z. B. ein Schädel-Hirn-Trauma (SHT) mit erhöhtem Hirndruck oder ein Status epilepticus.
Weiter sind sekundäre Indikationen mit Situationen verbunden, in denen der generalisierte Metabolismus oder Sauerstoffverbrauch reduziert werden soll (z. B. akutes Lungenversagen – ARDS, Schockzustände), der Patient gefährdet ist, sich weiter zu verletzen (z. B. Immobilisierung im Rahmen von Trauma und operativer Versorgung), oder aufgrund therapeutischer bzw. technischer Maßnahmen eine weitere Verletzungsgefahr besteht (z. B. kinetische Therapie, Bauchlage).
Die Auswahl der Hypnotika ist sowohl von der gewünschten Sedierungstiefe als auch der Steuerbarkeit abhängig. Neben der kontinuierlichen Propofolinfusion bietet sich eine in den vergangenen Jahren zunehmend erprobte inhalative Sedierung mit volatilen Anästhetika an. Verschiedene Metaanalysen deuten auf einen Vorteil inhalativer Sedierungsverfahren für Aufwach- und Extubationszeiten sowie das Auftreten von Übelkeit, Erbrechen und Delir hin.
Eine kontinuierliche Verabreichung von Midazolam, um eine moderate bis tiefe Sedierung aufrechtzuerhalten, hat aufgrund einer Assoziation mit einem schlechteren Outcome und einer längeren Beatmungszeit erwachsener Patienten ohne erhöhten Hirndruck keine Evidenz und Empfehlung mehr.
Eine andauernde Therapie mit Midazolam steht außerdem in Verbindung mit der Entwicklung eines Delirs, von Angstzuständen, Depressionen, kognitiven Dysfunktionen und einer höheren Gefahr für eine PTSD. Daher und aufgrund der schlechten Steuerbarkeit wird Midazolam für eine kontinuierliche Gabe als alleiniges Sedativum in der neuen Leitlinie ausdrücklich nicht mehr empfohlen.
Angehörige eng einbeziehen
Für die Behandlung von Patienten mit einem Delir stehen nichtpharmakologische Maßnahmen im Vordergrund. Neben Maßnahmen, die den Tag-Nacht-Rhythmus fördern, brauchen diese Patienten Möglichkeiten zur (Re-)Orientierung. Insbesondere das Einbeziehen der Angehörigen in ihren Alltag der Intensivbehandlungszeit kann hier eine wichtige Hilfe sein.
Eine medikamentöse Delirtherapie soll nur zusätzlich und gezielt symptomorientiert erfolgen. Die Behandlung produktiver Psychosen soll durch Neuroleptika wie Haloperidol, Risperidon, Olanzapin oder Quetiapin erfolgen. Sowohl bei Agitation als auch bei vegetativer Symptomatik sollen kontinuierlich Alpha-2-Agonisten wie Clonidin oder Dexmedetomidin infundiert werden. Zur Behandlung des Alkoholentzugsdelirs sind langwirksame Benzodiazepine wie Lorazepam oder Diazepam angezeigt.
Für regionale Analgesieverfahren besteht nun die Empfehlung einer täglichen kritischen Indikationsüberprüfung des Schmerzkatheters und dessen zeitnaher Entfernung bei fehlender Indikation.
Der Einsatz von Muskelrelaxantien soll in der Intensivmedizin nur noch in definierten Einzelfällen erfolgen. Hierzu gehören neben der Behandlung von Tetanusverläufen und Shivering während der therapeutischen Hypothermiebehandlung nach Reanimation lediglich kurzzeitige Rescue-Manöver in lebensbedrohlichen Situationen, die mit Hypoxie, Azidose oder hämodynamischem Versagen einhergehen.
Besondere Patientengruppen
Besondere Patientengruppen im Sinne der neuen Leitlinie sind
- schwangere und stillende Mütter,
- sterbende Patienten,
- brandverletzte Patienten,
- polytraumatisierte und Patienten mit erhöhtem Hirndruck,
- kardiochirurgische Patienten und
- Patienten, die extrakorporale Herz- und Lungenersatzverfahren benötigen.
Für die palliative Versorgung Sterbender soll eine Versorgung gemäß der erweiterten S3-Leitlinie „Palliativmedizin für Patienten mit einer nicht heilbaren Krebserkrankung“ [3, 4] erfolgen, die die Bedürfnisse der Angehörigen verstärkt berücksichtigt. Ferner sollen auch diese Patienten eine anxiolytische und analgesierende Therapie nach Bedarf anhand erhobener Scores erhalten.
In der intensivstationären Behandlung Schwangerer bzw. stillender Mütter bestehen keine signifikanten Unterschiede bezüglich den Empfehlungen zur Sedierung, Analgesie und Delirmanagement erwachsener Personen. Hier sollte jedoch Rücksprache z. B. mit Expertinnen und Experten des Pharmakovigilanz- und Beratungszentrums für Embryonaltoxikologie (www.embryotox.de) gehalten werden, welche standardisiert eingesetzten Medikamente u. U. gegen fruchtunschädliche Alternativen auszutauschen sind. Auch kann das Beratungszentrum Hinweise geben, ob ggf. abgepumpte Muttermilch zur Ernährung des Säuglings verwendet werden darf oder ob diese verworfen werden sollte.
Zur Schmerzbehandlung Brandverletzter bei Verbandwechseln und Hauttransplantationen lässt sich nach individueller Indikationsstellung Lidocain lokal auch mittels Infiltration einsetzen. Zudem sieht ein Konsensbeschluss der Expertinnen- und Expertengruppe vor, periphere Regionalanästhesieverfahren fallbezogen einzusetzen.
Die Verwendung von methohexitalbasierten Sedierungsregimes an Patienten mit erhöhtem Hirndruck ist nicht mehr empfohlen. Insgesamt sollte eine Barbiturattherapie nur noch nach individueller Indikationsstellung erfolgen, wenn eine intrakranielle Hypertension sowohl mit alternativen Medikamenten als auch mithilfe chirurgischer Intervention nicht anders beherrschbar ist. Für die Sedierung solcher Patienten stehen weiter midazolambasierte Sedierungsregimes zur Verfügung. Sollte jedoch eine rasche neurologische Beurteilbarkeit gewünscht sein, sollte auch hier eine propofolbasierte Sedierung erfolgen.
Nach wie vor geht die Expertinnen- und Expertengruppe der Leitlinie mit großem Respekt die extrakorporale Ersatztherapie von Herz und/oder Lunge an, da einige zur Anwendung kommende Verfahren Blutdurchflussraten von einigen Litern pro Minute erfordern. Daraus resultiert ein beträchtliches Potenzial für lebensbedrohliche Komplikationen im Fall von Fehlfunktionen oder – im Extremfall – akzidentiellen Dekanülierungen der punktierten Gefäße. Hier steht insbesondere die Frage nach der Therapiesicherheit im Fokus. Vor diesem Hintergrund erfordern solche Verfahren ausreichende Sicherheitsmaßnahmen, die auch den Einsatz von Sedativa an agitierten bzw. deliranten Patienten beinhalten können. Jedoch kommen diese Verfahren zuletzt auch zunehmend an wachen und orientierten Patienten zum Einsatz.
Einige Studien zeigten deutlich reduzierte Intubationsraten und auch erfolgreiche Anwendungen im Bridging vor Lungentransplantationen. In jedem Fall beschreiben die Studien eine frühzeitige und sichere Physiotherapie und Mobilisation, um präventiv der Entwicklung eines Delirs entgegenzuwirken. Unterm Strich sollte die Entscheidung für oder gegen eine Sedierung von Patienten mit einem extrakorporalen Herz-Lungen-Ersatzverfahren hochindividuell geschehen. Für ein in der Therapie erfahrenes Team ist auch Zielscore 0 gemäß der Richmond-Agitations-Sedations-Skala (RASS) möglich.
Auch zur intensivmedizinischen Behandlung von pädiatrischen Patienten gibt es inzwischen zahlreiche Studien, die das protokollbasierte Management von Analgesie, Sedierung und Delir untersucht haben. Ergebnis: Es ist durchführbar, sicher und reduziert das Auftreten von schweren Entzugssymptomen.
Ähnlich wie Erwachsene sollen Kinder, soweit möglich, ihre Schmerzen selbst einschätzen können. Schmerzerfassung in der Neonatologie und Pädiatrie erfolgt unter Berücksichtigung des Entwicklungsalters des Patienten [5]. Die entwicklungsbedingt unterschiedlichen Schmerzkonzepte von Kindern spiegeln sich auch im Schmerzerleben und in der Schmerzäußerung wider. Sollte eine Selbsteinschätzung aufgrund kognitiver Beeinträchtigungen nicht möglich sein, stehen hierfür entwickelte validierte Messinstrumente zur Verfügung (z. B. Individualisierte numerische Bewertungsskala – INRS, Paediatric Pain Profile).
Das Monitoring der Sedierungstiefe Früh- und Neugeborener soll anhand der Neonatal Pain, Agitation and Sedation Scale (N-PASS, Einsatz nach chirurgischen Eingriffen und für beatmete Säuglinge: bewertet Weinen, Reizbarkeit, Verhaltensmuster, Mimik, Extremitätentonus, Vitalzeichen [6]) oder der COMFORTneo Scale [7] erfolgen.
Auch im Kindesalter spielt das Thema Delir eine Rolle, weshalb auch hier ein regelmäßiges Screening auf delirante Symptome unter Zuhilfenahme eines validierten pädiatrischen Delir-Assessments vorzusehen ist.
In der Schmerztherapie ist bei Kindern nach dem Ausschleichen von Opioiden die Entwicklung von Entzugssymptomen möglich, die neben der psychischen Belastung und der Gefahr einer Traumatisierung ebenfalls eine Gefahr für die Entwicklung eines Delirs mit sich bringen. Daher sollte die Gabe von Alpha-2-Agonisten das Ausschleichen einer kontinuierlichen Opioidtherapie unterstützen.
Neben den pharmakologischen schmerztherapeutischen Ansätzen sind nichtpharmakologische Interventionen des Schmerzmanagements eine unverzichtbare Säule der Schmerztherapie. Sie geben sowohl den jungen Patienten als auch deren Eltern wichtige Instrumente an die Hand, um aktiv mit Schmerzen umzugehen. All diese Maßnahmen haben zum Ziel, das Schmerzempfinden zu verringern, die Schmerztoleranzgrenze zu erhöhen und ein adaptives Verhalten des intensivstationär behandelten Kindes zu ermöglichen.
Neben dem Einsatz schmerzpräventiver Pflegekonzepte, z. B. Minimal Handling, Basale Stimulation und Förderung eines normalen Schlafmusters, gehören zur nichtmedikamentösen Therapie auch physikalische Techniken (z. B. Transkutane Elektrische Nervenstimulation – TENS, Kryotherapie) sowie Stressreduktions- und Entspannungsinterventionen (z. B. Atemübungen, Anleitung zu Meditation, Massagen). Umgebungsfaktoren, die im Sinne eines verbesserten Schmerzerlebens veränderbar sind, sind für die Versorgung zu berücksichtigen. So kann auch Ablenkung mittels Musik, Fernsehen, Gesprächen oder Selbstimagination eine wichtige Copingstrategie zur Schmerzbewältigung sein. Selbstverständlich sind auch Kinder altersentsprechend über anstehende Interventionen und zu erwartende Schmerzen aufzuklären, um so lindernd auf Schmerz- und Disstressempfinden des Kindes zu wirken.
Im Fall der Notwendigkeit einer Dauersedierung sollte eine sorgfältige Titration auf die niedrigst mögliche Dosis anhand regelmäßig erhobener Scores erfolgen. Die kontinuierliche intravenöse Applikation von Alpha-2-Agonisten (Clonidin oder Dexmedetomidin) ist zur vegetativen Dämpfung adjuvant oder alternativ zur Sedierung mit Midazolam zu erwägen. Tägliche Sedierungspausen bei Säuglingen und Kleinkindern finden in der neuen Leitlinie keine Berücksichtigung mehr. Dennoch gilt es, eine Übersedierung zu vermeiden.
Die Delirtherapie soll auch an Kindern symptomorientiert zunächst nichtmedikamentös und mit psychosozialen Interventionen erfolgen. Sollte auch eine pharmakologische Therapie notwendig werden, empfiehlt sich der Einsatz von Alpha-2-Agonisten sowie Levomepromazin.
Delir bei älteren Patienten häufig unterschätzt
Der „ältere Patient“ lässt sich nicht eindeutig anhand des kalendarischen Alters definieren. Auch eine feste Altersgrenze, ab wann ein Patient dieser Gruppe zugehörig ist, lässt sich nicht ziehen. Vielmehr ist das klinische Alter eine Zusammensetzung aus biologischem Alter, Komorbidität, Komedikation und externen Einflüssen. Die demografische Entwicklung führt jedoch zu einer immer größer werdenden Zahl alter und hochaltriger Patienten in den Krankenhäusern und auf den Intensivstationen.
Die Deutsche Gesellschaft für Geriatrie (DGG) stellte schon vor vier Jahren fest, dass über 20 Prozent der Intensivpatienten auf internistischen Intensivstationen bereits das 80. Lebensjahr beendet haben. Diese Patientengruppe birgt im Hinblick auf eine veränderte Altersphysiologie, teilweise traumatische Erfahrungen in Kindheit und Jugend und häufig auftretende altersbedingte, physische und psychische Vorerkrankungen eine besondere Herausforderung für das behandelnde Team. Daher fordert die DGG, die Position der Geriaterinnen und Geriater auf den Intensivstationen zu stärken [8].
Nach wie vor kommt es viel zu oft zu problematischen, ärztlich induzierten, akzidentiellen Komazuständen nach Midazolam/Fentanyl-Dauerinfusionen, die es gerade wegen einer deutlich erhöhten Delirinzidenz in dieser Altersgruppe zu vermeiden gilt. Daher soll ein regelmäßiges Screening für ein Delir erfolgen. Insbesondere bei älteren Patienten wird ein Delir häufig unterschätzt. Alter ist ein starker Prädiktor für ein hypoaktives Delir, das mangels Delirmonitoring häufig nicht diagnostiziert wird.
Zur Schmerzerfassung ist an Patienten mit demenziellen Erkrankungen ein für diese Patienten entwickeltes validiertes Schema (z. B. Beurteilung von Schmerzen bei Demenz – BESD) anwendbar.
Häufig bringen Patienten gehobenen Alters bereits eine beträchtliche Anzahl häuslich verordneter Medikamente mit, die eine anticholinerge Wirkung entfalten. Im Rahmen der Delirtherapie älterer Patienten sind diese Medikamente kritisch zu überprüfen und ggf. durch Alternativen zu ersetzen. Eine nichtmedikamentöse Therapie und Prävention eines Delirs ist in jedem Falle vorrangig zu sehen.
Präventiv gibt es jedoch auch Hinweise auf eine verringerte Delirinzidenz und -dauer geriatrischer Patienten, die bei anstehender Hüfttotalendoprothese (TEP) bereits präoperativ mit einer niedrigen Haloperidoldosis behandelt wurden. Neben den nichtpharmakologischen Maßnahmen zur Förderung eines Tag-Nacht-Rhythmus zeigt die Behandlung geriatrischer Patienten mit Melatonin eine positive Entwicklung bezüglich Dauer und Inzidenz eines Delirs. Benzodiazepine sind bei dieser Patientengruppe nur nach strenger Indikationsprüfung und dann auch nur titriert nach Ziel-RASS einzusetzen.
Sedierung von COVID-19-Patienten
Ein umfangreiches Addendum der Leitlinie befasst sich mit der Sedierung von COVID-19-Patienten. So zeigte eine klinische Beobachtung, dass intensiv-stationäres Personal auf eine generelle Sedierung von an COVID-19 erkrankten Patienten verzichtete, da der mediane RASS während der Beatmung bei -4 (-5 bis -3) lag, obwohl auch hier die Vorteile der leichten Sedierung überwiegen. Dabei wurde herausgearbeitet, dass für bestimmte Prozeduren und pflegerische Interventionen eine prozedurale Sedierung bzw. eine kurzzeitig vertiefte Sedierung durchaus notwendig sein können. Dies sollte aber immer unter einer individuellen Nutzen-Risiko-Abwägung erfolgen.
Ökonomie, Implementierung, Qualitätssicherung
Intensivstationen gehören neben den Operationseinheiten zu den kostenintensivsten Abteilungen eines Krankenhauses. Ca. 15 Prozent der Kosten verursacht der Einsatz von Medikamenten. Neben den Anschaffungskosten verursachen Analgetika, Sedativa und Muskelrelaxantien auch indirekte Kosten, die v. a. bei Fehlsteuerung in Form von z. B. einer verlängerten Beatmungsdauer und damit einhergehender Pneumonieinzidenz zu Buche schlagen. Daher ist es Ziel, eine optimale Behandlung zu angemessenen Kosten zu fördern und unnötige oder sogar schädliche Therapiemaßnahmen auszuschließen. Die Sicherheit der Patienten darf jedoch nicht wegen einer unzureichenden Personalsituation gefährdet sein.
Sofern das Intensivpflegepersonal über spezielle und qualifizierte Kenntnisse, Erfahrungen und Fertigkeiten verfügt, kann es die zielorientierte Steuerung von Analgesie und Sedierung nach vorgegebenen Protokollen und ärztlicher Anordnung übernehmen. Dies ist klinikintern über weitere Standardarbeitsanweisungen (Standard Operating Procedures, SOP) oder Verfahrensanweisungen zu regeln. Um hier eine Therapiesicherheit zu erlangen, sind Kliniken dazu angehalten, leitliniengerechte Standards zu Analgesie, Sedierung und Delirtherapie zu entwickeln und zu implementieren. Niedrige Delirinzidenzen können das langfristige Outcome von Intensivpatienten verbessern und deren Lebensqualität über den Heilungsverlauf hinaus erheblich steigern.
Die Änderungen der Leitlinie im Überblick
Zusammenfassend lassen sich die Änderungen in der aktualisierten Leitlinie in folgende Kernpunkte gliedern:
1. Zur Prävention und Behandlung von Delirzuständen und zur Reorientierung ist die Erhebung und Erhaltung der Kommunikationsfähigkeit der Patienten unabdingbar. Intensivstationen sollten mit augmentierenden oder alternativen Kommunikationssystemen ausgestattet werden. Zudem ist das Personal in der Anwendung dieser zu schulen.
2. Eine Sedierung von Patienten ist zielorientiert mit gut steuerbaren Medikamenten vorzusehen. Das Ziel RASS < -2 ist nur noch bei bestimmten Indikationen sinnvoll.
3. Patienten benötigen eine bedarfsgerechte Schmerztherapie. Zur Ermittlung dieses Bedarfs hat ein patientenadaptiertes Schmerzassessment regelmäßig zu erfolgen. Das Personal sollte sensibilisiert werden, Schmerzsymptome zeitnah zu erfassen und zeitnah Gegenmaßnahmen einzuleiten.
4. Ein gezieltes, regelmäßiges und möglichst objektives Monitoring eines Delirs bzw. einer akuten Enzephalopathie sowie des Bewusstseinsgrads und des Schmerzlevels ist für alle Bereiche und Patienten obligat.
[1] Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin (DGAI), Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin (DIVI). S3-Leitlinie Analgesie, Sedierung und Delirmanagement in der Intensivmedizin (DAS-Leitlinie 2020). www.awmf.org uploads/tx_szleitlinien/001–012l_S3_Analgesie-Sedierung-Delir management-in-der-Intensivmedizin-DAS_2021–08.pdf
[2] Hermes C. Bewährte Methode mit neuem Nutzen. PflegenIntensiv 2021; 18 (2): 60–65
[3] Leitlinienprogramm Onkologie. Erweiterte S3-Leitlinie Palliativ-medizin für Patienten mit einer nicht heilbaren Krebserkrankung. www.awmf.org/uploads/tx_szleitlinien/128–001OLl_S3_ Palliativmedizin_2020–09_02.pdf
[4] Montag M, Starbatty B, Thomas M et al. SOP – Behandlung und Betreuung in der Sterbephase. Der Onkologe 2017; 23: 385–388. DOI: 10.1007/s00761–017–0213-y
[5] EKG – Ein Konstruktives Gespräch. Der Podcast für die Fach- und Funktionspflege. Atmungstherapie in der Neonatologie mit Malte Hanelt von 10.09.2021. Im Internet: ekg.letscast.fm
[6] Hummel P et al. Clinical reliability and validity of the N-PASS: neonatal pain, agitation and sedation scale with prolonged pain. J Perinatol 2008; 28 (1): 55–60
[7] Aktuelle Versionen auch zu Delir-Scores z. T. in Deutsch abrufbar unter: www.comfortassessment.nl
[8] Deutsche Gesellschaft für Geriatrie e. V. (DGG). DGG fordert: „Die Position der Geriater auf den Intensivstationen muss stärker wahrgenommen werden!“ (23.03.2017). bit.ly/2Z4y5Hm; Zugriff: 15.10.2021