Ein neues spezielles pflegetherapeutisches Lagerungs- und Maßnahmenbündel gegen Delirien soll dazu beitragen, das Delirmanagement für Intensivpatienten zu verbessern, indem es Symptomkontrolle sowie einen adäquaten Schutz vor negativer Reizüberflutung bietet.
Ein adäquates Delirmanagement auf Intensivstationen stellt eine interprofessionelle Herausforderung und parallel einen Qualitätsindikator dar. Delirien müssen frühzeitig und zügig erkannt sowie evidenzbasiert und strukturiert behandelt werden. Das Behandlungsteam auf der Intensivstation trägt somit eine hohe Verantwortung.
Das durch den Autor entwickelte Fachkonzept Pro-Lira soll dem Behandlungsteam konkrete Entscheidungshilfen aufzeigen und zugleich die Teammitglieder für die Symptomatik des Delirs sensibilisieren. Pro-Lira (lat. „in die Spur“) ist das Gegenwort zu Delir (lat. „aus der Spur“).
Das Pro-Lira-Konzept – „Pro-Lira Position (PLP) & Bündel (PLB) mit dem Anti-Delir-U – in Kombination mit dem ADMOS-Modell“ – stellt ein ganzheitliches multimodales Maßnahmenbündel gegen das Delir dar.
Es definiert eine neue pro-lirante Positionierung, die Halt bietet und eine 360-Grad-Schutzatmosphäre für alle Sinne erzielen möchte, insbesondere für den Tastsinn, um eine negative Reizüberflutung der Patientin oder des Patienten abzuwehren.
Das Konzept orientiert sich an den aktuellen Fassungen der S3-Leitlinie Analgesie, Sedierung und Delirmanagement (DAS-Leitlinie) von 2015 und 2020 [1, 2].
ADMOS-Modell
Gemäß der in der DAS-Leitlinie empfohlenen Medikationsvorgabe entwickelte der Autor das Anti-Delir- Management-Opioid-Sedierungs-Modell (ADMOS-Modell). Dieses sieht ein effektives Management von Schmerz vor. Insbesondere der Schmerz induziert Agitation und/oder ein Delir [11].
Das ADMOS-Modell soll strukturiert und systematisch eine Übersedierung gemäß Richmond Agitation-Sedation Scale (die RASS stellt ein zehnstufiges medizinisches Scoring-System zur Einschätzung des Agitations- oder des Sedierungszustands eines Patienten dar) verhindern sowie eine suffiziente Schmerztherapie gewährleisten. Dabei gilt der Grundsatz „Analgesie first – Sedation second“ (Tab. 1).
Grundsätzlich sollen mit diesem Konzept alle Pflegefachpersonen und Ärzte auf klinischen Intensivstationen, Intermediate-Care-(IMC-)Stationen und in Funktionsabteilungen wie Anästhesie und zentraler Notaufnahme (ZNA) angesprochen werden. Hinsichtlich der Freigabe zur Anwendung der notwendigen Medikamente ist festzuhalten, dass alle Medikamente innerhalb des ADMOS-Modells einer ärztlichen Anordnung bedürfen.
Analgesie first. Die ADMOS-Stufen 1 bis 3 sind primär opioidbasierte Schmerzstufen und -gaben:
- ADMOS 1 bedeutet, dass initial mit 2 mg Morphin Bolusinjektion(en) begonnen werden kann, wenn eine subjektive Schmerzwahrnehmung des Patienten laut VAS (visueller Analogskala) oder NRS (numerische Ratingskala) von 3–5 oder ein BPS-/BPS-NI-Wert (Behavior Pain Scale, Skala zur Beurteilung des Schmerzgrades bei Patienten, die nicht verbal kommunizieren können und BPS-NI für nichtbeatmete intensivmedizinische Patienten) von 3–6 besteht.
- ADMOS 2 wäre indiziert, wenn NRS/VAS von > 5–6 oder BPS/BPS-NI von > 6 vorherrscht; hier sollte mit Bolusgaben via 3,75 mg Piritramid (Dipidolor®) zügig interveniert werden.
- ADMOS 3 stellt mit NRS/VAS von > 7 oder BPS/BPS-NI von > 7 die erste Endstufe in der Kategorie: „Analgesie first“ dar. Ein Sufenta-Perfusor als Applikationsform ist umgehend zu installieren – dies zu Beginn mit einer Startdosis von 5 μg/h. Bedarfsgerechte Bolusgaben von 5 μg sind im Verlauf gerechtfertigt.
Wichtig zu wissen: Das ADMOS-Modell sollte nur auf Grundlage der integrierten Schmerz-Scores (NRS-V, BPS-NI) angewendet werden.
Nach Schmerzmittelgabe sollte die Evaluation mithilfe der Schmerz-Scores dokumentiert werden. Eine Übersedierung RASS –2 oder tiefer sollte vermieden werden.
Sedation second. Primär sollten frühzeitig adjuvante Alpha-2-Rezeptor-Agonisten wie Clonidin > 0,06 mg/h bis maximal 0,15 mg/h oder Dexmedetomidin > 0,2 – 1,4 µg/kgKG/h als Sedierung verwendet werden. Die Zielstufe ADMOS 1–2/α2 wird eingeleitet.
Lassen sich schwerste manifest hyperaktiv-delirante Zustände (RASS 4, Fremd- und/oder Eigengefährdung) noch immer nicht unter Kontrolle bringen, stellt dies die Indikation für die finale Endstufe ADMOS 1–3/α2 Pro-Dex/Mi-Dex dar.
Es können unter Dexdor-Gabe niedrig dosierte Propofol-Boli (30–50 mg) oder Midazolam-Boli (2,5 mg gegebenenfalls höher – insbesondere bei C2-Abusus) gezielt verabreicht werden, um möglichst wieder eine Ziel-RASS von 0/-1 zu erreichen.
Anschließend ist die Wirkung engmaschig zu evaluieren. Sollten alle Bolusgaben nicht ausreichend zu einem RASS-Niveau –2/–3 führen, stellt dies die kurzzeitige Indikation für einen niedrig dosierten Propofol- oder Midazolam-Perfusor dar.
Die Anwendung muss unter einem kontinuierlichen Monitoring sowie einer kontinuierlichen Sauerstoffgabe erfolgen. Zur Sicherheit sollten eine Zwei-/Vier-Punkt-Fixierung vorgenommen und/oder Bettgitter unter hochfrequenter Kontrolle eingesetzt werden (richterliche FEM-Dokumentation – freiheitsentziehende Maßnahmen – beachten). Der Grundsatz: „Analgesie first – Sedation second“ kann bei C2- Patienten oder nichtverletzten Patienten umgekehrt werden: „Sedation first“. Mobilisation und Defixierung müssen im Verlauf geplant und individuell umgesetzt werden.
Wichtig zu wissen: An dieser Stelle sollte die gesamte Pro-Lira-Philosophie initialisiert werden. Meist befinden sich delirante Patienten in einem akuten Diskomfort. Das sogenannte 360-Grad-Anti-Diskomfort-Management, das in ein 360-Grad-High-Komfort überführt werden kann, wird später vorgestellt.
Sedierung. Früher galt der inzwischen überholte Grundsatz: je mehr Sedierung, desto schonender für den intubierten Patienten. Heutzutage ist eine der wichtigsten präventiven Strategien eines Anti-Delir-Managements die Vermeidung einer zu tiefen Sedierung. Zahlreiche Studien konnten zeigen, dass eine medizinisch nicht indizierte Übersedierung intensivpflichtiger Patienten (RASS ≤ –2) nicht nur mit einer erhöhten Delirinzidenz verbunden war, sondern auch mit verlängerter Beatmungsdauer, intensivmedizinischer Behandlungs- und Krankenhausverweildauer sowie höherer Mortalität. Eine Ziel- und Score-basierte Sedierungsstrategie mit einer Ziel-RASS von 0 bis –1 verbessert die kognitive und kommunikative Funktion, verkürzt die Beatmungsdauer, ermöglicht eine frühe Mobilisierung sowie ein zuverlässiges Delirscreening und führt zur Reduktion von Delirinzidenz, -schwere und -dauer [3].
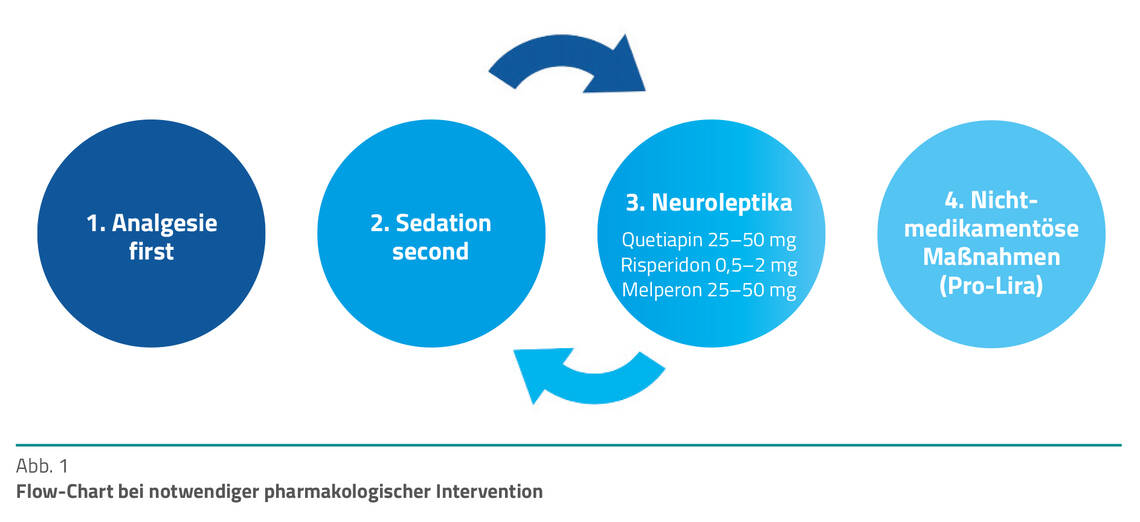
Wichtig zu wissen: Wenn sich das therapeutische Team tief im pharmakologischen Teil der Delirtherapie befindet, weil der Delirpatient nicht zugänglich ist und/oder sich aggressiv präsentiert, kann es passieren, dass die nichtmedikamentösen Maßnahmen außer Acht gelassen werden. Das Pro-Lira-Flow-Chart soll bei notwendiger pharmakologischer Intervention insofern unterstützen, als an diese sensitiven nicht-medikamentösen Maßnahmen erinnert wird (Abb. 1).
Sedierungspausen. Einmal pro Schicht Sedierungspausen, gegebenenfalls -reduktion bedarfsadaptiert erwägen und/oder planen. Zielstufe ADMOS 1–2/α2 wieder nach Symptomkontrolle in Betracht ziehen.
Neuroleptika. Atypische Neuroleptika/Antipsychotika wie Quetiapin und Melperon oder Risperidon und Melperon sollten primär kombiniert werden. Die Verordnung sollte abends oder nachts erfolgen, zum Beispiel Quetiapin 25–50 mg sowie Melperon 25–50 mg (0–0–1–2) oder Risperidon 0,5–2 mg sowie Melperon 25–50 mg. Beide Kombinationen sollten vor Haloperidol intravenös (i.v.) bevorzugt werden.
Haldol. Haloperidol ist ein klassisches hochpotentes Neuroleptikum mit sehr gutem anti-psychotischen Effekt. Für ältere Patienten sollte eine niedrige Einzeldosierung, zum Beispiel 0,5 bis 1 mg i.v. begonnen werden. Zu hinterfragen ist ein starres Dosierungsintervall von dreimal 2,5 mg Haloperidol/Tag. In einer multizentrischen, randomisierten verblindeten und placebokontrollierten Studie mit 1.000 Patienten aus 16 Intensivstationen in Dänemark, Finnland, Großbritannien, Italien und Spanien zeigte sich, dass der Einsatz von Haloperidol bei intensivmedizinisch behandelten Patienten mit Delir im Allgemeinen die Delirdauer und das delirfreie Überleben nicht überzeugend beeinflusst [10].
Pro-Lira-Position
Bisher existieren in der medizinischen Fachliteratur nur wenig bis keine anti-delirante Lagerungsformen, die ein Delirium erfolgreich begleiten und/oder supportiv behandeln können. Der Autor hat dazu die sogenannte Pro-Lira-Position (PLP) mit einem „Anti-Delir-U“ entwickelt. Die speziell gewählte Lagerungsform, die mit Basaler Stimulation arbeitet, soll allen Delirformen gerecht werden. Sie sieht eine Lagerung des Patienten in Rückenlage, mit einer 30-Grad-Oberkörperhochlagerung sowie Spitzfußlagerung mit leicht angehobenem Fußteil vor. Der Oberkörper ist von dem Anti-Delir-U umfasst (Aufmacherbild). Die PLP kann ebenfalls bei einer Vier-Punkt-Fixierung unter engmaschiger Kontrolle angewandt werden.
Die Pro-Lira-Philosophie wurde aus den Grundsätzen der Basalen Stimulation erarbeitet. Die Basale Stimulation versteht sich als Ansatz, grundlegende Wahrnehmungen anzuregen, wenn im Rahmen einer Erkrankung oder Behinderung die Kommunikation mit der Umwelt eingeschränkt ist. Die Basale Stimulation ist eine Form ganzheitlicher, körperbezogener Kommunikation für Menschen mit wesentlichen Einschränkungen. Mit einfachen und grundlegenden Angeboten helfen Pflegende, die Kompetenzen beeinträchtigter Menschen zu erhalten, zu sichern und aufzubauen [8].
Damit die PLP adäquat wirken kann, sollten vier Grundvoraussetzungen erfüllt sein:
- Ziel-RASS 0/-1,
- effektive Schmerztherapie,
- angenehme Atmosphäre,
- alle Grundbedürfnisse des Patienten werden erfüllt.
Die leitliniengerechte Therapie, das Scoring sowie das Assessment eines Delirs stellen die Grundlage allen Handelns dar. Ohne diese Grundlage verliert die Pro-Lira-Position mit dem Anti-Delir-U und den zwei Pro-Lira-Phasen innerhalb des Pro-Lira-Bündels für alle Sinne ihre Wirkung.
Pro-Lira-Phasen
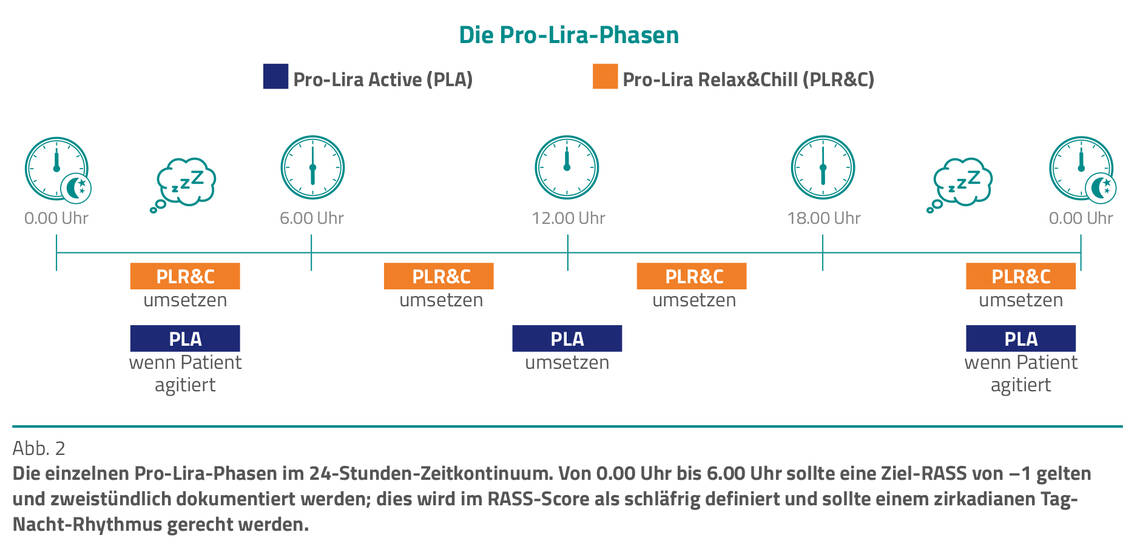
Delirante sowie delirgefährdete Patienten werden in zwei definierte Pro-Lira-Phasen – Phase der Aktivität (Active = PLA) und Phase der Ruhe (Relax&Chill = PLR&C) – strukturiert sowie im Wechsel mehrfach am Tag im therapeutischen Team multiprofessionell mobilisiert und positioniert. Die Phasen PLA und PLR&C sollten mehrmals im Wechsel in 24 Stunden über mehrere Tage im Team umgesetzt werden (Tab. 2).
Insbesondere zwischen 0.00 Uhr und 6.00 Uhr sollten Delirpatienten schlafen (PLR&C). Sollte der Patient es wünschen oder so stark agitiert sein, dass ein einzuleitender Schlafrhythmus in PLR&C nicht möglich ist, sollte er an die Bettkante mobilisiert werden (PLA). Ansonsten sollte mit PLA erst nach 6.00 Uhr begonnen werden (Abb. 2). Erste Erfahrungen zeigen, dass die Pro-Lira-Position (PLP) bei Intensivpatienten mit Delir ein mittleres fixierungsfreies Ruheintervall von 30 Minuten im Minimum und bis zu drei Stunden im Maximum erreicht – je nach Delirform länger oder kürzer.
Nach einer oft anstrengenden Mobilisation an die Bettkante oder in den Stand freuen sich die Intensivpatienten in der Regel auf die Pro-Lira-Position, um offensichtlich körperlich unterstützt zu entspannen. Nicht selten verlangten auch COPD-Patienten nach der PLP aufgrund der atemunterstützenden Positionierung.
Von Anti-Diskomfort zu High-Komfort
Das Anti-Diskomfort-Management ist aufgrund seiner Ansätze zur Vermeidung von Stressoren und der Behandlung akuter Symptome auf der beschriebenen Intensivstation das bevorzugte Verfahren zur Behandlung von Delirien.
Das umgesetzte Konzept des 360-Grad-High-Komfort-Managements (Textkasten) integriert verschiedene Ansätze, um sowohl die physischen als auch die psychischen Bedürfnisse der Patienten zu berücksichtigen, und konzentriert sich primär auf die Schaffung eines multimodal komfortablen Umfelds und angenehmer sensitiver Erlebnisse für den Patienten. Pro-Lira stellt ein strukturiertes klinisches 360-Grad-Anti-Diskomfort-Management (Textkasten) dar, das parallel eine hohe Symptomkontrolle sowie einen adäquaten Schutz vor negativer Reizüberflutung bietet und in ein hohes Niveau von 360-Grad-High-Komfort(-Management) aller Sinne mündet.
PAD- und Pro-Lira-Management
Schmerz ist Faktor Nummer 1 des Delirs. Mit der validierten Erfassung von Schmerz (Pain), Agitation und Delir beschäftigt sich das PAD-Management. Schmerzen, Agitation und Delir sind keine isolierten Herausforderungen und die Themenkomplexe müssen zwingend zusammen gedacht und gelöst werden [11]. Das Pro-Lira-Management ist erfüllt, wenn
- alle zwei Stunden
- RASS konsequent bei 0/–1 erreicht und dokumentiert wird,
- VAS oder NRS bei ≤ 3 liegen; diese Werte sind alle zwei Stunden abzufragen und zu dokumentieren,
- BPS/BPS-NI bei ≤ 3 liegt; dieser Wert ist alle zwei Stunden zu erheben und zu dokumentieren.
- einmal pro Schicht die CAM-ICU (Confusion Assessment Method for Intensive Care) oder das standardisierte Verfahren ICDSC (Intensive Care Delirium Screening Checklist) erhoben und dokumentiert wird, um das standardisierte Verfahren ICDSC oder die CAM-ICU zwingend umzusetzen.
Dabei gilt:
- Das Ziel-RASS 0/–1 gilt bei allen intensivstationären Patienten – sofern keine andere Indikation vorliegt, wie etwa die Notwendigkeit eines Ziel-RASS –5 im Rahmen einer Bauchlage.
- Patienten-Schmerz-Selbsteinschätzung geht vor Fremdeinschätzung, soweit dies möglich ist. Die behandelnde Pflegefachperson sollte nach Bedarfsmedikation eigenständige Opiat-Bolusgaben i.v. oder via patientenkontrollierter Analgesie (PCA) verabreichen. Bei schwersten Schmerzsituationen sollten die Kolleginnen und Kollegen der Anästhesie einen Periduralkatheter mit PCA-Funktion installieren. So können eventuell Opiate und andere i.v.-Medikamente eingespart werden.
- Analgesie first – Sedation second.
- Sollte bei einer diagnostischen Untersuchung, zum Beispiel einer Bronchoskopie/Gastroskopie oder einer kurzzeitigen medizinischen Intervention (Kardioversion), eine RASS-Vertiefung notwendig sein, gilt anschließend umgehend wieder eine Ziel-RASS von 0/–1.
- Wichtig: Propofol ist nach Intervention zügig auszuschleichen oder die Gabe zu pausieren.
- Wichtig: i.v. Benzodiazepine bei > 65-Jährigen sind hochgradig delirogen! Alkoholkranke (C2-)Patienten sollen vor allem im Delirum Tremens i.v. Benzodiazepine erhalten.
- Adäquates Handeln via Checklisten und validierter Scoring-Systeme ist gemäß DAS-Leitlinie unverzichtbar [1, 2].
Neue Impulse
In einer vom Autor initiierten Umfrage mit 60 Teilnehmenden bezeichneten 54 Prozent der befragten Pflegefachpersonen, Ärztinnen und Ärzte sowie Physiotherapeutinnen und -therapeuten das Delirmanagement als anstrengend, 34 Prozent als sehr anstrengend. 66 Prozent gaben sogar an, gelegentlich bei der Versorgung von Patienten mit schwerem Delir zu verzweifeln. Nicht selten werde zwar die Mobilisation im Tagesziel interprofessionell festgelegt, könnte jedoch bei hohen Arbeitsspitzen oder in Notfällen entfallen. Die Physiotherapie sei eine wertvolle zusätzliche Ressource zur Mobilisation und der anschließenden selbstständigen Pro-Lira-Positionierung der Intensivpatienten. Pflegefachpersonen haben hier die Führungsrolle eingenommen.
Pro-Lira gibt dem Behandlungsteam neue Impulse für die Behandlung von Patienten mit Delir auf der Intensivstation. Derzeit existieren keine Medikamente, um ein Delir kausal aufzulösen. So lange die Ursachen eines Delirs nicht erkannt und/oder behandelt werden, so lange wird auch das komplexe Syndrombild eines Delirs fortbestehen.
Anti-Diskomfort in High-Komfort überführen
- 360-Grad-Anti-Diskomfort-Management
- Alle Grundbedürfnisse sind multimodal nicht erfüllt.
- Definition: Unsichere, negative Atmosphäre oder Patienten fühlen sich in alle Richtungen mehrfach nicht wohl/ komfortabel; haben zum Beispiel oft Schmerzen, Angst oder Atemnot, sind agitiert oder aggressiv (RASS 1 bis 4) oder übersediert (RASS –2 bis –4), fühlen sich gestresst oder (massiven) Stressoren wie Lärm, Durst, Hunger, Übelkeit, Belästigungen und/oder Temperaturschwankungen ausgesetzt, schlechtes Blasen-/Darmmanagement, kein Schlaf, kein strukturierter Tag-Nacht-Rhythmus, kein Kontakt zu Angehörigen, niedrige Patientenautonomie oder -mobilität, werden desintegriert/entmündigt, erleben Habituation oder viele negative Sinneseindrücke oder eine Reizdeprivation, keine Basale Stimulation oder Kinästhetik, Brille/Hörgeräte/Hilfsmittel fehlen unter Umständen, „Save Tubes und Lines“ ausstehend (Zu- und Ableitungen sind nicht gesichert), autoritäre Bezugspersonen, kein Verständnis für die Bedürfnisse des Patienten.
- Anti-Diskomfort-Management kennzeichnet einen 360-Grad-Rundumblick gegen einen mehrdimensionalen Diskomfort aller Sinne auf der Intensivstation.
- Es wird proaktiv etwas gegen die genannten Stressoren unternommen.
360-Grad-High-Komfort-Management
- Alle Grundbedürfnisse sind multimodal erfüllt.
- Definition: Sichere, positive Atmosphäre oder Patienten fühlen sich in alle Richtungen mehrfach wohl/ komfortabel; haben zum Beispiel nur wenig bis keine Schmerzen, Angst oder Atemnot, sind nicht agitiert oder aggressiv oder übersediert (Ziel-RASS 0 bis –1), fühlen sich nicht gestresst oder (massiven) Stressoren wie Lärm, Durst, Hunger, Übelkeit und/oder Belästigungen ausgesetzt, erleben Normothermie, erfolgreiches Blasen-/Darmmanagement, mindestens vier Stunden Schlaf zwischen 0.00 Uhr und 6.00 Uhr, strukturierter Tag-Nacht-Rhythmus, viele Kontakte zu Angehörigen, hohe Patientenautonomie oder -mobilität, werden integriert, sind mündig, erleben viele positive Sinneseindrücke durch Basale Stimulation oder Kinästhetik, Brille/Hörgeräte/Hilfsmittel sind ausgehändigt, „Tubes and Lines are save, daily evaluated or removed“ (Zu- und Ableitungen gesichert, täglich evaluiert gegebenenfalls entfernt), vertrauensvolle Bezugspersonen, Verständnis für die Bedürfnisse des Patienten.
- High-Komfort-Management kennzeichnet einen 360-Grad-Zustand für maximalen mehrdimensionalen Komfort aller Sinne auf der Intensivstation.
- Lässt Diskomfort proaktiv nicht aufkommen.
Das Pro-Lira-Konzept vereinheitlicht das Delirvorgehen, sodass es nun nicht mehr primär von Belang ist, welche Delirform aktuell vorherrscht, ob der Patient ein Prädelir entwickelt, im Delir ist oder sich bereits in einem schweren/manifesten Delir befindet (postoperativ, C2-bedingt, bei Demenz, ein hyper- oder hypoaktives Delir oder eine Mischform aus beidem). Mithilfe des ADMOS-Modells existiert nun eine schnelle und übersichtliche Delir-SOS-Systematik, die eine klare und delirgerechte rein pharmakologische Anwendung sicherstellt.
Nach Ansicht des Autors wurde bisher noch keine delirspezifische Lagerung in Kombination mit einer einheitlichen delirkomplementären Vorgehensweise definiert. Die Wirkungsweise der PLP&B via Anti-Delir-U sowie den zwei sensitiven Pro-Lira-Phasen Active und Relax&Chill, insbesondere die medikamentöse und bedarfsgerechte Handhabung des ADMOS-Modells, wurden auf Grundlage der eigenen praxiserprobten Erfahrung des Autors entwickelt. All diese Maßnahmen müssten konsekutiv evidenzbasiert kontrolliert und im Kontext einer Studie erforscht werden.
[1] Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e. V. (AWMF) S3-Leitlinie Analgesie, Sedierung und Delirmanagement in der Intensivmedizin (DAS-Leitlinie), Fassung von 2015. Im Internet nicht mehr abrufbar.
[2] AWMF. S3-Leitlinie Analgesie, Sedierung und Delirmanagement in der Intensivmedizin (DAS-Leitlinie), Fassung von 2020. Im Internet: www. awmf.org/uploads/tx_szleitlinien/001-012l_S3_Analgesie-Sedierung-Delirmanagement-in-der-Intensivmedizin-DAS_2021-08.pdf
[3] Braune S, Gurlit S. Management des Delirs auf der Intensivstation. In: DMW 2017; 142 (24): 1820–1824
[4] AWMF. S1-Leitlinie Delir und Verwirrtheitszustände inklusive Alkoholentzugsdelir. Fassung von 2020. Im Internet: register.awmf.org assets/guidelines/030-006l-S1_Delir-und-Verwirrtheitszustaende-Alkoholentzugsdelir_2022-01.pdf
[5] Nydahl P, Hermes C, Dewes M. Leitlinie PADIS – Teil 1–3. PflegenIntensiv 2019: 16 (1) 5–20
[6] Larsen R. Anästhesie und Intensivmedizin für die Fachpflege. 8., vollst. Überarb. Aufl. Berlin: Springer; 2012: 155, 654
[7] Schneider D, Richling F (Hrsg.). Datenbank Arzneimittel. Stuttgart: Thieme eRef (2020, 2021)
[8] Pschyrembel. WHO-Stufenschema. Im Internet: www.pschyrembel.de/WHO-Stufenschema/K0PQ7
[9] Knels C, Grün H. Basale Stimulation. In: Knels C (Hrsg.). Sprache und Ernährung bei Demenz. 1. Aufl. Stuttgart: Thieme; 2018
[10] Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin e.V. (DIVI). Haloperidol for the Treatment of Delirium in ICU Patients. Gemeinschaftsartikel. Deutscher Ärzteverlag 2/2023; 14 (2): 132–133, auf Grundlage von Andersen-Ranberg et al. N Engl J Med 2022; 387: 2425–2435
[11] Orion-Pharma (2018), mod. nach Reade MC. Sedation and Delirium in the Intensive Care Unit. NEJM 2014; 370: 1567