Posttraumatische Blutungen sind nach wie vor eine der Haupttodesursachen verletzter Patienten. Bei der Versorgung der Betroffenen stellen Gerinnungsstörungen eine besondere Herausforderung dar. Aussagen zur richtigen Behandlung macht eine neue Leitlinie.
Das Verständnis der Pathophysiologie der posttraumatischen Koagulopathie hat zugenommen und zu verbesserten Behandlungsstrategien geführt. Heute ist bekannt, dass eine frühzeitige, individualisierte, zielgerichtete Behandlung das Outcome schwerverletzter Patienten verbessert.
Die zum fünften Mal aktualisierte Leitlinie (LL) „The European guideline on management of major bleeding and coagulopathy following trauma“ (dt. „Europäische Leitlinie zum Management von Blutung und Koagulopathie nach Trauma“) ist im März 2019 in der Fachzeitschrift „Critical Care“ erschienen. Die LL hat einen Umfang von 74 Seiten und kann auf der Website von „Critical Care“ kostenlos heruntergeladen werden [1].
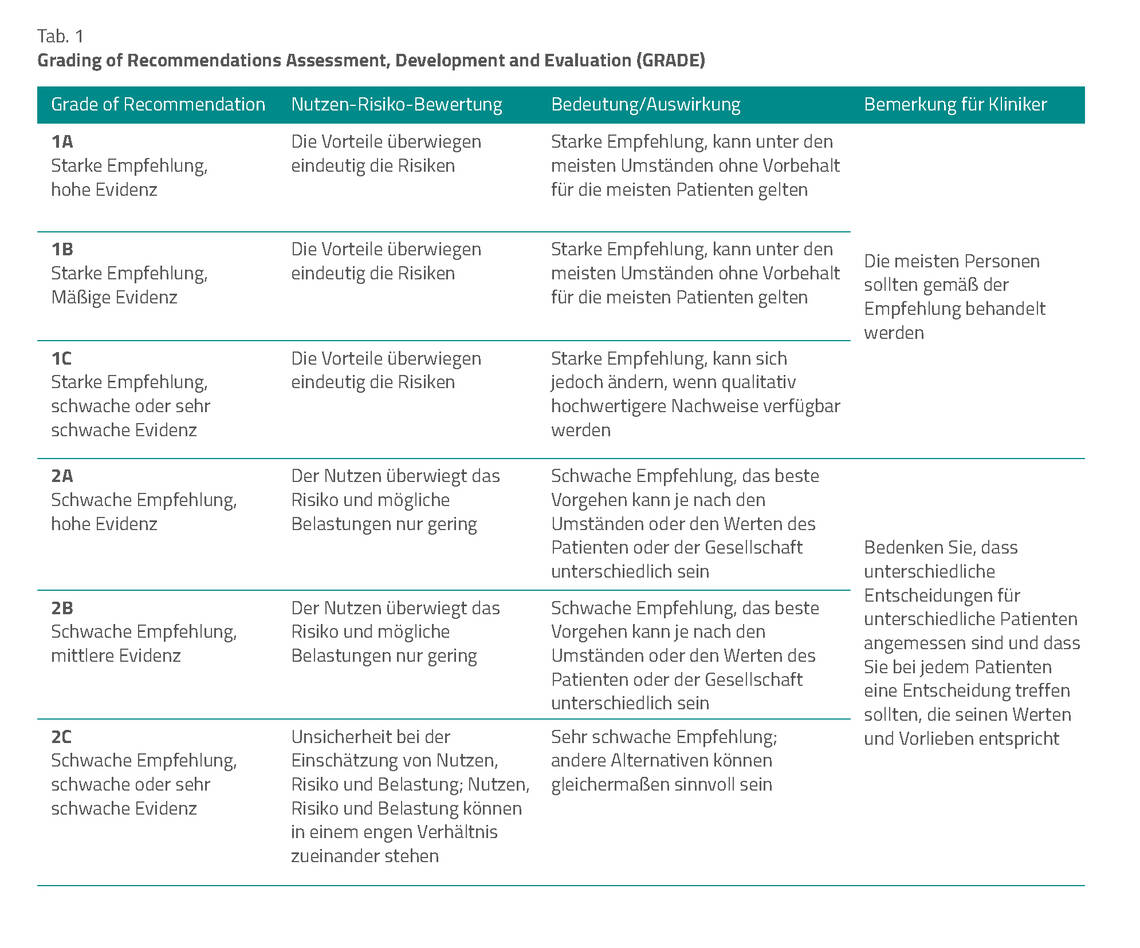
Die Empfehlungen wurden hinsichtlich ihrer Evidenz bewertet und entsprechend eingestuft. Die Einteilung in die Evidenzstufen 1A, 1B, 1C, 2A, 2B und 2C erfolgte nach dem sog. GRADE-System (Grading of Recommendations Assessment, Development and Evaluation, Tab. 1) [2]. Die Empfehlungen der LL sind in verschiedene Abschnitte untergliedert. Dieser Beitrag fokussiert auf einige innerklinisch interessante Empfehlungen oder Schnittstellenbereiche.
Initiale Rettungsmaßnahmen und Prävention weiterer Blutungen
Die Autoren empfehlen die Vermeidung einer Hypoxämie (Grade 1A) sowie die Normoventilation von Traumapatienten (Grade 1B).
Begründung: Die negativen Auswirkungen einer Hypoxämie sind bekannt, insbesondere bei Patienten mit Schädel-Hirn-Trauma (SHT). Daher werden bei der initialen Versorgung dieser Patienten i. d. R. hohe Sauerstoffkonzentrationen angestrebt, um die Sauerstoffabgabe an ischämische Bereiche sicherzustellen. Es gibt jedoch Hinweise darauf, dass eine anhaltende Hyperoxie mit einer erhöhten Mortalität verbunden ist [3, 4]. So zeigte kürzlich eine Studie, dass die Mortalität mit der Dauer und dem Ausmaß der Hyperoxie korreliert [5] und dass eine maschinelle Beatmung mit Einstellungen, die eine Sauerstoffsättigung von 88–92 % im Vergleich zu höher als 95 % anstrebten, das Überleben nicht negativ beeinflusste [6]. Die negativen Auswirkungen von Hyperoxie stehen wahrscheinlich in Zusammenhang mit einer veränderten Mikrozirkulation in Verbindung mit hohem PaO2 und einer erhöhten Produktion freier Radikale [7] – und Patienten mit schweren Hirnverletzungen können einem besonderen Risiko ausgesetzt sein. Obwohl eine Hyperoxie bei einem extrem anämischen Traumapatienten den Sauerstoffgehalt und die Sauerstoffabgabe ans Gewebe erhöhen und daher in dieser speziellen Situation vorteilhaft sein kann, sollte die Hyperoxie auf Normoxie zurückgeführt werden, sobald der Hämoglobingehalt (Hb) dies zulässt [8].
Diagnostik und Monitoring einer Blutung
Erste Einschätzung. Die LL empfiehlt eine klinische Beurteilung des Patienten durch den Arzt oder die Ärztin (im Folgenden: Arzt), um das Blutungsausmaß einzuschätzen. Dazu sei eine Kombination der physiologischen Parameter, der anatomischen Verletzungszeichen, des Verletzungsmechanismus und der Patientenreaktion auf die bislang erfolgte Therapie zu nutzen (Grade 1C). Begründung: Der behandelnde Arzt in der Notaufnahme bzw. im Schockraum muss den Patienten zügig einschätzen und entscheiden, ob ein spezielles Behandlungsprotokoll (Massivtransfusion etc.) erforderlich ist. Dies schließt die erforderliche Logistik ein. Obwohl ein Blutverlust manchmal offensichtlich sein kann, sind weder eine visuelle Abschätzung noch physiologische Parameter zuverlässige Anhaltspunkte zur Abschätzung der Blutungsschwere [9]. Die Kenntnis des Verletzungsmechanismus liefert nützliche Informationen, um Patienten, bei denen ein erhebliches Blutungsrisiko besteht, frühzeitig zu identifizieren. So hat z. B. das „American College of Surgeons“ sechs Meter als „kritische Fallhöhe“ im Zusammenhang mit schweren Verletzungen, einschließlich Blutungen, definiert [10]. Bildgebung. Die LL empfiehlt, das Assessmentinstrument FAST (Focused Assessment with Sonography in Trauma) zu nutzen, um freie Flüssigkeit im Rumpf zu erkennen (Grade 1C). Zudem sei die frühe Bildgebung mittels Ganzkörper-Computertomografie (CT) mit Kontrastmittel zu empfehlen, um Verletzungen und potenzielle Blutungsquellen zu erkennen (Grade 1B). Begründung: Die FAST-Untersuchung hat sich zu einem Schlüsselinstrument bei der akuten Beurteilung von Traumapatienten mit Verdacht auf abdominale und thorakoabdominelle Verletzungen entwickelt [11]. FAST-Techniken werden mit verkürzten Untersuchungszeiten und einer gezielten Beurteilung spezifischer klinischer Probleme eingesetzt [12]. Als schneller und nichtinvasiver diagnostischer Ansatz zur Erkennung von Blutungen in der Peritoneal-, Pleura- und Perikardhöhle ist FAST ein Eckpfeiler der initialen Diagnostik im Schockraum. Die Vorteile des mehrzeiligen Ganzkörper-Spiral-CT bei schwerverletzten Patienten in Bezug auf Zeitersparnis, diagnostische Genauigkeit und potenzielles Überleben sind vielfach dokumentiert [13, 14]. Die Integration moderner mehrzeiliger Spiral-CT in die Notaufnahme ermöglicht die sofortige Beurteilung aller Traumapatienten, wodurch eine rechtzeitige Diagnose, die Unterscheidung zwischen verschiedenen Arten schwerer Gefäßverletzungen und die Identifizierung der damit verbundenen Befunde ermöglicht wird. Hämoglobin (Hb). Die LL empfiehlt, einen niedrigen Hb-Wert als Marker für eine schwere Blutung mit assoziierter Koagulopathie heranzuziehen (Grade 1B). Es seien wiederholte Hb-Bestimmungen als laborchemischer Marker für eine Blutung zu nutzen, da ein initial innerhalb des Normbereichs liegender Hb-Wert eine Blutung maskieren könne (Grade 1B). Begründung: Der diagnostische Wert von Hb oder Hkt (Hämatokrit) für die Erkennung von Traumapatienten mit schweren Verletzungen und okkulten Blutungsquellen ist Gegenstand vieler Diskussionen gewesen. Eine wesentliche Einschränkung des diagnostischen Werts von Hb/Hkt ist der störende Einfluss von Behandlungsmaßnahmen wie intravenösen Infusionen und Erythrozytenkonzentraten. Darüber hinaus spiegeln anfängliche Hb- oder Hkt-Messungen möglicherweise den Blutverlust nicht genau wider, da Patienten „Vollblut“ verlieren und Kompensationsmechanismen etwas Zeit benötigen. Dennoch wurde die Annahme, dass initial gemessene Hb/Hkt-Werte zum Nachweis schwerer Blutungen eine geringe Aussagekraft besitzen, infrage gestellt. Knottenbelt et al. untersuchten 1.000 Traumapatienten und fanden einen niedrigeren initialen Hb-Wert bei Patienten mit mittlerem und schwerem Schock [15]. Holstein et al. zeigten, dass ein Hb-Wert unter 80 g/l bei Patienten mit Beckentrauma mit einem Nichtüberleben assoziiert war [16]. Serum-Laktat und Basendefizit. Die LL empfiehlt, das Serum-Laktat und/oder das Basendefizit als sensitive Tests und zum Monitoring für Blutung und Schock zu nutzen (Grade 1B). Begründung: Das Serum-Laktat wird seit den 1960er-Jahren als diagnostischer Parameter und prognostischer Marker für den hämorrhagischen Schock genutzt. Das durch anaerobe Glykolyse produzierte Laktat ist ein indirekter Marker für den Sauerstoffmangel, die Gewebehypoperfusion und die Schwere des hämorrhagischen Schocks [17]. Vergleichbar damit bieten die Basendefizit-Werte aus der arteriellen Blutgasanalyse eine indirekte Abschätzung der globalen Gewebeazidose aufgrund einer beeinträchtigten Perfusion [18].Gewebeoxygenierung, Volumenersatz, Temperatur
Die LL empfiehlt bei Patienten ohne Hirnverletzungen die permissive Hypotension mit einem systolischen Zielblutdruck von 80–90 mmHg (mittlerer arterieller Druck = MAP 50–60 mmHg), bis starke Blutungen gestoppt wurden (Grade 1C). Bei Patienten mit schwerem Schädel-Hirn-Trauma (GCS ≤ 8) wird empfohlen, einen MAP ≥ 80 mmHg aufrechtzuerhalten (Grade 1C). Die Autoren sprechen sich für eine restriktive Volumentherapie aus, um den Zielblutdruck zu erreichen, bis Blutungen kontrolliert werden können (Grade 1B). Beim Vorliegen einer lebensbedrohlichen Hypotension wird empfohlen, ergänzend zur Volumentherapie Vasopressoren bis zum Erreichen des arteriellen Zielblutdrucks einzusetzen (Grade 1C). Begründung: Bei schwerverletzten Patienten hat sich seit vielen Jahren das Konzept der „Damage Control Surgery“ (DCS) durchgesetzt. Darunter wird ein dreistufiges Konzept verstanden: chirurgische Blutstillung, Intensivtherapie, definitive chirurgische Versorgung. In der ersten Behandlungsphase beschränkt man sich auf lebensrettende Eingriffe, um durch kurze OP-Verweildauer das zusätzliche operationsbedingte Trauma zu minimieren. Danach folgt die Phase der Intensivtherapie. Ziel ist, den Kreislauf, die Gerinnung und die Stoffwechselsituation zu stabilisieren, Normothermie zu erhalten oder wiederherzustellen und die Beatmung zu optimieren. Erst danach erfolgt, unter Umständen Tage später, die definitive chirurgische Versorgung. Zu diesem Konzept gehört gegenwärtig auch die permissive Hypotension. Wichtig zu wissen: Die sog. permissive Hypotension beschreibt zwei Ansätze:- erstens einen niedrigeren als den normalen Blutdruck zu tolerieren, um so die Thrombusbildung zu unterstuützen,
- zweitens zur Verhinderung einer iatrogenen Verdünnung nur wenig Infusionslösung zu infundieren, während dennoch eine akzeptable Durchblutung der Endorgane gewährleistet wird.
Zusammenfassung
Traumapatienten sind möglichst in einem spezialisierten Zentrum zu behandeln. Maßnahmen zur Überwachung und Unterstützung der Gerinnung sind so früh wie möglich einzuleiten. Die chirurgische Behandlung nach dem „Damage Control“-Konzept ist bei der Versorgung schwerverletzter Patienten essenziell. Die Patientenversorgung sollte auf multidisziplinären, evidenzbasierten Behandlungsprotokollen fußen und einer regelmäßigen Qualitätsbewertung unterzogen werden. Dieser Beitrag hat einige wenige Empfehlungen der europäischen Leitlinie vorgestellt. Allen, die mit Traumapatienten zu tun haben, sei ein Blick in das Originaldokument nahegelegt.[1] Spahn et al. The European guideline on management of major bleeding and coagulopathy following trauma: fifth edition. Critical Care 2019; 23: 98. doi.org/10.1186/s13054–019–2347–3. ccforum.biomedcentral.com/articles/10.1186/ s13054–019– 2347–3
[2] Grade Leitlinien: Von der Evidenz zur Empfehlung. Determinanten, die Richtung und Stärke einer Empfehlung bestimmen. zefq-journal.com/article/S1865–9217(14)00159–7/pdf
[3] Damiani E, Adrario E, Girardis M et al. Arterial hyperoxia and mortality in critically ill patients: a systematic review and meta-analysis. Crit Care 2014;18 (6): 711
[4] Page D, Ablordeppey E, Wessman BT et al. Emergency department hyperoxia is associated with increased mortality in mechanically ventilated patients: a cohort study. Crit Care 2018; 22 (1): 9
[5] Aggarwal NR, Brower RG, Hager DN et al. National Institutes of Health Acute Respiratory Distress Syndrome Network I. Oxygen exposure resulting in arterial oxygen tensions above the protocol goal was associated with worse clinical outcomes in acute respiratory distress syndrome. Crit Care Med 2018; 46 (4):517–524
[6] Panwar R, Hardie M, Bellomo R et al. Conservative versus liberal oxygenation targets for mechanically ventilated patients. A pilot multicenter randomized controlled trial. Am J Respir Crit Care Med 2016; 193 (1): 43–51
[7] Smit B, Smulders YM, van der Wouden JC et al. Hemodynamic effects of acute hyperoxia: systematic review and meta-analysis. Crit Care 2018; 22 (1): 45
[8] Vincent JL, Taccone FS, He X. Harmful effects of hyperoxia in postcardiac arrest, sepsis, traumatic brain injury, or stroke: the importance of individualized oxygen therapy in critically ill patients. Can Respir J vol. 2017, Article ID 2834956, 7 pages, 2017
[9] Frank M, Schmucker U, Stengel D et al. Proper estimation of blood loss on scene of trauma: tool or tale? J Trauma 2010; 69 (5): 1191–1195
[10] Liu CC, Wang CY, Shih HC et al. Prognostic factors for mortality following falls from height. Injury 2009; 40 (6): 595–597
[11] Wongwaisayawan S, Suwannanon R, Prachanukool T et al. Trauma ultrasound. Ultrasound Med Biol 2015; 41 (10): 2543–2561
[12] Schieb E, Greim CA. Emergency sonography. Anaesthesist 2015; 64 (4): 329–342
[13] Gunn ML, Kool DR, Lehnert BE. Improving outcomes in the patient with polytrauma: A review of the role of whole-body computed tomography. Radiol Clin N Am 2015; 53 (4): 639–656
[14] Huber-Wagner S, Biberthaler P, Haberle S et al. Whole-body CT in haemodynamically unstable severely injured patients-a retrospective, multicentre study. PLoS One 2013; 8 (7): e68880
[15] Knottenbelt JD. Low initial hemoglobin levels in trauma patients: an important indicator of ongoing hemorrhage. J Trauma 1991; 31 (10): 1396–1399
[16] Holstein JH, Culemann U, Pohlemann T, Working Group Mortality in Pelvic Fracture P. What are predictors of mortality in patients with pelvic fractures? Clin Orthop Relat Res 2012; 470 (8): 2090–2097
[17] Bilkovski RN, Rivers EP, Horst HM. Targeted resuscitation strategies after injury. Curr Opin Crit Care 2004; 10 (6): 529–538
[18] Wilson M, Davis DP, Coimbra R. Diagnosis and monitoring of hemorrhagic shock during the initial resuscitation of multiple trauma patients: a review. J Emerg Med 2003; 24 (4): 413–422
[19] Lou X, Lu G, Zhao M. Preoperative fluid management in traumatic shock: a retrospective study for identifying optimal therapy of fluid resuscitation for aged patients. Medicine (Baltimore) 2018; 97(8): e9966
[20] Brenner M, Stein DM, Hu PF et al. Traditional systolic blood pressure targets underestimate hypotension-induced secondary brain injury. J Trauma Acute Care Surg 2012; 72 (5): 1135–1139
[21] Cohn SM, McCarthy J, Stewart RM et al. Impact of low-dose vasopressin on trauma outcome: prospective randomized study. World J Surg 2011; 35 (2): 430–439
[22] Chowdhury AH, Cox EF, Francis ST et al. A randomized, controlled, double-blind crossover study on the effects of 2-L infusions of 0.9% saline and Plasma-Lyte(R) 148 on renal blood flow velocity and renal cortical tissue perfusion in healthy volunteers. Ann Surg 2012; 256 (1): 18–24
[23] Raghunathan K, Shaw A, Nathanson B et al. Association between the choice of IV crystalloid and in-hospital mortality among critically ill adults with sepsis. Crit Care Med 2014; 42 (7): 1585–1591
[24] Self WH, Semler MW, Wanderer JP et al. Balanced crystalloids versus saline in noncritically ill adults. N Engl J Med 2018; 378 (9): 819–928
[25] Kutcher ME, Howard BM, Sperry JL et al. Evolving beyond the vicious triad: differential mediation of traumatic coagulopathy by injury, shock, and resuscitation. J Trauma Acute Care Surg 2015; 78 (3): 516–523
[26] Watts DD, Trask A, Soeken K et al. Hypothermic coagulopathy in trauma: effect of varying levels of hypothermia on enzyme speed, platelet function, and fibrinolytic activity. J Trauma 1998; 44 (5): 846–854