2013 wurde erstmals eine Sonderform von Schluckstörungen beschrieben, die typischerweise bei „frisch extubierten“ Intensivpatienten auftritt: die Post-Extubation-Dysphagie. Es handelt sich um ein ernst zu nehmendes Gesundheitsproblem, doch bislang ist es unter Praktikern kaum bekannt.
Ein intakter Schluckvorgang ist für den Menschen von vitaler Bedeutung. Täglich muss das Schlucken mehrere 1.000-mal fehlerfrei ablaufen, um ein Eindringen von Flüssigkeiten oder Nahrung in die Atemwege zu vermeiden. Die Zahl der Schluckvorgänge variiert im Tagesverlauf: Im Durchschnitt ist es ein Schluckvorgang pro Minute, während der Nahrungsaufnahme können es bis zu fünf sein. Im Schlaf verlängern sich die Abstände wieder deutlich.
Um Nahrung und Flüssigkeiten unterschiedlicher Konsistenzen von der Mundhöhle in den Magen zu befördern, bedarf es einer komplexen Koordination kinematischer Abläufe. Zur leichteren Steuerung werden Informationen aus sensomotorischen Aktivitäten gesammelt, u. a. über Geschmack und Größe. Auf diese Weise gelingt es i. d. R., neben der reinen Abfolge der Muskelkontraktionen eine reizabhängige Feinabstimmung des Schluckvorgangs zu erhalten [1].
Der Schluckvorgang ist aus anatomischer Sicht jedoch störanfällig, sodass auch beim gesunden Menschen bereits durch Unaufmerksamkeit ein fehlerhafter Schluckakt auftreten kann. Dies liegt daran, dass der obere Verdauungstrakt und Atemweg sich erst im unteren Pharynx wieder voneinander trennen. Um ein Eindringen von Nahrungsbestandteilen in den Kehlkopfeingang bzw. unter das Stimmlippenniveau zu vermeiden, hilft beim gesunden Menschen die intakte Sensibilität im Bereich des Hypopharynx bzw. des Kehlkopfs. Durch reflektorisches Abhusten ist die Entfernung des Fremdmaterials möglich.
Sonderform PED – kein seltenes Phänomen
Bei bestimmten Erkrankungen und Patientengruppen kann der Schluckvorgang gestört sein. Man spricht dann von einer Schluckstörung bzw. Dysphagie [1]. Die mit ihr verbundenen Komplikationen, wie Aspirationspneumonie [2], ein verlängerter Krankenhausaufenthalt [3, 4] und eine höhere Mortalität und Morbidität [4, 5], sind in der Praxis häufig zu beobachten.
Laut aktueller Datenlage weisen 3–62 % der Intensivpatienten Schluckstörungen auf. Die große Spannbreite lässt sich größtenteils mit den unterschiedlichen Studiendesigns begründen, die aufgrund unterschiedlich großer Patientenkohorten sowie verschiedener Ein- und Ausschlusskriterien nur schwer miteinander vergleichbar sind [6].
2013 wurde erstmals eine Sonderform der Dysphagie beschrieben, die typischerweise bei „frisch intubierten“ Patienten auftritt – die sog. Post-Ex- tubation-Dysphagie, kurz PED (engl. „ICU-acquired swallowing disorder“). Sie wird durch multifaktorielle Einflüsse beim kritisch kranken Patienten im intensivmedizinischen Krankenhaussetting begünstigt [7].
In einer großen Studie aus dem Jahr 2017, die sich speziell auf die PED bezog, wurde eine Inzidenz von 12,4 % identifiziert [4]. Da ein standardisiertes Dysphagiescreening auf allgemeinen Intensivstationen nicht erfolgt und in Leitlinien bislang auch nicht empfohlen wird [8, 9], bleibt die PED im Alltag einer Intensivstation meist unerkannt. Somit ist die PED ein bislang wenig wahrgenommenes, unterschätztes Gesundheitsproblem.
Typische Symptome: „Leaking“ und „Pooling“
Die Symptome der „allgemeinen“ Dysphagie und PED unterscheiden sich nicht voneinander. Typische Zeichen sind das sog. Leaking und Pooling sowie Residuen, Penetrationen und Aspirationen.
Beim Leaking entweichen orale Bolusbestandteile unkontrolliert entweder aus dem Mund (anteriores Leaking) oder nach hinten in den Rachenraum (posteriores Leaking). Das Ansammeln von Bolusbestandteilen im Rachenbereich wird in der Literatur auch als Pooling bezeichnet. Ursächlich für diese beiden Symptome sind sowohl eine gestörte orolinguale Boluskontrolle als auch eine verspätete Schluckreflextriggerung.
Unter Residuen sind Bolusreste zu verstehen, die nach dem Schluckvorgang z. B. in den Wangentaschen zurückbleiben. Für den Patienten können sie gefährlich werden, wenn diese aufgrund von Sensibilitätsstörungen im oralen/pharyngealen Bereich nicht wahrzunehmen sind.
Bei der Penetration gelangen Flüssigkeiten oder Speisereste in den Kehlkopfeingang, ohne die Stimmlippen zu passieren. Ursachen hierfür sind u. a. ein eingeschränkter Verschluss des Kehlkopfeingangs oder eine eingeschränkte Hebung des Kehlkopfs in der pharyngealen Phase.
Gelangt das Material in die Luftwege unterhalb der Stimmlippenebene, spricht man von einer Aspiration. Als Symptome einer direkten Aspiration können vor, während oder nach dem Schlucken Husten, ein gurgelndes Atemgeräusch, eine veränderte Stimmqualität (rau, feucht) sowie eine Zyanose oder Tachykardie auftreten [1].
Schädigung durch einen Tubus wohl Hauptursache für PED
Beim Intensivpatienten ist die Bestimmung der Dysphagieursache häufig erschwert, da von einem multifaktoriellen Einfluss auszugehen ist. Die Schluckstörungen sind jedoch meistens auf unterschiedliche Beeinträchtigungen der am Schluckvorgang beteiligten Hirnareale bzw. anatomischen Strukturen zurückzuführen. Vor allem bei einigen neurologischen Erkrankungen, z. B. beim Stroke im Bereich des Hirnstamms, ist die Wahrscheinlichkeit einer Dysphagie sehr hoch. Auch Beeinträchtigungen der Schluckmuskulatur, wie sie bei primär neuromuskulären Funktionsstörungen vorkommen, erhöhen das Risiko. Gleiches gilt für entzündliche Nervenschädigungen, z. B. im Rahmen einer Critical-Illness-Polyneuropathie.
Die Sonderform PED lässt sich durch folgende Faktoren erklären [6, 7]:
- oropharyngeales/laryngeales Trauma (z. B. durch einen Tubus)
- qualitative und/oder quantitative Bewusstseinsstörungen
- gastroösophagealer und pharyngealer Reflux
- Dyskoordination zwischen Atmung und Schlucken
- Neuromyopathien (Critical-Illness-Neuro- und Myopathien)
Besonders die direkte Schädigung durch einen Tubus scheint für die Entstehung einer PED eine der Hauptursachen zu sein. Durch die Beeinträchtigung der Chemo- und/oder Mechanorezeptoren in der Larynx-/Pharynxmukosa werden sensorische Beeinträchtigungen, die Entstehung lokaler Inflammationsprozesse und Ulzerationen begünstigt. Dies kann zu Beeinträchtigungen des Schluckvorgangs während der pharyngealen Phase führen [1]. Krankheitsbilder wie Sepsis oder Multiorganversagen bzw. deren Folgeschäden – in Form von Critical-Illness-Neuro- und Myopathien oder allgemeiner Muskelschwäche [10] – beeinträchtigen über die systemischen inflammatorischen Prozesse Rezeptoren im Oropharynx und Larynx. Häufig korreliert auch die Notwendigkeit einer invasiven Beatmung mit der Schwere der Sepsis, wodurch längere Beatmungszeiträume notwendig werden und das Risiko einer PED steigt [11–14].
Risikopatienten früh erkennen
Zur Diagnostik der PED stehen unterschiedliche Methoden zur Verfügung, wobei die Fiberoptische Endoskopische Evaluation des Schluckens (FEES) – neben der Videofluoroskopischen Untersuchung des Schluckens (VFSS) – als „Goldstandard“ anzusehen ist [6, 9]. Diese Untersuchungen erfolgen im stationären Bereich häufig bettseitig durch speziell qualifizierte Ärztinnen und Ärzte oder Logopädinnen und Logopäden.
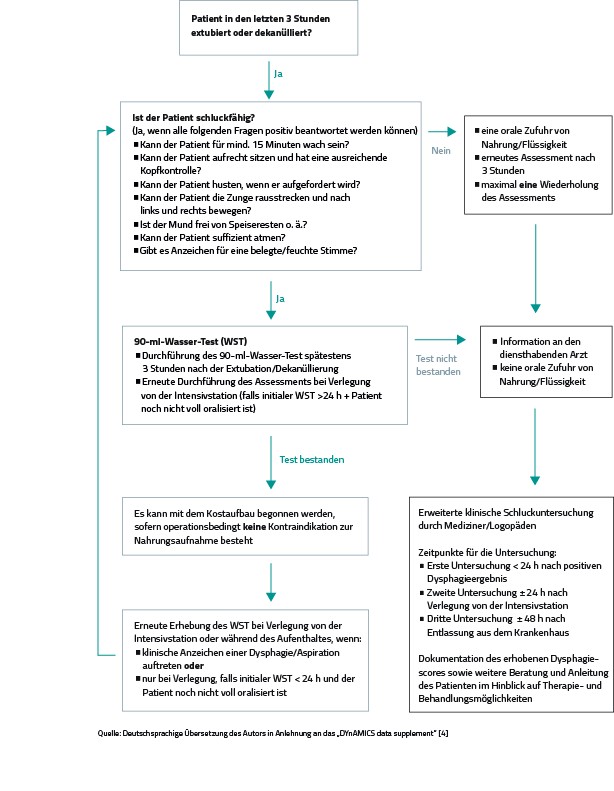
Um gefährdete Patienten frühzeitig detektieren zu können, empfiehlt sich eine algorithmusbasierte Vorgehensweise, die bei einem positiven Screeningbefund eine genaue Beurteilung des Schluckvorgangs durch eine FEES veranlasst. Die Literatur empfiehlt zum Screening der Patienten den „3-Ounce Water Swallow Test“ (WST) [4, 7, 13, 16]. In der deutschsprachigen Literatur lautet die Bezeichnung „90-ml-Wasser-Test“ [15]. Mithilfe dieses Tests lassen sich mit einer Wahrscheinlichkeit von 96,5 % aspirationsgefährdete Patienten detektieren [15]. Für die Durchführung des Tests muss der Patienten 90 ml Wasser ohne Unterbrechung aus einer Tasse (mit oder ohne Strohhalm) trinken. Von einer Aspiration ist auszugehen, wenn der Patient nicht die gesamte Flüssigkeitsmenge trinken kann, innerhalb von bis zu einer Minute nach Ende des Tests ein Husten auftritt oder eine feuchte Stimmqualität auffällt.
In Abbildung 1 ist ein zweischrittiges Screening dargestellt, um eine PED diagnostizieren zu können. Der Algorithmus wurde innerhalb einer Studie mit mehr als 1.300 Patienten erfolgreich getestet [4].
Drei Säulen der Behandlung
Die Studienlage zur Behandlung von Intensivpatienten mit einem positiven Dysphagiebefund ist limitiert. Dennoch lassen sich drei Säulen in der Behandlung beschreiben, die die Anpassung der Nahrungskonsistenz, das Erlenen von Kompensationstechniken sowie Maßnahmen zur Verbesserung des Schluckvorgangs beinhalten. Diese Maßnahmen sind in ein interdisziplinäres Behandlungskonzept einzubetten. Zur Veränderung der Nahrungs- und Flüssigkeitskonsistenz werden Andickmittel oder spezielle Trinkbecher genutzt, die eine zu schnelle und unkontrollierte Passage des Oropharynx/Larynx verhindern. Kompensationstechniken zur Vermeidung von Aspirationen sind z. B. Haltungsänderungen während der Nahrungsaufnahme, sodass – je nach Befund – die Kopfposition nach vorne, hinten oder zur Seite geneigt werden kann, um das Abschlucken des Bolus zu ermöglichen. Zur Verbesserung des Schluckvorgangs könnten bei herabgesetzten Schluckreflexen z. B. mit Eiswürfeln verstärkte Reize gesetzt sowie Übungen zur Verbesserung der am Schluckvorgang beteiligten Muskeln erfolgen [2, 6].Folgeschäden vermeiden
Aufgrund der Komplexität und der Dynamik der Dysphagie ist – unabhängig vom genutzten Assessmentinstrument – eine Einschätzung nicht als einmalige diagnostische Maßnahme anzusehen, sondern eine kontinuierliche Aufgabe. Hierbei können Pflegende aufgrund ihres engen Kontakts mit dem Patienten einen entscheidenden präventiven Einfluss auf seine Mortalität und Verweildauer nehmen. Voraussetzung ist, dass entsprechendes Hintergrundwissen über dysphagiebezogene Risikofaktoren und Assessmentinstrumente vorliegen. Die Einschätzung mit dem 90-ml-Wasser-Tests bzw. die Nutzung des zweischrittigen Algorithmus kann helfen, um Risikopatienten zu detektieren und diese bei positiven Screeningbefunden einer instrumentellen Diagnostik im Rahmen einer FEES zuzuführen. Folgeschäden sind so vermeidbar. Dies scheint auch vor dem Hintergrund, dass nach der Entlassung bei einem Großteil der Patienten die Dysphagiesymptomatik weiterhin besteht, als äußerst relevant [4].[1] Prosiegel M, Weber S. Grundlagen der Schluckanatomie und -physiologie. Dysphagie: Diagnostik und Therapie. Ein Wegweiser für kompetentes Handel (Praxiswissen Logopäde). Springer 2018: 5–68
[2] Zielske J, Bohne S et al. Acute and long-term dysphagia in critcally ill patients with severe sepsis: results of a prospective controlled observational study. Eur Arch Otorhinolaryngol 2014; 271 (11): 3085–3093
[3] Macht M, King CJ et al. Post-extubation dysphagia is associated with longer hospitalization in survivors of critical illness with neurologic impairment. In: Critical Care 2013; 17 (3): R119
[4] Schefold JC, Berger D et al. Dysphagia in mechanically ventilated ICU-patients (DYnAMICS): a prospektive observational trial. In: Critical Care Medicine 2017; 45 (12): 2061–2069
[5] Ponfick M, Linden R et al. Dysphagia-a common transient symptom in critical illness polyneuopathy: a fiberoptic endoscopic evaluation of swallowing study. Critical Care Medicine 2015; 43 (2): 365–372
[6] Zuercher P, Moret C et al. Dysphagia in the intensive care unit: epidemiology, mechanisms and clinical management. Critical Care 2019; 23 (103): 1–11
[7] Macht M, Wimbish T et al. ICU-aquired swallowing disorders. Critical Care Medicine 2013; 41 (10): 2396–2405
[8] Wirth R, Dziewas R et al. Leitlinie der Deutschen Gesellschaft für Ernährungsmedizin (DGEM). Klinische Ernährung in der Neurologie 2013; DOI: 10.1055/s-0033–1343317
[9] Prosiegel M. Neurogene Dysphagien – Leitlinie für Diagnostik und Therapie in der Neurologie. Diener H (Hrsg.). Leitlinien für Diagnostik und Therapie in der Neurologie. Springer 2012: 1078–1087
[10] Berger D, Bloechlinger S et al. Dysfunction of respiratory muscles in critically ill patients on the intensive care unit. J Cachexia Sarcopenia Muscle 2016; 7 (4): 403–412
[11] Brown C, Hejl K et al. Swallowing dysfunction after mechanical ventilation in trauma patients. J Critical Care 2011; 26: 9–13
[12] Kwok A, Davis J et al.Post-Extubation dysphagia in trauma patients: it’s hard to swallow. Am J Surgery 2013;206: 924–928
[13] Perren A, Zuercher P et al. Clinical Approaches to assess post-extubation dysphagia (PED) in the critically ill. Dysphagia 2019: 1–12
[14] Kim M, Park Y et al. Associations between prolonged intubation and developing post-extubation dysphagia and aspiration pneumonia in non-neurologic critically ill patients. Ann rehab med 2015; 39 (5): 763–771
[15] Suiter DM, Leder SB. Clinical Utility of the 3-ounce Water Swallow Test. Dysphagia 2008; 23: 244–250
[16] Skoretz S, Flowers H et al. The incidence of dysphagia following Endotrachel intubation: a systematic review.Chest 2010; 137 (3): 665–673