Patienten mit geblockter Trachealkanüle auf der Intensivstation können meist nicht sprechen. Die „Above Cuff Vocalisation“ (ACV) ermöglicht durch gezielte Luftzufuhr über das subglottische Lumen temporär die Sprachfähigkeit und verbessert so Lebensqualität, Kommunikation sowie Sekretmanagement – dabei ist auf sorgfältige Indikationsstellung, korrekte Ausführung und mögliche Kontraindikationen zu achten.
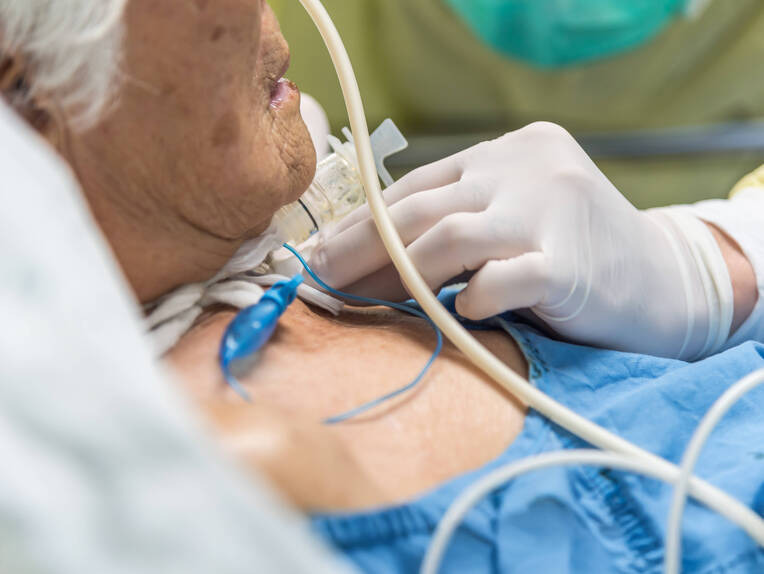
Patienten auf der Intensivstation, die im Rahmen der intensivmedizinischen Therapie eine invasive Beatmung oder eine Sicherung der Atemwege mittels eines Tubus oder einer Trachealkanüle benötigen, sind infolge des geblockten Cuffs der entsprechenden Atemwegszugänge nicht in der Lage, zu sprechen. Denn der geblockte Cuff an der Trachealkanüle oder dem Endotrachealtubus verhindert einen Luftstrom aus dem Larynx in Richtung Stimmbänder, sodass keine Stimmbildung möglich ist [1–3].
Im Jahr 2023 erhielten 24.686 erwachsene Patientinnen und Patienten auf den deutschen Intensivstationen temporäre Tracheotomien. Rund zwei Drittel dieser Patienten waren über 65 Jahre alt und überwiegend männlich [4]. Vorausgegangen ist in diesen Fällen stets die primäre Intubation mittels endotrachealen Tubus, ehe zum Beispiel bei einem zu erwartenden prolongierten Weaning, einer Beatmungsdauer von mehr als zehn Tagen oder anderen Indikationsstellungen eine temporäre Tracheotomie erfolgte [5]. Somit handelt es sich bei diesem eher älteren tracheotomierten Klientel häufig um Patienten, die bereits mehrere Tage auf der Intensivstation liegen und bei denen frühere Weaningversuche oder Spontanatmungsversuche (SBT) frustran geblieben sind – in der Literatur als prolongiertes Weaning bezeichnet [6].
Anders als Patienten mit einem oralen Tubus benötigen tracheotomierte Patienten häufig deutlich weniger oder idealerweise gar keine Sedierung. Mit zunehmender Wachheit wächst der Wunsch der Patienten, mit dem Personal oder den Angehörigen zu kommunizieren.
Das Tracheostoma macht dies jedoch oft unmöglich. Diese Unfähigkeit zur Kommunikation geht unter Umständen mit Ängsten, Stress, Frustration und Depression der Patienten einher [2, 7]. Auch wenn verschiedene Alternativen in Form von Schreibtafeln, Lippenlesen, Körpersprache oder Piktogrammen zum Ausdruck von Bedürfnissen und zur Kommunikation auf der Intensivstation vorübergehend unterstützen können, so stellt aus Sicht der Patienten die Wiederherstellung der eigenen Sprache die bevorzugte Art und Weise dar, um mit anderen Personen zu interagieren [1, 7].
Die Wiedererlangung der Sprachfähigkeit führt nicht nur zu einer Verbesserung der wahrgenommenen Lebensqualität der beatmeten Patienten [8], sondern ermöglicht auch dem medizinischen Fachpersonal ein besseres Verständnis von der Stimmung, der Orientierung sowie der kognitiven Leistungsfähigkeit der Patienten. Darüber hinaus lassen sich auch laryngeale Verletzungen oder Funktionseinschränkungen sowie Beeinträchtigungen im Sekretmanagement oder auch eine Dysphagie detektieren [9, 10].
Während des Weaningprozesses von der Trachealkanüle oder der Beatmung ist es bereits auf der Intensivstation ein Ziel, mit sukzessiver Verlängerung der Entblockung des Cuffs an der Trachealkanüle den oberen mit dem unteren Atemweg zu verbinden. Die so wiederhergestellte laryngeale Luftführung erlaubt die Sprachfähigkeit.
Dafür stehen in der klinischen Praxis verschiedene Verfahren zur Verfügung, die sowohl unter Beatmung als auch unter Spontanatmung eine Reaktivierung von Larynx und Pharynx sowie die Sprachfähigkeit unterstützen [9, 11]. Allen Verfahren gemeinsam ist die notwendige Entblockung des Cuffs an der Trachealkanüle. Eine Entblockung ist jedoch kontraindiziert bei Patienten mit eingeschränktem Sekretmanagement – etwa infolge vermehrter Sekretbildung, ineffizienter mukoziliärer Clearance, eines unzureichenden Hustenstoßes oder bei bestehender Dysphagie [6].
Sprechen ermöglichen
Die „Above Cuff Vocalisation“ (ACV) ist ein Verfahren, um Patienten mit geblockter Trachealkanüle temporär das Sprechen zu ermöglichen. Die Literatur beschreibt die Anwendung der ACV bei einer Vielzahl von Patienten – nahezu unabhängig von der Grunderkrankung. Kontraindiziert ist sie lediglich bei Patienten mit Stenosen oder Schwellungen der oberen Atemwege, etwa nach Hals-Nasen-Ohren-Eingriffen [12].
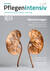
Für eine ACV muss die Trachealkanüle über ein subglottisches Absaugungslumen verfügen und für die ACV selbst zugelassen sein (zum Beispiel Portex™ BLUselect™ von Smith Medical, Duracuff® Pro von Fahl Medizintechnik, Tracoe Extract Kanülen von Atos Medical), da es sich sonst gemäß Medizinproduktegesetz um einen Off-Label-Use handelt.
Bei Applikation eines Flows von ein bis fünf Litern pro Minute Sauerstoff oder Druckluft mittels subglottischen Ports lässt sich dieser über die Stimmbänder leiten und ermöglicht dem Patienten das Sprechen [10, 12].
Die Methode wurde erstmals 1967 beschrieben [13], später im Rahmen des Global Tracheostomy Collaborative in Australien und Großbritannien weiterentwickelt und ist auch unter den Bezeichnungen „External Subglottic Air Flow“ (ESAF) [14], „Vocalaid“ oder „Speaking Tracheostomy“ [8, 15] bekannt. In der Literatur sind durchschnittliche Anwendungsdauern von wenigen bis maximal 30 Minuten beschrieben. Die Anwendung kann zwei- bis viermal täglich oder bei Bedarf – etwa bei Patientenwunsch oder Angehörigenbesuch – erfolgen [16].
ACV – einzelne Schritte
Prüfung. Vor dem erstmaligen Einsatz ist individuell zu prüfen, ob die ACV für den jeweiligen Patienten geeignet ist. Dafür sollten der Zeitpunkt der (dilatativen) Tracheostomaanlage etwa 36 bis 48 Stunden [12] zurückliegen, das Tracheostoma einen reizlosen und entzündungsfreien Eindruck machen sowie keine Obstruktionen der oberen Atemwege vorliegen [17].
Sekretentfernung. Nach der entsprechenden Patientenaufklärung über das geplante Vorgehen und potenzielle Nebenwirkungen, zum Beispiel zunehmende Sekretion, Übelkeit oder Husten, erfolgt die Sekretentfernung über das subglottische Lumen der Trachealkanüle, wobei ein zu starker Sog zu vermeiden ist, um Hustenreiz zu reduzieren.
Das Sekret lässt sich entweder mit einem Instrument mit regulierbarer Sogstärke oder langsam mittels einer Spritze (10 ml) absaugen. Der Patient ist in Rückenlage mit nach hinten geneigtem Oberkörper zu positionieren, um möglichst viel optionales Sekret aus dem subglottischen Bereich entfernen zu können.
Ein Ansaugen von Luft in der Spritze oder an der Absaugeinrichtung zeigt das freie Lumen oberhalb des Cuffs an und spricht für eine erfolgreiche Reinigung. Lässt sich weder Sekret noch Luft mobilisieren, so spricht dies für eine Verlegung des subglottischen Absaugschlauchs, die sich mit behutsamer Spülung des okkludierten Schlauchs mit geringen Menge (etwa 2 bis 3 ml) einer 0,9-prozentigen Natriumchlorid-Lösung beheben lässt [18, 19].
Anschließend ist der Oberkörper des Patienten zur Förderung der Wahrnehmung und Interaktion wieder aufzurichten und die Position nach Wunsch anzupassen.
Anschluss. Im nächsten Schritt erfolgt die Konnektion der subglottischen Absaugung mit Druckluft oder Sauerstoff über einen entsprechenden Verbindungsschlauch. Geeignete Adapter oder Konnektoren sind häufig im Lieferumfang der Trachealkanüle enthalten.
Luftzufuhr. Nach erfolgreichem Anschluss kann die Luftzufuhr zunächst mit einem geringen Flow beginnen und ist schrittweise von etwa einem auf maximal fünf bis sechs Liter pro Minute zu steigern. Ist eine Phonation beim Patienten festzustellen, so ist der Luftstrom auf das erforderliche Maß zu reduzieren. Dies verringert nicht nur das Risiko einer Austrocknung oder Reizung der Atemwege, sondern auch die Entstehung störender Umgebungsgeräusche [17, 19].
Ebenfalls reizreduzierend kann zu Beginn eine subglottische Luftzufuhr ausschließlich während der Exspiration wirken, da sich die Auswirkungen einer möglichen Hypersensibilisierung der Atemwege – bedingt durch einen zuvor fehlenden Luftstrom – besser kontrollieren lassen [19].
Phonation. Zu Beginn führt der Flow zu einer möglichen Mobilisation von Sekreten aus dem Pharynx oder Larynx in Richtung Mundraum, wo es ent- sprechend abzusaugen oder zu expektorieren ist. Für die Beurteilung der Kommunikationsmöglichkeiten des Patienten empfiehlt sich das sogenannte Reihensprechen: das Aufzählen von Wochentagen, Monaten oder Zahlen.
Bei wahrnehmbarer Phonation (Wiederholung) kann die ACV fortgeführt werden. Treten hierbei jedoch Probleme auf, so ist der Versuch zu beenden und zu einem späteren Zeitpunkt neu aufzunehmen.
Zur akustischen Beurteilung des Luftstroms ist im Zweifelsfall auf die Auskultation der Atemwege mittels eines Stethoskops zurückzugreifen. Ist dabei kein laryngealer, nasaler oder oraler Flow feststellbar, so ist auch in diesem Fall der Versuch abzubrechen, um das Risiko eines potenziellen Hautemphysems im Zuge der Maßnahme zu vermeiden [20]. In der Erprobungs- oder Anfangsphase sollte die ACV daher nicht unbeaufsichtigt erfolgen.
Da die für die Phonation erforderliche Regulation des subglottischen Drucks über die Bauchmuskulatur beim geblockten Cuff nicht möglich ist, ist für eine ausreichende Stimmbandschwingung ein geeigneter Druck über die Variation des Flows zu erzielen [19].
Dokumentation. Ließen sich in Zusammenarbeit mit dem Patienten geeignete Einstellungen des Flows festlegen, sind diese sinnvollerweise in der Patientendokumentation oder auf einem separaten Dokumentationsbogen festzuhalten. Neben dem Flow sind auch die Anwendungsdauer, besondere Auffälligkeiten sowie weitere Beobachtungen zu dokumentieren – etwa zur Information der nachfolgenden Schicht oder als Verlaufsbeschreibung.
Idealerweise lassen sich unter Einbeziehung der Logopädie weitere Parameter erfassen – etwa zum Sekretstatus (New Zealand Secretion Scale, NZSS [21]), zur Schlucksicherheit (Penetrations-Aspirations-Skala, PAS [22]) oder zur Schluckeffizienz (Yale Pharyngeal Residue Severity Rating Scale, YPRSS [23]).
Aktivierung des Patienten
Die ACV empfiehlt sich besonders bei antriebs- geminderten Personen, um deren Beteiligung zu fördern und gezielt einen Kommunikationsanlass zu schaffen – zum Beispiel im Rahmen einer Visite, eines Angehörigenbesuchs oder eines Telefonats – oder um gezielt zum Schlucken anzuleiten oder aufzufordern. Ist eine gute Verständigung möglich, empfindet der Patient den kontinuierlichen Luftstrom jedoch als unangenehm, lässt sich die Stimmbildung bei ausreichender motorischer Aktivität des Patienten über eine manuelle Steuerung (Fingertip) bedarfsorientiert auslösen [24]. Zu Beginn kann infolge begrenzter Belastbarkeit des Patienten ein zeitlich befristeter ACV-Versuch erfolgen. Zeigen sich Anzeichen einer Erschöpfung, ist die Maßnahme zu beenden, der Luftanschluss zu entfernen und der subglottische Zugang aus hygienischen Gründen zu verschließen [8, 19].
Trotz der einfachen Handhabung lassen sich in der Literatur verschiedene Problemstellungen und Herausforderungen finden, die eine erfolgreiche Umsetzung der ACV in der Praxis beeinträchtigen oder deren Lösungsstrategien für eine sichere Anwendung am Patienten bekannt sein sollten (Tabelle).
Vorteile der ACV bei moderater Evidenz
Auch wenn die gegenwertige Qualität der Evidenz, in Anlehnung an die internationalen GRADE-Kriterien von moderat bis sehr niedrig zu bewerten ist (GRADE steht für Grading of Recommendations, Assessment, Development and Evaluation und ist eine international anerkannte Methode zur Bewertung der Qualität von Evidenz und der Stärke von Empfehlungen im Gesundheitswesen), so lassen sich dennoch potenzielle Benefits für den Patienten bezüglich Schlucken, Schluckakt, Sekretmanagement, Husten(stoß) und Lebensqualität feststellen [16, 26, 27].
Diese beschriebenen Vorteile überwiegen auch nach Ansicht anderer Autoren gegenüber den berichteten Nebenwirkungen der ACV wie temporärer Diskomfort, Übelkeit und Unwohlsein oder zwischenzeitlicher Sekretaufstau oberhalb des Cuffs bei Hypersekretionen [17, 25, 26, 28].
Somit ist die ACV aus pflegerischer Sicht eine einfache Maßnahme, die sich positiv auf das Schluckvermögen und das Sekretmanagement auswirken kann und vor allem in der Frühphase, in der eine Entblockung noch nicht realisierbar ist, eine risikoarme Intervention mit einem nicht nur kommunikativen Nutzen bietet.
[1] Zaga CJ, Berney S, Vogel AP. The Feasibility, Utility, and Safety of Communication Interventions with mechanically ventilated intensive care unit patients: a systematic review. American Journal of Speech and Language Pathology 2019; 28 (3): 1335–1355
[2] Ten Hoorn S, Elbers PW, Girbes AR, Tuinman PR. Communicating with concious and mechanically ventilated critically ill patients: a systematic review. Critical Care 2016; 20 (1): 333
[3] Karlsen MW, Olnes MA, Heyn LG. Communication with patients in intensive care units: a scoping review. Nursing in Critical Care 2019; 24 (3): 115–131
[4] Statistisches Bundesamt (Destatis). Operationen und Prozeduren an vollstationären Patienten: Deutschland, Jahre, Geschlecht, Altersgruppen, Operationen und Prozeduren mit der OPS-5–311. 2015. Im Internet: https:// www-genesis.destatis.de/datenbank/online/statistic/ 23141/table/23141-0101; Zugriff 14.06.2025
[5] Vargas M, Sutherasan Y, Antonelli M. Tracheostomy procedures in the intensive care unit: an international survey. Critical Care 2015; 19: 291e1–291e10
[6] Schönhofer B, Geiseler J, Braune S et al. S2k-Leitlinie prolongiertes Weaning. 2019: 13–22. Im Internet: register.awmf.org/assets/guidelines/020-015l_ S2k_Prolongiertes_Weaning_2024-08_abgelaufen.pdf; Zugriff: 14.06.2025
[7] Freeman-Sanderson AL, Togher L, Elkins MR et al. Quality of life improves with return of voice in tracheostomy patients in intensive care: An observational study. Journal of Critical Care 2018; 33: 186–191
[8] Pandian V, Cole T, Kilonsky D et al. Voice-related quality of life increases with a talking tracheostomy tube: a randomized controlled trail. Laryngoscope 2020; 130 (5): 1249–1255
[9] Wallace S, McGowan S, Sutt AL. Benefits and optionas for voice restoration in mechanically ventilated intensive care unit patients with a tracheostomy. Journal of the Intensive Care Societey 2022; 24 (1): 104–111
[10] McGrath BA, Wallace S, Lynch J et al. Improving tracheostomy care in the United Kingdom: results of a guided quality improvement programme in 20 diverse hospitals. Brit J Anaes (BJA) 2020; 125: e119–e129
[11] Nusser-Müller-Busch R, Jädicke M. Vom Entblocken zur Teilhabe. Trachealkanüle-Management beginnt auf der Intensivstation. Forum:Logopädie 2022; 36 (4): 16–21
[12] McGrath BA, Lynch J, Wilson M, Nicholson L, Wallace S. Above cuff vocalisation: a novel technique for communication in the ventilator-dependant tracheostomy patient. Journal of the intensive care society 2016; 17 (1): 19–26
[13] Safar P, Grenvik A. Speaking cuffed tracheostomy tube. Critical Care Medicine 1975; 3 (1): 23–26
[14] Kothari M, Bjerrum K, Nielsen LH et al. Influence of external subglottic air flow on dysphagic tracheotomized patients with severe brain injury: preliminary findings. Annals of Otology, Rhinology & Laryngology 2017; 126 (3): 199–204
[15] Mitate E, Kubota K, Ueki K et al. Speaking Tracheostomy Tube and Modified Mouthstick Stylus in a Ventilator-Dependent Patient with Spinal Cord Injury. Case Reports in Emergency Medicine 2015: 1–3
[16] Mills CS, Michou E, Bellamy MC et al. Determining the prevalence, implementation approaches, and opinions of above cuff vocalization: a survey of health care professionals. Archives of Physical Medicine and Rehabilitation 2022a; 103 (3): 394–401
[17] McGrath BA, Wallace S, Wilson M et al. Safety and feasibility of above cuff vocalisation for ventilator-dependant pateints with tracheostomie. Journal of the Intensive Care Society 2019; 20 (1): 59–65
[18] Husain T, Gatward JJ, Harris RD. Use of subglottic suction port to enable verbal communication in ventilator-dependent patients. American Journal of Respiratory and Critical Care Medicine 2011; 184: 384–384
[19] Niers N. Subglottische Luftinsufflation bei tracheotomierten Patien- tInnen. ACV: „above cuff vocalisation“ oder „above cuff ventilation“? Eine Übersicht mit praktischer Handreichung. Logos 2019; 27 (2): 106–112
[20] Calmai I, Giuntini R, Tomeo F, Spina R. Sudden apperance of neck and face emphysema during above cuff vocalisation. Intensive Care Medicine 2018; 44 (11): 1951–1952
[21] Miles A, Hunting A. Development, intra- and interrater reliability of the New Zealand Secrection Scale (NZSS). International Journal of Speech and Language Pathology 2019; 21 (4): 377–384
[22] Borders JC, Brates D. Use of the penetration-aspiration scale in dysphagia research: a systematic review. Dysphagia 2020; 35 (4): 583–597
[23] Neubauer P, Rademake A, Leder SB. The Yale Pharyngeal Residue Severity Rating Scale: an anatomically defined and image-based tool. Dysphagia 2015; 30 (5): 521–528
[24] Mills CS, Michou E, Bellamy MC et al. Worth a try or a last resort: healthcare professionals’ experiences and opinions of above cuff vocalisation. International Journal of Language and Communication Disorders 2024; 59: 932–946
[25] Mills CS, Michou E, Siddle HJ, Bojke C, the ACoUSTiC Group. Troubleshooting above cuff vocalisation. Intensive Care Medicine 2025; 51: 421–425
[26] Petosic A, Viravong MF, Martin AM et al. Above Cuff Vocalisation (ACV): a scoping review. ACTA Anaesthesiologica Scandinavica 2021; 65: 15–25
[27] Mills CS, Michou E, King N et al. Evidence for above cuff vocalization in patients with a tracheostomy: a systematic review. The Laryngoscope 2022b; 132 (3): 600–661
[28] Pandian V, Bose S, Miller C et al. Exploring quality of life in critically ill tracheostomy patients: a pilot study. Journal oft he Society of Otorhinolaryngology and Head-Neck Nurses 2014; 32 (1): 6–13