Ältere, hochbetagte und immungeschwächte Intensivpatienten sind besonders anfällig für schwere Infektionen. Auslöser können viele pathogene Mikroorganismen wie Hefe- und Schimmelpilze sein. Eine Immunsuppression kann auch Viren, die latent im Körper vorhanden sind, reaktivieren und so den Gesundheitszustand weiter verschlechtern.
In einer Übersichtsarbeit haben Intensivmedizinerinnen und -mediziner der Universitätsklinik Lille in Frankreich aktuelle Aspekte der Diagnostik nosokomialer Infektionen im Zusammenhang mit der Behandlung immunsupprimierter Patientinnen und Patienten auf Intensivstationen dargestellt [1].
Für ihre Studie unternahmen die Autorinnen und Autoren eine Stichwortsuche in medizinischen Literaturdatenbanken für den Zeitraum von 2003 bis 2023. Die eingegebenen Stichworte waren – in englischer Sprache – Immunsuppression, Intensivtherapie, Infektionen und Antibiotikaresistenz. Zusätzlich gaben sie zahlreiche hämatologisch-onkologische Stichworte wie Karzinom, Leukämie, HIV oder Transplantation ein. Den Literaturverzeichnissen der Arbeiten entnahmen die Autoren weitere Hinweise auf wichtige Literaturquellen. Nach Durchsicht der Arbeiten werteten sie diejenigen Originalarbeiten aus, die sich mit der Definition der Immunsuppression auf der Intensivstation und den besonderen diagnostischen Möglichkeiten bei dieser Patientengruppe befassten.
Definition einer Immunsuppression
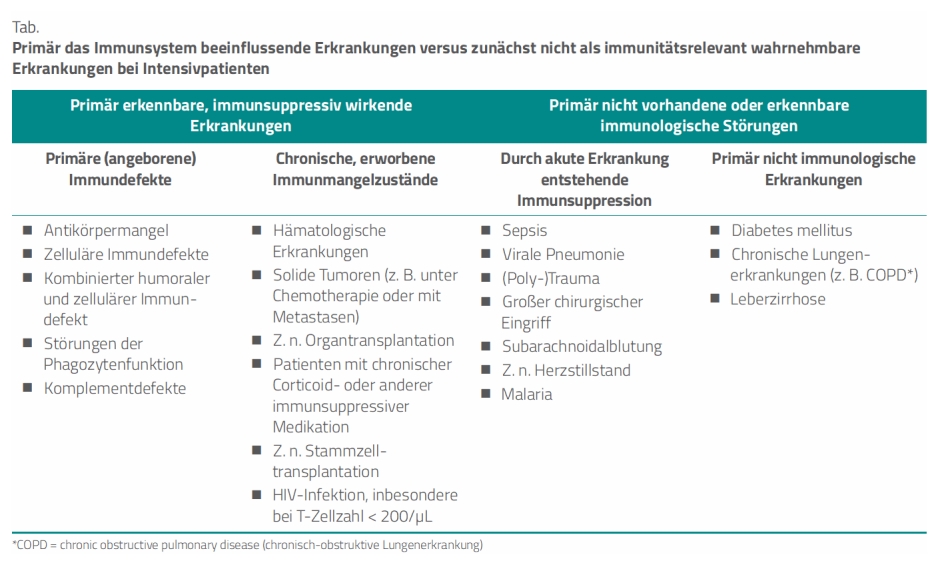
Die Studienautoren unterscheiden zwei grundsätzlich verschiedene Arten von immunsuppressiven Erkrankungen auf der Intensivstation (Tab.):
- Erkrankungen oder chronische Zustände, die das Knochenmark oder das Immunsystem betreffen. Diese Patienten sind meist schon bei der Aufnahme auf die Intensivstation als immunsupprimiert erkennbar.
- Primär nicht als immunrelevant wahrnehmbare Erkrankungen, die aber – nicht zuletzt erkennbar an Labormarkern – mit einer erheblichen Störung der Infektabwehr einhergehen können.
Ursachen für die Anfälligkeit gegenüber Infektionserregern
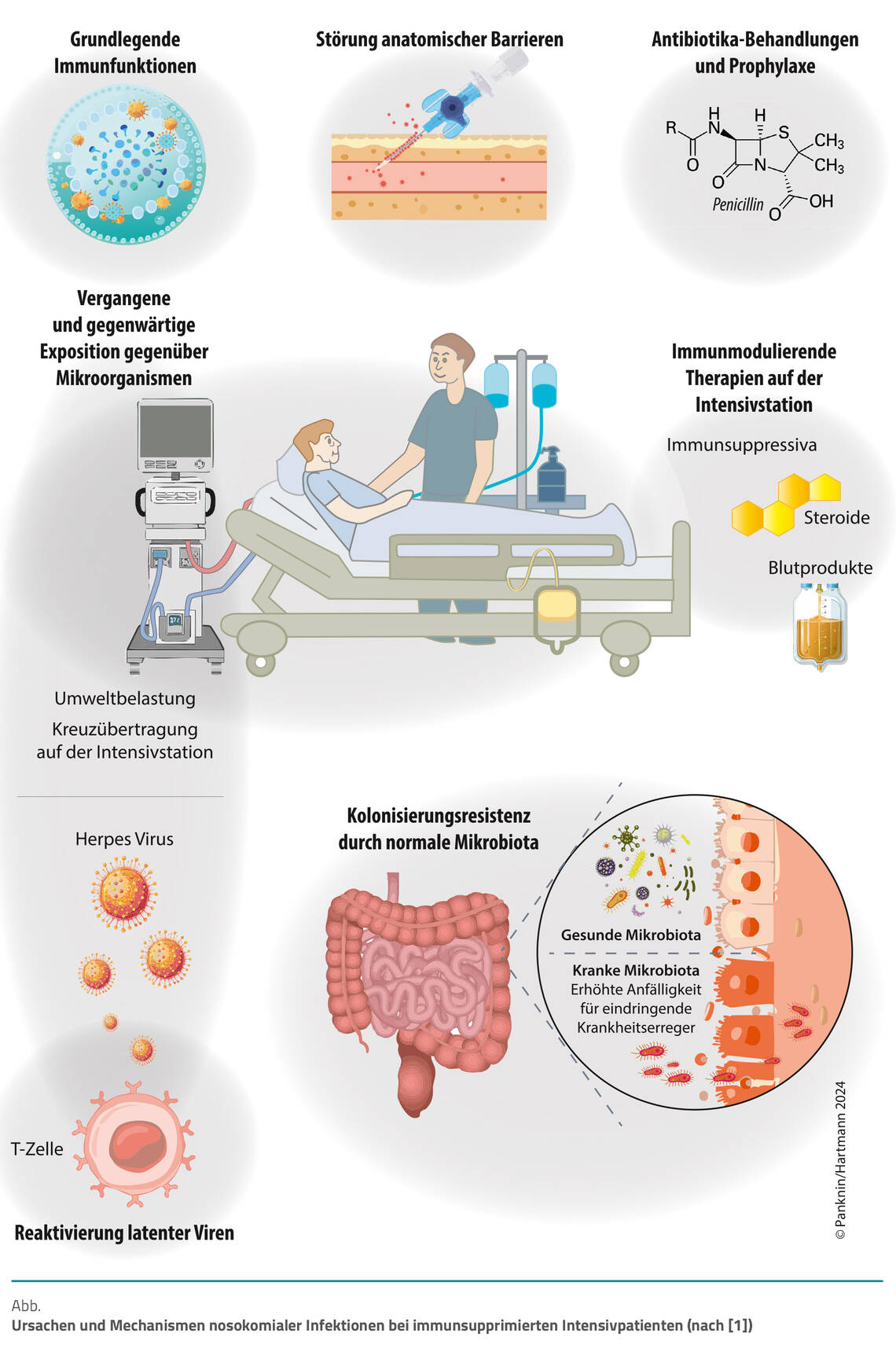
Immunsupprimierte Patienten sind auf der Intensivstation einem deutlich höheren Risiko ausgesetzt, eine nosokomiale Infektion durch Bakterien, Viren sowie Pilze zu erleiden, als immungesunde Patienten. Die Abbildung zeigt die Ursachen und Mechanismen, die dabei eine Rolle spielen.
Das stilisierte entzündliche Granulom im linken oberen Feld der Abbildung stellt die Verminderung der allgemeinen Immunität durch Leukozytenmangel (Leukopenie), Störung der Makrophagenfunktion und Einschränkung der zellulären Immunität dar. Dadurch kann die Bildung von Granulomen gestört sein, die für die Abwehr intrazellulär lebender Erreger entscheidend sind. Erreger dieser Gruppe sind Mykobakterien, einschließlich Mycobacterium tuberculosis, sowie Listerien, die eine Sepsis oder Meningitis auslösen können.
Ein weiterer wichtiger Mechanismus ist im rechten unteren Feld der Abbildung dargestellt. Es handelt sich um die therapiebedingte Störung der normalen Darmflora. Durch vorangegangene Antibiotika-Therapiezyklen (rechtes oberes Feld), Durchblutungsstörungen des Darms und Unterbrechung der enteralen Ernährung verschwindet die physiologische, schützende Bakterienflora des unteren Dünn- und Dickdarms. Stattdessen treten Erreger aus dem Krankenhausmilieu auf, wie gramnegative (oft multiresistente) Stäbchenbakterien, Pseudomonaden und Pilzarten (zum Beispiel Candida spp.). Diese Erreger können bei fehlender Abwehr durch physiologische Keime die Darmwand durchdringen und in den Blutkreislauf gelangen.
Weitere Felder der Abbildung zeigen die mögliche Übertragung von Keimen über die Hände des medizinischen Personals, über medizinische Geräte (Mitte links) und die Durchdringung anatomischer Barrieren wie der Haut durch invasive Katheter oder Punktionen (Mitte oben).
Infolge des Stresses einer Intensivbehandlung können auch latent im Körper des Patienten vorhandene Viren „erwachen“ und eine akute Infektionssymptomatik auslösen (Feld links unten). Ein typisches Beispiel hierfür ist der plötzlich auftretende Herpes zoster (Gürtelrose), der aufgrund der bei Intensivpatienten häufig anzutreffenden Hautreizungen und -rötungen unterschiedlichster Genese zunächst oft verkannt wird.
Blutstrominfektionen (Sepsis) bei immunsupprimierten Patienten. In der Literatur finden sich unterschiedliche Ergebnisse zur Anfälligkeit immunsupprimierter Patienten für Blutstrominfektionen. In einer Studie mit 6.339 Intensivpatienten in Australien waren immunologische Störungen und ein Zustand nach Malignomen mit einem um drei bis vier Prozent erhöhten Risiko für eine primäre Sepsis assoziiert. Dieser Unterschied zu immungesunden Patienten erreichte jeweils Signifikanz (p = 0,02 oder 0,04).
Das Erregerspektrum scheint jedoch wie bei primär Immungesunden von Koagulase-negativen Staphylokokken und Staphylococcus-aureus-Stämmen dominiert zu sein. Seltener wurden gramnegative Stäbchenbakterien und Pilze isoliert. Das Mortalitätsrisiko bei einer einmal aufgetretenen Sepsis war jedoch in mehreren hierzu publizierten Studien signifikant um den Faktor 1,4 bis 3,2 erhöht.
Besteht bei der Diagnostik durch Blutkulturen kein Unterschied zu immungesunden Patienten, so ist bei der empirischen Initialtherapie immunsupprimierter Patienten zu berücksichtigen, wie lange und wie oft die Patienten bereits in anderen Abteilungen des Krankenhauses (oder anderswo) waren und ob dort gegebenenfalls bereits multiresistente Erreger nachgewiesen wurden. Sind längere Voraufenthalte auf Stationen mit multiresistenten Erregern bekannt, sollte die Primärtherapie moderne Breitspektrum-β-Laktame mit einem erweiterten Wirkungsspektrum gegen solche Erreger umfassen.
Eine primäre Kombinationstherapie mit einem Aminoglykosid ist ebenfalls denkbar, sollte aber nur so lange erfolgen, bis die Ergebnisse der Blutkultur und der Antibiotikaresistenzbestimmung vorliegen und die Notwendigkeit einer solchen Therapie rechtfertigen. Andernfalls sind Aminoglykoside so schnell wie möglich abzusetzen.
Hefepilze und Aspergillen. Für Patienten mit einer Neutropenie von mehr als sieben Tagen ist bei erneutem Fieber wegen der möglichen Beteiligung einer Pilzinfektion oder Fungämie anzuraten, ein Antimykotikum in das Therapieschema aufzunehmen. Die Studienautoren empfehlen dafür in erster Linie ein Echinocandin (zum Beispiel Anidulafungin, Caspofungin). Sofern kein septischer Schock zum sofortigen Beginn einer solchen antimykotischen Therapie zwingt, ist jedoch das Ergebnis des (1–3)-β-D-Glucan-Tests im Serum abzuwarten.
Dieser Test weist einen Bestandteil der Zellmembran verschiedener medizinisch relevanter Pilzarten nach, zum Beispiel Candida spp., Aspergillus spp. und Pneumocystis jirovecii. Ein positives Ergebnis beweist jedoch nur das Vorhandensein solcher Pilzbestandteile im Serum. Bei der Interpretation ist zu bedenken, dass auch chirurgische Schwämme (wie sie zum Aufsaugen von Blut bei großen Operationen dienen) oder Dialysemembranen ähnliche Moleküle enthalten. Nach größeren chirurgischen Eingriffen oder nach Dialyse können daher falsch-positive Ergebnisse des (1–3)-β-D-Glucan-Tests auftreten.
Das Testergebnis ist somit immer im klinischen Kontext zu bewerten. Ein negatives Testergebnis schließt zudem eine systemische Pilzinfektion nicht aus, da die Konzentration des β-D-Glucans zu Beginn einer Pilzsepsis noch zu gering sein kann. Eine Wiederholung des Tests nach zwei bis drei Tagen ist bei fortbestehendem Verdacht angezeigt.
Beatmungsassoziierte Pneumonien. Entgegen den Erwartungen wiesen mehrere von den Autoren gefundene Studien nach, dass die Inzidenz beatmungsassoziierter Pneumonien bei immunsupprimierten Patienten signifikant niedriger war als bei immungesunden Intensivpatienten.
So zeigte eine Studie an 2.960 Intensivpatienten von 114 Intensivstationen, dass immunsupprimierte Patienten (n = 662) nach 28 Tagen Intensivpflege eine Pneumonierate von 16,6 Prozent, immungesunde Patienten hingegen eine Pneumonierate von 24,2 Prozent aufwiesen. Ähnliches galt für die beatmungsassoziierte Tracheobronchitis. Auch Studien an intensivmedizinisch behandelten Patienten nach Leber- oder Lungentransplantation zeigten diesen Unterschied.
Eine Erklärung dafür könnte sein, dass Patienten während einer ärztlich geplanten Immunsuppression eine sehr breit wirksame Antibiotika- und Antimykotikaprophylaxe erhalten, die einen Schutz gegen nosokomiale Erreger auf der Intensivstation bietet. Darüber hinaus werden Patienten mit hohem Infektionsrisiko in der Regel in einer Schutzisolierung mit Kittel-Handschuh-Pflege behandelt.
Breite Differenzialdiagnose von Beatmungspneumonien. Die Diagnostik der beatmungsassoziierten Pneumonie unterscheidet sich nicht von der Diagnostik immungesunder Beatmungspatienten. Ob eine Polymerase-Kettenreaktion (Multiplex-PCR) zum Nachweis der wichtigsten Erreger nosokomialer Pneumonien die Diagnostik wesentlich beschleunigen kann, ist unter Expertinnen und Experten noch umstritten. Das Spektrum der in Betracht zu ziehenden Differenzialdiagnosen einer Pneumonie unter Immunsuppression ist jedoch deutlich breiter. Zu denken ist an Lungenmetastasen, Flüssigkeitsüberladung, intraalveoläre Blutungen bei Gerinnungsstörungen und reaktivierte Virusinfektionen.
Ein besonderes diagnostisches Problem stellt die Früherkennung einer pulmonalen Aspergillus-Infektion bei immunsupprimierten Patienten dar. Aspergillen sind ubiquitär in der Umwelt vorkommende Schimmelpilze, die über die Atemwege in die Lunge eindringen können. Für immungesunde Personen ist die inhalative Aufnahme relativ unbedenklich, da Phagozyten in der Lage sind, geringe Mengen dieser Schimmelpilze aufzunehmen und abzutöten. Bei immungeschwächten Patienten mit gestörter Phagozytosefunktion kann es dagegen zu einer invasiven pulmonalen Aspergillose (IPA) mit hohem Sterberisiko kommen.
Diagnostik der invasiven pulmonalen Aspergillose (IPA). Die IPA ist klinisch gekennzeichnet durch persistierendes Fieber trotz breiter antibiotischer Therapie sowie durch beidseitige pulmonale Infiltrate im Thoraxröntgenbild und in der Computertomografie. Die radiologische Diagnostik zeigt in typischen Fällen ein sogenanntes Halozeichen. Hierbei handelt es sich um halbmondförmige Lufteinschlüsse über untergegangenem Lungengewebe.
Labordiagnostisch hat der kulturelle Nachweis von Aspergillen aus bronchoalveolärer Lavageflüssigkeit eine Sensitivität von circa 58 Prozent im Vergleich zum histologischen Nachweis einer IPA, der als Goldstandard gilt. Die kulturelle Diagnostik allein ist daher nicht ausreichend.
Weitere Infektionen. Die Studienautoren weisen darauf hin, dass viele latent im Körper der Patienten vorhandene Viren unter Immunsuppression wieder aktiv werden können. Bei entsprechenden Hautveränderungen ist an einen Herpes zoster (Varizella-Zoster-Virus, VZV) zu denken, bei Haut- und Genitalveränderungen sowie Enzephalitiden an das Herpes-simplex-Virus (HSV). Das Cytomegalovirus (CMV) kann systemische Infektionen mit vielfältigen Manifestationen wie Ösophagitis, Gastritis, Retinitis, Enzephalitis und Pneumonie verursachen. Bei all diesen Infektionen ist die PCR aus entsprechenden Flüssigkeiten wie Pustelinhalt oder Liquor sehr aussagekräftig.
Obwohl schwere COVID-19-Verläufe eher selten geworden sind, ist bei nachgewiesener COVID-19-Pneumonie auch an eine begleitende pulmonale Aspergillose zu denken. Die IPA-Diagnostik sollte dann wie zuvor beschrieben erfolgen.
Große Herausforderungen
Die Behandlung von Infektionen bei immungeschwächten Patienten stellt das Gesundheitssystem vor große Herausforderungen. Längst reicht es nicht mehr aus, sich nur auf die akute Behandlung dieser Infektionen zu konzentrieren. Gerade bei immungeschwächten Patienten muss der Fokus verstärkt auf die Prävention gelegt werden, um lebensbedrohliche Infektionen bereits im Vorfeld zu verhindern.
Prophylaktische Maßnahmen müssen breit gefächert und auf das individuelle Risiko jedes Patienten abgestimmt sein. Dies reicht vom gezielten Einsatz von Impfstoffen über die Vermeidung nosokomialer Infektionen bis hin zur regelmäßigen Überwachung latenter Infektionen, die durch Immunsuppression reaktiviert werden können.
Darüber hinaus erfordert die Prävention einen umfassenden Ansatz, der neben dem medizinischen Personal auch das Pflegepersonal, die Hygieneteams und die Patienten selbst einbezieht. Dies lässt sich mit verbesserten Schulungsmaßnahmen, strengeren Hygienestandards und dem gezielten Einsatz antimikrobieller Prophylaxen erreichen.
Ein weiterer wichtiger Baustein ist die Früherkennung von Infektionsrisiken mithilfe moderner diagnostischer Methoden, um rechtzeitig eingreifen zu können, bevor sich eine Infektion ausbreitet. Angesichts der steigenden Zahl immungeschwächter und älterer Patienten ist es unerlässlich, dass das Gesundheitssystem diesen präventiven Ansatz stärker in den Vordergrund rückt. Nur so sind langfristig bessere Behandlungsergebnisse zu erzielen und lässt sich die hohe Belastung der Gesundheitssysteme infolge vermeidbarer Infektionen reduzieren.
Eine schnelle und präzise Diagnose ist bei immunsupprimierten Patienten von größter Bedeutung, da ihr geschwächtes Immunsystem oft nicht in der Lage ist, Infektionen wirksam abzuwehren. Verspätete oder ungenaue Diagnosen können bei dieser besonders gefährdeten Patientengruppe schnell fatale Folgen haben, wie die rasche Entwicklung einer Sepsis oder anderer schwerwiegender Komplikationen wie Multiorganversagen.
Moderne diagnostische Methoden, insbesondere PCR-basierte Techniken, spielen dabei eine zentrale Rolle. Sie ermöglichen eine schnelle und präzise Identifizierung von Bakterien, Viren oder Pilzen, oft noch bevor klinische Symptome auftreten. Diese Methoden verbessern die Behandlungsmöglichkeiten erheblich, indem sie die gezielte Einleitung einer geeigneten Therapie ohne Zeitverlust ermöglichen. Vor allem aber lässt sich die Therapie individuell auf den Patienten abstimmen.
Immunsupprimierte Patienten weisen häufig komplexe Krankheitsbilder auf, bei denen eine Standardtherapie nicht ausreicht. Faktoren wie bestehende Vorerkrankungen, der Grad der Immunsuppression und mögliche Wechselwirkungen mit anderen Medikamenten sind bei der Therapieplanung zu berücksichtigen. Darüber hinaus können bestimmte Krankheitserreger wie Pilze oder Viren, die unter Immunsuppression reaktiviert werden, spezielle Behandlungsansätze erfordern.
Eine solche personalisierte Therapie erfordert eine enge interdisziplinäre Zusammenarbeit von Intensivmedizinerinnen und -medizinern, Infektiologinnen und Infektiologen, Mikrobiologinnen und -biologen, Immunologinnen und Immunologen sowie spezialisiertem Pflegefachpersonal, damit die Behandlung nicht nur wirksam, sondern auch sicher und gut verträglich ist. Letztlich ist es das Zusammenspiel von schneller Diagnostik und maßgeschneiderter Therapie, das die Prognose immunsupprimierter Patienten deutlich verbessern kann.
[1] Kreitmann L et al. ICU-acquired infections in immunocompromised patients. Intensive Care Med 2024; 50: 332–349. doi: 10.1007/s00134–023–07295–2