Seit über 50 Jahren kommt der sogenannte Swan-Ganz-Katheter in der Intensivmedizin für das erweiterte hämodynamische Monitoring zum Einsatz. Die Autoren beschreiben die besonderen pflegerischen Aspekte und geben einen kurzen Überblick zu weniger invasiven Alternativen.
Die präzise Überwachung und Steuerung der Herz-Kreislauf-Funktionen schwerstkranker Patientinnen und Patienten (im Folgenden: Patienten) war schon immer von vitaler Bedeutung – insbesondere in der Intensivmedizin und in der Anästhesie. Ende der 1960er-Jahre entwickelten die amerikanischen Kardiologen Harold J. Swan und William Ganz eine neue Methode zum hämodynamischen Monitoring – den Swan-Ganz-Katheter (SGK) [1]. Mittlerweile existieren viele synonyme Begriffe, wie „Pulmonaliskatheter/Pulmonalarterienkatheter“ [2, 3], „PA-Katheter“, „Einschwemmkatheter“ [4] oder „PAK/PAC“ [2, 3].
Funktionsprinzip des Swan-Ganz-Katheters
Ursprünglich handelte es sich um einen zweilumigen [1], heute oft vier- oder fünflumigen Venenkatheter mit einem kleinen aufblasbaren Ballon kurz hinter der distalen Katheterspitze (Abb. 1) [5]. Diese lässt sich mithilfe einer venösen Schleuse, z. B. über die V. Jugularis, durch die obere Hohlvene in den rechten Vorhof vorschieben. Dort wird der Ballon aufgeblasen und schwimmt dann, während der SGK weiter vorgeschoben wird, mit dem Blutstrom durch den rechten Ventrikel bis in die Pulmonalarterie. Von dort aus mit dem Blutstrom weiter in die kleineren Pulmonalarterien – daher der synonym verwendete Begriff „Einschwemmkatheter“ [5, 6]. Werden die Lungenarterien im Durchmesser so klein, dass der aufgeblasene Ballon sie verschließt, ist über die Katheterspitze der „lungenkapilläre Verschlussdruck“ („Wedge-Druck“, pulmonary capillary wedge pressure, PCWP) zu messen. Dieser gibt einen Einblick in die Druckverhältnisse im Lungenkreislauf und somit über die Vorlast des linken Ventrikels [6].
Zusätzlich lässt sich mittels der Thermodilutionsmethode das Herzzeitvolumen (HZV) als Maß für die Pumpleistung des Herzens bestimmen. Hierzu ist eine definierte Menge kalter Flüssigkeit, üblicherweise physiologische Kochsalzlösung, mindestens in Raumtemperatur über die proximale Öffnung des SGK in den rechten Vorhof einzubringen. Direkt mit der Injektion dieser Lösung wird bereits die Temperatur derselben ermittelt. Ein weiterer am distalen Katheterende platzierter Temperatursensor bestimmt dann die Zeitdauer des Temperaturabfalls von der aktuellen Körpertemperatur bis zur Temperaturnormalisierung in der Blutbahn. Aus dem Zusammenspiel all dieser Faktoren errechnet sich das HZV [6, 7]. Ein spezieller, mit Elektroden besetzter SGK ist zusätzlich für ein intrakardiales Pacing einsetzbar [8]. Mittels einer Röntgenaufnahme lässt sich nach Anlage des SGK dessen korrekte Position sicherstellen [5].
Indikation, Kontraindikation und Komplikationen
Der SGK hat aufgrund seiner spezifischen Einsatzmöglichkeiten eine wichtige Funktion im hämodynamischen Monitoring der Intensivmedizin [9]. Tabelle 1 stellt eine Übersicht der wichtigsten Vitalparameter dar [6, 7] – die Normwerte sind in der Literatur unterschiedlich angegeben und daher innerhalb einer Einrichtung individuell festzulegen.
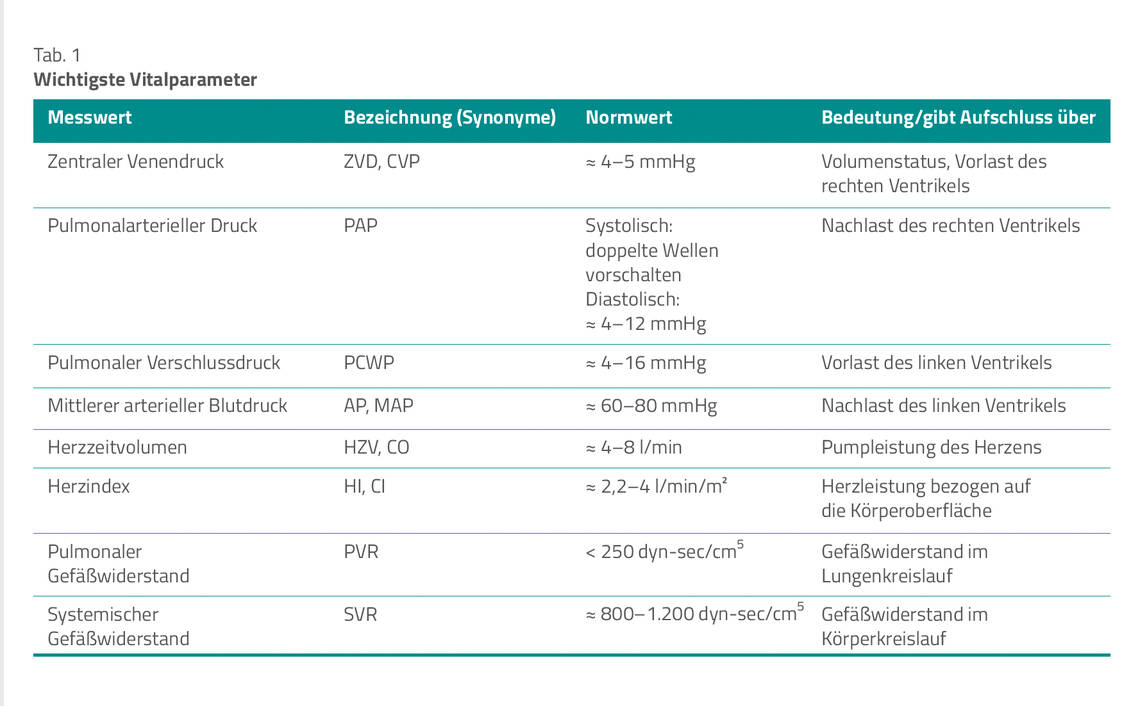
Diese Übersicht der relevanten Parameter ermöglicht eine sehr gezielte Therapieentscheidung, u. a.:
- die Verabreichung von kreislaufwirksamen Substanzen adaptiert an die aktuelle hämodynamische Situation [6],
- die Therapie mit inhalativem Stickstoffmonoxid (iNO) unter maschineller Beatmung [10],
- die Verringerung der linksventrikulären Nachlast durch Antihypertensiva oder die gezielte Anpassung des Volumenstatus.
Der Einsatz des SGK ist hingegen infrage zu stellen bzw. kontraindiziert bei
- ausgeprägter Insuffizienz der Trikuspidalklappe [11] oder nach deren operativer Rekonstruktion,
- Einsatz eines mechanischen Ersatzes der Trikuspidalklappe oder der Pulmonalklappe [6, 7],
- Vorhandensein eines Tumors im rechten Herzen [6, 7] oder
- einer stark ausgeprägten Aortenklappenstenose [6, 7].
Neben den klassischen Herausforderungen bei der Anlage venöser Katheter, z. B. Infektionen, zählen zu den Komplikationen des SGK u. a. Arrhythmien, Knotenbildungen, Schädigungen der Herzklappen, pulmonale Infarkte oder Thrombosen und Ruptur der Pulmonalarterie [12, 13].
Zum Einsatz des SGK liegen heterogene Studienergebnisse vor. So hatte z. B. ein Cochrane Review von 2013 u. a. zum Ziel, die Bedeutung der Wirksamkeit des SGK für Sterblichkeit, (intensiv)stationäre Aufenthaltsdauer sowie die Kosten bei erwachsenen Intensivpatienten zu identifizieren [8]. Die Autorenschaft schlussfolgerte, dass der Einsatz eines SGK diese Faktoren nicht veränderte [8].
In der aktuellen „S3-Leitlinie zur intensivmedizinischen Versorgung herzchirurgischer Patienten – Hämodynamisches Monitoring und Herz-Kreislauf“ fasst die Autorenschaft als Kernempfehlung zusammen, den SGK „[...] bei Patienten mit präoperativer Rechtsherzdysfunktion, Risiko für Rechtsherzdysfunktion und/oder pulmonal-arterieller Hypertonie und zur Differenzierung der Ursache und Steue rung der Therapie eines schweren [...]“ kardiogenen Schocks mit Low-Outpout-Syndrom (LCOS) einzusetzen [14].
Pflegerische Versorgung
Für die pflegerische Versorgung von Patienten mit einem SGK sind eine entsprechend intensive Schulung sowie praxisnahe Begleitung und Einarbeitung obligat [2, 8]. Dazu gehören neben der allgemeinen Überwachung des Monitorings auch die
- Vorbereitung und Assistenz bei der Anlage des SGK [15],
- Medikamentengabe über den SGK (Cave: Über den PAP-Schenkel dürfen mit wenigen Ausnahmen keine Medikamente verabreicht werden!),
- Verbandswechsel mit Kontrolle der Einstichstelle nach Infektionszeichen – nach Möglichkeit sind Folienverbände einzusetzen, sofern keine Kontraindikationen bestehen [16],
- Polsterung des Katheters und der Schleuse, um Dekubitus zu vermeiden [17],
- Fixierung des Katheters, um ein intrapulmonales Verrutschen zu verhindern,
- Abnahme von gemischtvenösem Blut zur Bestimmung des Sauerstoffpartialdrucks in der Blutgasanalyse über den PAP-Schenkel (Cave: Z. B. beim Rechts-Links-Shunt können falsche Ergebnisse entstehen) [12, 18],
- Kontrolle des Ballons – dieser ist nach der Messung zu entblocken und entsprechend zu sichern [5, 12],
- Dokumentation der ermittelten Werte,
- Infusionssystemwechsel [16],
- Beratung des Patienten, um Komplikationen zu vermeiden,
- Beratung Angehöriger zu spezifischen Fragen zum SGK in Abstimmung mit dem ärztlichen Dienst.
Patienten mit einem SGK dürfen bei stabiler Hämodynamik, sofern es keine weiteren Kontraindikationen gibt, aktiv mobilisiert werden [19, 20].
Dabei sind Komplikationen wie Arrhythmien oder ein intrapulmonales Verrutschen des Katheters möglich, mit einer guten Vorbereitung aber vermeidbar [19]. Dazu gehören z. B. der Einsatz standardisierter Protokolle und ein geschultes multiprofessionelles Team [20].
Alternative Möglichkeiten
Weitere Möglichkeiten des hämodynamischen Monitorings bieten neuere und weniger invasive Verfahren. Dazu gehört z. B. die arterielle Pulskonturanalyse via PiCCO, PulseCO und FloTrac/Vigileo [9, 21]. Für den Einsatz ist ein arterieller Katheter notwendig, der dann die Blutdruckkurve neben dem klassischen Kreislaufmonitoring auch auf das erweiterte hämodynamische Monitoring spiegelt.
Eine vergleichende Untersuchung dieser weniger invasiven Methodik zeigte bei erfolgreich reanimierten Patienten häufig eine Übereinstimmung der ermittelten Werte [22]. Andere Autoren verglichen u. a. den SGK mit dem FloTrac/Vigileo bei kardiochirurgischen Patienten. Die Ergebnisse waren heterogen.
Die Autorenschaft schlussfolgerte, dass bei der Interpretation der Werte eines isolierten Systems Vorsicht geboten ist [23].
In der genannten S3-Leitlinie zur intensivmedizinischen Versorgung herzchirurgischer Patienten fasste die Autorenschaft als Konsens zusammen, dass „die kalibrierte Pulskonturanalyse bei postoperativen kardiochirurgischen Patienten […] zum erweiterten hämodynamischen Monitoring eingesetzt werden [kann]“ [14].
Bereits vor einigen Jahren haben Janssens und Graf [24] aufgezeigt, dass der Einsatz eines SGK in der Intensivmedizin fortlaufend auch kritisch diskutiert wird. Das gilt bis heute.
Fazit
Der SGK stellt auch über 50 Jahre nach seiner Vorstellung einen wichtigen Baustein in der intensivmedizinischen Versorgung dar. Der ärztliche Dienst muss entsprechend abwägen, ob ein Einsatz der invasiven Messmethodik erfolgt oder alternative Möglichkeiten anzuwenden sind.
Pflegende haben in dem Zusammenhang eine wichtige Aufgabe in der direkten Versorgung der Patienten. Sie unterstützen nicht nur bei der Anlage des Katheters, sondern gestalten maßgeblich den weiteren Ablauf der Versorgung im multiprofessionellen Team. Dazu sind spezifische Kenntnisse besonders wichtig. Daher ist das Verfahren, sofern es in Kliniken zum Einsatz kommt, unbedingt in Einarbeitungsprozesse auf der Intensivstation zu integrieren [8]. Flankierende Schulungsmaßnahmen wie (Kurz-)Fortbildungen, Workshops und der unterstützende Einsatz von One Minute Wonder (OMW) [25] können den Theorie-Praxis-Transfer maßgeblich unterstützen.
Die Autorenschaft erklärt, dass keine Interessenkonflikte bestehen.
[1] Swan HJ et al. Catheterization of the heart in man with use of a flow-directed balloon-tipped catheter. N Engl J Med 1970; 283 (9): 447–451
[2] Cisar NS et al. Changing the Environment of Care for Patients With a Pulmonary Artery Catheter. Critical Care Nurse 2010; 30 (2): 34–44
[3] Kerscher C et al. Spezielle Aspekte der intensivmedizinischen Therapie nach herzchirurgischen Eingriffen. Intensivmedizin up2date 2013; 10 (01): 73–96
[4] Striebel HW. Operative Intensivmedizin. Sicherheit in der klinischen Praxis. Vol. 2. Schattauer; 2015
[5] Er F, Erdmann E. The pulmonary artery catheter. Dtsch Med Wochenschr 2009; 134 (15): 753–756
[6] Hansen M. Invasive and minimally invasive hemodynamic monitoring. Anasthesiol Intensivmed Notfallmed Schmerzther 2016; 51 (10): 616–625
[7] Gassanov N et al. Hemodynamic monitoring in the intensive care unit: pulmonary artery catheter versus PiCCO. Dtsch Med Wochenschr 2011; 136 (8): 376–380
[8] Rajaram SS et al. Pulmonary artery catheters for adult patients in intensive care. Cochrane Database Syst Rev 2013 (2): CD003408
[9] Janssens U et al. Empfehlungen zum hämodynamischen Monitoring in der internistischen Intensivmedizin. Der Kardiologe 2016; 10 (3): 149–169
[10] Mannebach T, Wiegmann K, Krüger L. Zusätzliche Unterstützung. Beatmung mit Stickstoffmonoxid. PflegenIntensiv 2021; 18 (4): 56–61
[11] Reuter DA, Goetz AE. Measurement of cardiac output. Anaesthesist 2005; 54 (11): 1135–1151; quiz 1152–1153
[12] de Waal EE, de Rossi L, Buhre W. Pulmonary artery catheter in anaesthesiology and intensive care medicine. Anaesthesist 2006; 55 (6): 713–728; quiz 729–730
[13] Schweitzer C. Neue Kraft für ein krankes Herz. intensiv 2020; 28 (03): 144–155
[14] Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF). S3-Leitlinie zur intensivmedizinischen Versorgung herzchirurgischer Patienten. Hämodynamisches Monitoring und Herz-Kreislauf. (AWMF Register 001/016); 2017
[15] Feldker W, Hilscher G. Der Swan-Ganz-Katheter. Pflegerische Aufgaben beim Legen des Katheters und Überwachen der Patienten. Deutsche Krankenpflegezeitschrift 1991; 44 (2): 86–89
[16] Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO). Prävention von Infektionen, die von Gefäßkathetern ausgehen. Teil 1 – Nichtgetunnelte zentralvenöse Katheter Empfehlung der KRINKO beim Robert Koch-Institut. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz 2017a; 60 (2): 171–206
[17] Deutsches Netzwerk für Qualitätsentwicklung in der Pflege (DNQP). Expertenstandard Dekubitusprophylaxe in der Pflege. Vol. 2. Osnabrück: Schriftreihe des DNQP; 2017
[18] Renner M. Die Blutgasanalyse (BGA) – Teil 1. intensiv 2009; 17 (04): 204–207
[19] Mattioli E et al. Safety and Patients‘ Response to Ambulation with a Pulmonary Artery Catheter in the Cardiac Intensive Care Unit. American Journal of Critical Care 2019; 28 (2): 101–108
[20] Sharma S et al. Safety First: An Ambulation Protocol for Patients With Pulmonary Artery Catheters. Crit Care Nurse 2021; 41 (1): 45–52
[21] Rozental O et al. To Swan or Not to Swan: Indications, Alternatives, and Future Directions. Journal of Cardiothoracic and Vascular Anesthesia 2021; 35 (2): 600–615
[22] Staer-Jensen H et al. Comparison of three haemodynamic monitoring methods in comatose post cardiac arrest patients. Scand Cardiovasc J 2018; 52 (3): 141–148
[23] Power P et al. Comparison of pulmonary artery catheter, echocardiography, and arterial waveform analysis monitoring in predicting the hemodynamic state during and after cardiac surgery. Int J Crit Illn Inj Sci 2017; 7 (3): 156–162
[24] Janssens U, Graf J. Der Pulmonalarterienkatheter in der Intensivmedizin. Intensivmedizin und Notfallmedizin 2007; 44 (5): 312–322
[25] Krüger L et al. One Minute Wonder – Fortbildung während der Arbeitszeit. HeilberufeScience 2021; 12 (1–2): 22–29








