Das Elektroenzephalogramm (EEG) ist eine bewährte und valide Methode der „Bildgebung“ des Gehirns. Doch es gilt als störanfällig und erlaubt keine unmittelbaren anatomischen Schlussfolgerungen. Hat es sich in der medizinischen Diagnostik zur Delir- und Enzephalopathie-Erkennung bisher nicht durchgesetzt, kann sich das nun durch bettseitige Anwendungen ändern. Routinemäßig wird das EEG in der Neurologie, in der Schlafmedizin und zur Hirntoddiagnostik eingesetzt.
Das Elektroenzephalogramm (EEG) hat sich nicht so flächendeckend durchgesetzt wie das Elektrokardiogramm (EKG). Auch Magnetresonanztomografen (MRT) und Computertomografen (CT) sind meist flächendeckend vorhanden. Dies vereinfacht eine Zuordnung von klinischen Symptomen zu anatomischen Strukturen. Zudem ist das EEG-Signal schwierig zu interpretieren, und die bisher komplexe Ableitungsmethode (10-20) ist störanfällig. Aufgezeichnet wird das EEG mit einem Analog-Digital-Wandler im Bereich zwischen 10 und 50 Mikrovolt (µV) – wohingegen ein EKG-Ausschlag wenige Millivolt (mV) aufweist.
Auch lassen sich nicht alle Potenziale, die an der kortikalen Oberfläche aufgezeichnet werden, über die Kopfhaut nachweisen. Potenziale aus der Großhirnrinde werden durch darüberliegende Strukturen wie die Pia und Dura mater, den Liquor und die Kopfhaut abgeschwächt. Es ist daher fast nicht möglich, von dem EEG direkte anatomische Schlussfolgerungen zu ziehen oder eine exakte Zuordnung zu den jeweiligen Arealen im Gehirn zu treffen. Für die Interpretation ist es wichtig zu wissen, dass verschiedene Krankheiten und Zustände ähnliche Veränderungen im EEG hervorrufen können. Es ist daher stets zu beachten, dass sich jede Interpretation des EEG immer an der individuellen Situation der Patientin oder des Patienten (im Folgenden: Patient) orientieren muss.
Grundprinzip EEG-Positionierung
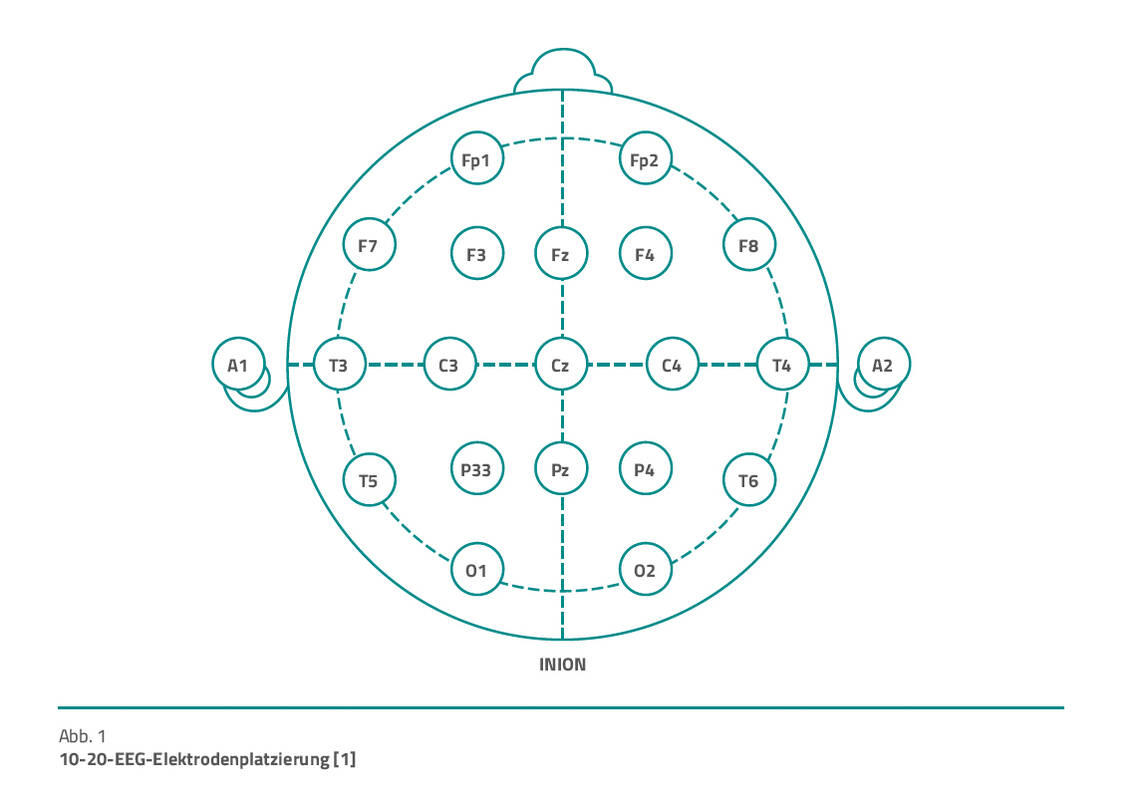
Analog dem EKG haben die Elektroden eine feste Zuordnung und Position, hier aber auf der Kopfhaut, um verschiedene EEG-Bilder miteinander vergleichen zu können. Bezeichnung und Positionierung erfolgten bislang nach dem 10-20-System (Abb. 1) [1]. Seit den 1950er-Jahren ist dieses das Standardsystem, das immer wieder Modifikationen erfahren hat. Das 10-20-System bietet den Vorteil der einheitlichen Bezeichnung. Buchstaben und Zahlen bilden ein Koordinatenkreuz und beschreiben das jeweilige Areal auf der Kopfhaut. Die fixen Ausgangspunkte sind dabei die Nasion, Inion (Os Occipitale) und der präaurikuläre Punkt. Die Buchstaben stehen für:
- F = frontal
- Fp = frontopolar
- T = temporal
- z = Mittellinie
Beispiel: Fp2 kennzeichnet die Stelle, an der die Elektrode frontopolar rechts (rechte Seite = gerade Zahlen) anzubringen ist. Das Gegenstück ist Fp1 und benennt frontopolar links.
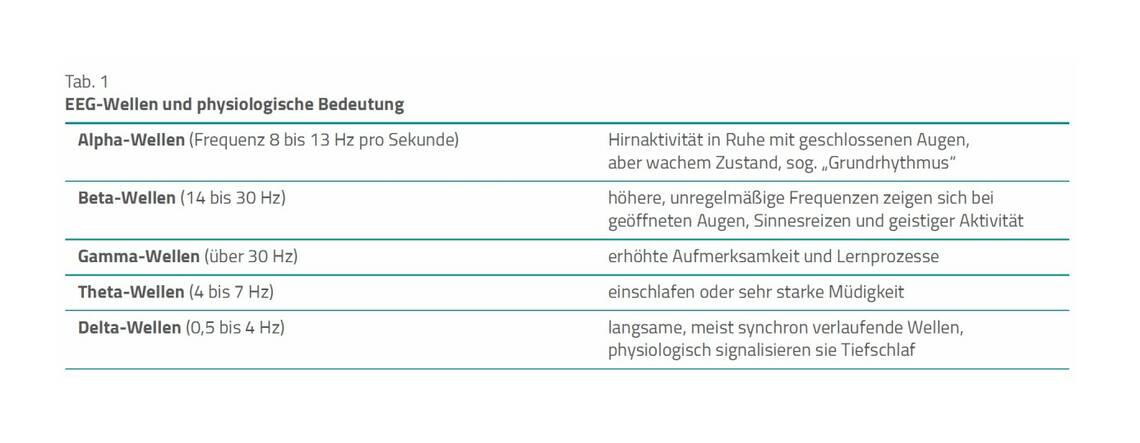
EEG-Analysen ermöglichen die Berechnung der Verteilung der Frequenzbänder in einem bestimmten Zeitrahmen. Am EEG eines gesunden Menschen lassen sich unterschiedliche Frequenzbänder (Tab. 1) beobachten. Im Gegensatz zum EKG sind diese nicht als Zacken, sondern als Wellen abgebildet.
Grundsätzlich ist zwischen generalisierten und fokalen EEG-Veränderungen zu unterscheiden. Fokale EEG-Veränderungen sind auf einen Teilbereich des betroffenen Gehirns zurückzuführen und treten z. B. bei Tumoren oder Blutungen auf. Generalisierte EEG-Veränderungen sind auf einen globalen Einfluss des Gehirns zurückzuführen. Typische Beispiele sind EEG-Veränderungen durch Sedativa, Hypothermie (meist unter 34 °C), Hypoglykämie und globale Hypoxie.
EEG-Anwendung zur Delir- und Enzephalopathie-Erkennung
Wie das Sedierungsregime auf den Intensivstationen unterliegen die neurologische Überwachung und das damit verbundene Monitoring einem stetigen Wandel. Auch hier wurde schon früh versucht, die Sedierungstiefe und das Bewusstsein zu monitoren. Zwei apparative Verfahren seien exemplarisch genannt:
Bispektralindex (BIS). BIS™ ist ein eingetragener Markenname der Firma Aspect Medical Systems, wurde 1994 eingeführt [2] und 2003 in den USA zugelassen. Die Idee der Messung der Narkosestadien besteht seit der Einführung der „Güdel-Stadien“ [3]. Dennoch ist die Erfassung dieser Parameter sehr subjektiv [4]. Größter Risikofaktor einer Fehlinterpretation klinischer Parameter ist die neuromuskuläre Blockade, da der Patient sich selbst bei schmerzhaften Stimuli nicht spontan bewegen kann. Diese Parameter unterliegen starken Schwankungen in der Interpretation und sind in ihrer Ausprägung sehr individuell, weshalb der BIS-Monitor zur Überwachung und Verhinderung einer sog. „awareness“ eingesetzt wird.
Das BIS nutzt eine gegenüber dem Standard-EEG reduzierte Kanalzahl. Herrschen im Wachzustand eines Erwachsenen Alpha- und Beta-Aktivitäten vor, so ändert sich dies infolge Sedierung und Anästhesie. Eine zunehmende Narkosetiefe führt zur Frequenzabnahme und zum Auftreten von Theta-Wellen. Im weiteren Verlauf zeigt sich ein langsamer Delta-Rhythmus. Parallel steigen die Amplituden im EEG an. Diese Roh-EEG-Messungen transferiert das BIS-System in einen Punktewert (Zahl) zwischen 0 und 100 auf den Monitor:
- 0 = isoelektrisches EEG
- 20 = Burst Suppression
- 40 = tiefe Bewusstlosigkeit/Vollnarkose
- 60 = mittlere Sedierungstiefe
- 80–100 = erweckbar bis wach
Narcotrend. Die Grundidee des Narcotrend-Monitorings wurde während der EXPO 2000 in Hannover erstmals vorgestellt. Der neuroprotektive Ansatz stellt die Messung der Sedierungs- bzw. Narkosetiefe in den Vordergrund. Für eine Standardmessung werden drei Elektroden auf der Stirn des Patienten befestigt und mit dem Narcotrend verbunden. Anschließend erfolgen eine Verstärkung und Digitalisierung der EEG-Signale und eine Umrechnung in ein Scoresystem. Basierend auf unterschiedlich abgeleiteten EEG-Parametern nimmt Narcotrend mithilfe eines Algorithmus eine automatische Klassifikation des EEG auf einer Skala von A (wach) bis F (sehr tiefe Hypnose) vor. Diese Stadieneinteilung lässt sich anhand eines EEG-Index (100 = wach, 0 = sehr tiefe Hypnose) zusätzlich verfeinern. Diese Steuerung dient neben der Vermeidung einer zu tiefen Sedierung auch der Steuerung in der Anästhesieausleitung und kann so zu verkürzten Aufwachzeiten beitragen [6].
Beide exemplarisch genannten Verfahren dienen in erster Linie dem objektiven Messen der Sedierungs- bzw. Narkosetiefe und sollten damit die vorher gängige subjektive Einschätzung durch Vitalparameter sinnvoll ergänzen. Sie eignen sich aber nicht oder nur sehr bedingt in der Prognose, der Diagnose und dem Monitoring kognitiver Störungen wie dem Delirium. Interessant ist in diesem Zusammenhang, dass innerhalb der Berufsgruppen Geriatrie, Psychiatrie, Anästhesie und Intensivmedizin der Begriff „Delirium“ bevorzugt, in der Neurologie und Neurointensivmedizin die gleiche Entität hingegen eher als (akute) „Enzephalopathie“ bezeichnet wird. Die uneinheitliche Terminologie hat sich negativ auf klinische Praxis und Forschung, im Sinne einer fast vollständigen Trennung von Delirium und Enzephalopathie, ausgewirkt.
Diese Probleme veranlassten eine interdisziplinäre Gruppe zu einer Konsenserklärung zur Nomenklatur, die zehn große Fachgesellschaften unterstützt haben [7]. Tatsächlich bedarf es einer Unterscheidung und Trennung des pathologischen Zustands des Gehirns, der Enzephalopathie, von den manifesten klinischen Merkmalen, genannt Delirium. Eine akute Enzephalopathie ist kein klinisches Syndrom (im Gegensatz zum Delirium), sondern ein sich schnell entwickelnder (meist innerhalb von Stunden bis wenigen Tagen), diffuser pathobiologischer Prozess, der sich allerdings als Delirium oder, in Fällen stark verminderter Bewusstseinslage, als Koma manifestieren kann.
Das typische Delir- und Enzephalopathie-EEG
Zugegeben: Das typische EEG wird es nicht geben und die individuellen Abweichungen sind noch wenig untersucht, aber bei pathologischen Prozessen im Körper, die äußerlich mit einem Delirium oder einer Enzephalopathie einhergehen, finden sich fast immer allgemeine EEG-Verlangsamungen. Diese können grundsätzlich auch bei anderen pathologischen Vorgängen auftreten und sind immer im klinischen Kontext zu betrachten. Diese Verlangsamungen treten auf bei:
- I. erhöhtem intrakraniellen Druck
- II. Intoxikation a. Barbiturat-Koma b. Lithium-Delir c. Clozapin-bedingte Minderung der Vigilanz
- III. Pathologie der hinteren Schädelgrube
- IV. Lewy-Body-Demenz
- V. schwerer Hyperventilation gesunder Personen
Sind dementsprechend eine Medikamenteninteraktion und/oder schwere Müdigkeit bei einem Patienten mit diesen EEG-Veränderungen auszuschließen und maßgeblich Theta- und/oder Delta-Wellen zu sehen, handelt es sich sehr wahrscheinlich um eine Enzephalopathie [8]. Dabei ist zu beachten, dass eine Auswertung des Standard-EEG insbesondere bei Vorliegen einer motorischen Unruhe/Agitation oft nicht eindeutig möglich ist und zudem der Einsatz auf der Intensivstation weiteren Einschränkungen unterliegt. Dennoch ist die größte Aussagekraft bei ruhigen und hypoaktiven Patienten gegeben. Die Beschreibung von Delta-Wellen im Zusammenhang mit einer EEG-Auswertung und dem Symptom Delirium ist dabei grundsätzlich nicht neu, allerdings wurde es vor der Novellierung vieler Delir-Leitlinien 2013 oft noch als organisches Psychosyndrom oder Durchgangssyndrom bezeichnet [5].
Deltascan
Eine Erkennung und v. a. das Monitoring eines Deliriums und/oder einer akuten Enzephalopathie sind in der Praxis auch mit den gängigen Scoresystemen – wie CAM-ICU (Confusion Assessment Method for Intensive Care Unit), ICDSC (Intensive Care Delirium Screening Checklist) oder NuDESC (Nursing Delirium Screening Scale) – schwierig bzw. die Ergebnisse und Interpretationen liegen weit hinter den in Studien erzielten Ergebnissen zurück [9]. So entstand die Idee, eine bettseitige Anwendung auf EEG-Basis hierfür zu entwickeln.
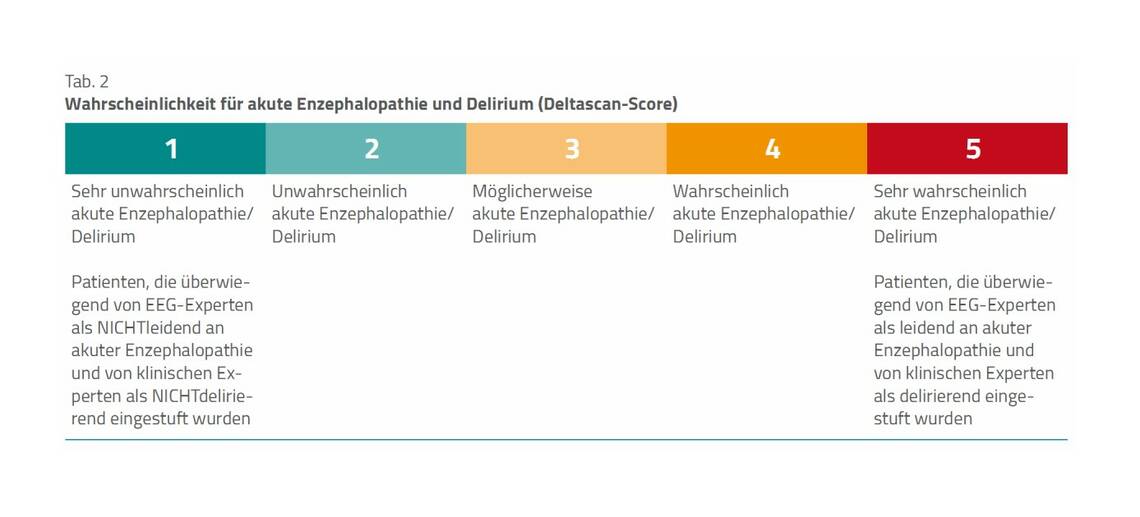
Die Grundlage des im Deltascan verwendeten Algorithmus schuf 2015 eine Arbeitsgruppe um A. J. Slooter [10]. Dabei wurde in einem 1-Kanal-EEG ein mind. 60 Sekunden artefaktfreies EEG auf die relative Delta-Power (1–4 Hz) analysiert. Insbesondere bei älteren Patienten in der postoperativen Phase konnten vielversprechende Ergebnisse erzielt werden [11]. Seit 2019 wird das Ergebnis der Messung nicht mehr dichotomisiert, sondern in einer kontinuierlichen und farblichen Skala angezeigt (Tab. 2). Die Deltascan-Scores 1 und 2 gelten nicht als akute/s Enzephalopathie/Delirium und sind eher physiologisch, die Scores 3, 4 und 5 gelten als akute Enzephalopathie/Delirium unterschiedlicher Schweregrade. Diese Analyse geht über die schon erwähnte Bestimmung der Geschwindigkeiten im EEG hinaus und überprüft dabei das Vorhandensein von sog. polymorphen Delta-Wellen [12]. Die Messung erfolgt mittels Einwegelektrode mit drei Messpunkten.
Der erste Messpunkt wird auf oder nahe Pz (oben am Hinterkopf) angebracht, der zweite auf oder nahe Fp2 (oberhalb der rechten Augenbraue des Patienten), die dritte (Referenz-)Elektrode oberhalb der Nase auf der Stirn. Die EEG-Signale werden dann im Gerät verstärkt, digitalisiert und von den Software-algorithmen so verarbeitet, dass dem Anwender einer der genannten Deltascan-Scores angezeigt wird. Dieser Algorithmus wurde in einer unabhängigen Kohorte von postoperativen Patienten validiert. Erste Hinweise deuten auf eine hohe Spezifität und Sensitivität auch bei Verwendung an Demenzpatienten hin [13]. Der Deltascan kann bisher nicht an Patienten mit tiefer Sedierung (RASS –4 oder –5), bei Patienten unter 18 Jahren und bei Patienten, die mit Lithium oder Clozapinen behandelt werden, zum Einsatz kommen.
Sonstige EEG-Anwendungen bei Delir
Polysomnografie. Eine ebenfalls 1-Kanal-EEG-Anwendung stellt die Polysomnografie dar. Mittels EEG, Elektrookulogramm (EOG) und Elektromyogramm (EMG) wird die Schlafarchitektur erfasst. Die Signale erlauben die Klassifizierung und grafische Darstellung der Schlafstadien. Die Polysomnografie lässt sich mittels respiratorischer und kardialer Parameter zur „Kardiorespiratorischen Polysomnografie“ erweitern [14]. Der Polysomnografie kommt in Bezug auf das Delir eine untergeordnete Rolle und hier nur im Bereich der Prävention zu [15].
Ausschluss Epilepsie. Eine rhythmische epileptische Aktivität im EEG ohne offensichtliche motorische Aktivität wird als non-konvulsiver Anfall definiert, ein wiederholtes oder persistierendes Auftreten wird als ein non-konvulsiver Status Epilepticus bezeichnet [16]. Diese non-konvulsiven epileptische Phasen sind mit ca. 20 % verhältnismäßig häufig bei kritisch kranken Patienten auf der Intensivstation [17] und werden dennoch oft nicht erkannt [18]. Laut deutscher S3- Leitlinie „Analgesie, Sedierung und Delirmanagement in der Intensivmedizin“ (DAS-Leitlinie 2020) soll bei allen Patienten mit unklaren Bewusstseinsstörungen und einem hypoaktivem Delir eine EEG-Diagnostik zum Ausschluss eines non-konvulsiven Anfalls bzw. Status Epilepticus erfolgen (GoR A, LoE ).
Das EEG wird dabei sowohl zur Diagnostik als auch zur Therapiesteuerung eingesetzt. Einige Symptome und Ursachen des non-konvulsiven Status Epilepticus überschneiden sich mit denen des Deliriums. Obwohl non-konvulsive Anfälle mit einer kurzen (<30/40 Minuten) EEG-Aufzeichnung übersehen werden können, ist es dennoch das wichtigste diagnostische Instrument in der Ausschlussdiagnostik!
[1] Rojas GM, Alvarez C, Montoya CE et al. Study of Resting-State Functional Connectivity Networks Using EEG Electrodes Position As Seed. Front Neurosci. 2018 Apr 24; 12: 235. doi: 10.3389/fnins.2018.00235. PMID: 29740268; PMCID: PMC5928390
[2] Sigl JC, Chamoun NG. An introduction to bispectral analysis for the electroencephalogram. J Clin Monitor Comput 1994; 10: 392–404. doi.org/10.1007/BF01618421
[3] Waters R, Guedel AE. Eminent Anesthetists, No. 7. Br J Anaesth. 1952 Oct; 24 (4): 292–299. doi: 10.1093/bja/24.4.292. PMID: 12987541
[4] Hermes C, Kaltwasser A, Dubb R, Rothaug O. Monitoring – mehr als Werte protokollieren. PflegenIntensiv 2011; (2): 1–7
[5] Schmid RG, Tirsch WS. Geschichte des EEG. In: Klinische Elektroenzephalographie des Kindes- und Jugendalters. Berlin, Heidelberg: Springer Verlag; 1995. doi.org/10.1007/978–3–642–79304–2_1
[6] Wilhelm W, Kreuer S, Larsen R; Narcotrend-Studiengruppe. Narcotrend-EEG-Monitoring bei total intravenöser Anästhesie. Klinische Erfahrungen bei 4.630 Patienten [Narcotrend EEG monitoring during total intravenous anaesthesia in 4.630 patients]. Anaesthesist. 2002 Dec; 51 (12): 980–988. German. doi: 10.1007/s00101–002–0417–3. PMID: 12486586
[7] Slooter AJ et al. Updated nomenclature of delirium and acute encephalopathy. Intensive Care Med. 2020; 46: 1020–1022
[8] Hansen HC. Bewusstseinsstörungen und Enzephalopathien. Berlin, Heidelberg: Springer Verlag; 2013
[9] van Eijk MM, van den Boogaard M, van Marum RJ et al. Routine use of the confusion assessment method for the intensive care unit: a multicenter study. Am J Respir Crit Care Med. 2011 Aug 1; 184 (3): 340–344. doi: 10.1164/rccm.201101–0065OC. Epub 2011 May 11. PMID: 21562131
[10] van der Kooi AW, Zaal IJ, Klijn FA et al. Delirium detection using EEG: what and how to measure. Chest. 2015 Jan; 147 (1): 94–101. doi: 10.1378/chest.13–3050. PMID: 25166725
[11] Numan T, van den Boogaard M, Kamper AM et al. Dutch Delirium Detection Study Group. Delirium detection using relative delta power based on 1-minute single-channel EEG: a multicentre study. Br J Anaesth. 2019 Jan; 122 (1): 60–68
[12] Kimchi EY et al. Clinical EEG slowing correlates with delirium severity and predicts poor clinical outcomes. Neurology, 2019; 93 (13): e1260–e1271.
[13] Shinozaki G, Chan A, Sparr N et al. Delirium detection by a novel bispectral EEG device in general hospital. Psychiatry Clin Neurosci. 2018 Sep 24
[14] American Academy of Sleep Medicine. Das AASM-Manual zum Scoring von Schlaf und assoziierten Ereignissen: Regeln, Technologie und technische Spezifikationen. Darmstadt: Steinkopff; 2008
[15] Hermes C, Dewes M, Nydahl P. Leitlinie PADIS – Teil 3. PflegenIntensiv 2019; 16 (1): 16–20
[16] Hirsch LJ, Laroche SM, Gaspard N et al. American clinical neurophysiology society‘s standardized critical care EEG terminology: 2012 version. Journal of Clinical Neurophysiology. 2013
[17] Claassen J et al. Detection of electrographic seizures with continuous EEG monitoring in critically ill patients. Neurology, 2004; 62 (10): 1743–1748
[18] Swisher CB et al. Baseline EEG Pattern on Continuous ICU EEG Monitoring and Incidence of Seizures. J Clin Neurophysiol. 2014
Erklärung zu möglichen Interessenkonflikten: Im Zusammenhang mit diesem Artikel wurden keine Honorare und Aufwandsentschädigungen der genannten Firmen gezahlt. Der Autor erklärt, dass er innerhalb der vergangenen drei Jahre Beratungshonorare und Aufwandsentschädigungen sowie Sachleistungen und Fahrtkosten der Firmen Prolira BV, Orion Pharma GmbH, Atmos Medizintechnik GmbH, Stryker, Hillrom, Arjo, Sedana, Heintel und GWP mbH, erhalten hat. Darüber hinaus hat er Honorare von diversen Bildungseinrichtungen, Akademien und Hochschulen im Gesundheitswesen erhalten.