Bei COVID-19-Patienten scheint es häufiger als bei anderen Intensivpatienten zu nosokomialen Infektionen durch krankenhausspezifische Erreger zu kommen. Wie häufig dies der Fall ist und welche Rolle nosokomiale Infektionen für den Intensivverlauf spielen, wurde kürzlich in einer Studie aus einem Madrider Universitätsklinikum untersucht.
Während ein Teil der betroffenen Patientinnen und Patienten (im Folgenden: Patienten) die COVID-19-Infektion symptomlos übersteht oder nur leichte Symptome entwickelt, erkranken andere Infizierte an schweren respiratorischen Manifestationen. Im Vordergrund steht dabei eine besondere Form der Pneumonie mit typischerweise rasch einsetzender massiver Sauerstoffdiffusionsstörung. Klinisch zeigen sich Atemnot und Hechelatmung, verbunden mit hohem Fieber und Kreislaufsymptomen. Eine Aufnahme auf eine Intensivstation mit nichtinvasiver oder invasiver Beatmung kann erforderlich sein.
Inzwischen ist bekannt, dass bis zu 50 % der auf Intensivstationen behandelten COVID-19-Patienten im weiteren Verlauf der Infektion sterben. Dabei spielt jedoch nicht nur das Virus selbst eine Rolle. Vielmehr scheint es bei den betroffenen Patienten in stärkerem Maße als bei anderen Intensivpatienten zu nosokomialen Infektionen durch krankenhausspezifische Erreger zu kommen. Wie häufig dies der Fall ist und welche Rolle nosokomiale Infektionen für den Intensivverlauf spielen, wurde kürzlich in einer Studie aus einem Madrider Universitätsklinikum untersucht [1].
Die Autorinnen und Autoren (im Folgenden: Autoren) um den Intensivmediziner Dr. Tommaso Bardi schlossen in die Untersuchung alle Patienten ein, die in den Monaten März bis Mai 2020 wegen einer laborbestätigten COVID-19-Infektion auf der Intensivstation des Universitätsklinikums Ramon y Cajal in Madrid/Spanien behandelt wurden. Die Aufnahme der Patienten in die Klinik hatte im März 2020 stattgefunden. Ausgeschlossen wurden COVID-19- Patienten, die aus anderen Kliniken zuverlegt worden waren und dadurch möglicherweise bereits einen nosokomialen Erreger mitbrachten.
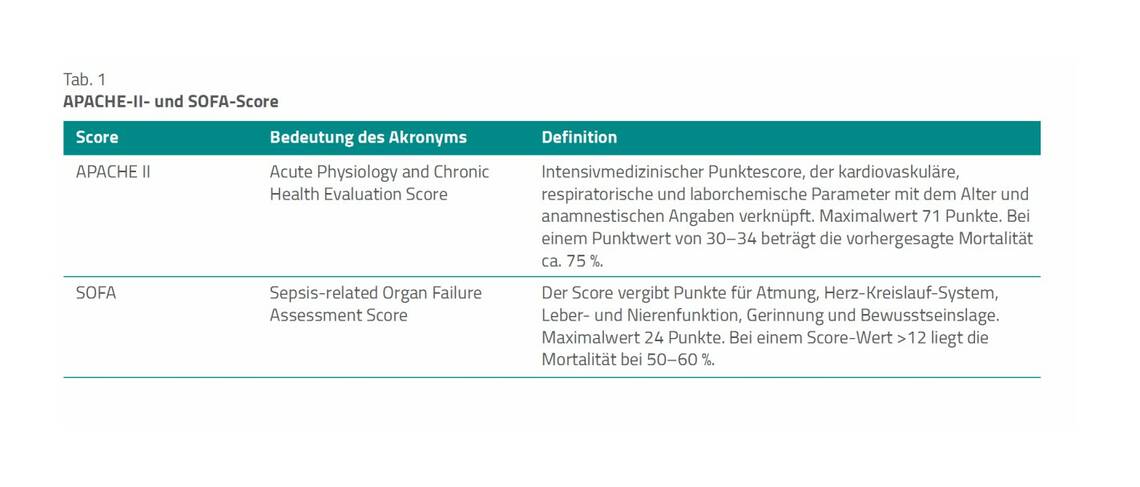
Auf der Intensivstation wurden mikrobiologische Kulturen indikationsbezogen gewonnen, wenn ein konkreter Infektionsverdacht bestand (z. B. Trachealsekret, Blutkultur, Urin). Die Infektionsdiagnosen wurden nach den Kriterien des US-amerikanischen Centers for Disease Control and Prevention (CDC) und nach denjenigen der spanischen Infektiologen-gesellschaft gestellt. Infektionen, die nach 48 Stunden nach Intensivaufnahme auftraten, wurden als nosokomial definiert. Neben den Infektionsdaten wurden für die Studie personenbezogene demografische Daten, medizinische Grund- und Begleiterkrankungen, intensivmedizinische Parameter wie APACHE-II- und SOFA-Score (Tab. 1) sowie der intensivmedizinische Verlauf ausgewertet.
Ergebnisse
Intensivmedizinischer Verlauf. Insgesamt erfüllten 140 Patienten die Einschlusskriterien. Das mittlere Alter der Patienten lag bei 61 Jahren, 77 % der Patienten waren männlich. Ein Bluthochdruck lag bei 42 %, ein Diabetes mellitus bei 20 %, eine koronare Herzkrankheit bei 14 % und eine chronische Nierenerkrankung bei 6 % als Grundkrankheiten vor. Im Mittel kam es 4 (1–6) Tage nach der Krankenhausaufnahme zu einer Übernahme auf die Intensivstation. Grund hierfür war in 59 % der Fälle ein Akutes Atemnotsyndrom (acute respiratory distress syndrome, ARDS). Die Behandlungsdauer auf der Intensivstation betrug im Mittel 14 (8–17) Tage, die Mortalität lag bei 36 % (51 Patienten). Unmittelbare Todesursachen waren mit 37 % ein nicht beherrschbares Lungenversagen, mit 33 % ein septischer Schock, mit 14 % ein Multiorganversagen und mit 12 % ein akuter Herzstillstand.
Nosokomiale Infektionen. 57 der 140 Patienten (40,7 %) erkrankten während des Aufenthalts auf der Intensivstation an einer oder mehreren nosokomialen Infektionen. Insgesamt traten 91 Infektionsepisoden auf.
Die häufigste Infektionsart waren primäre Blutstrominfektionen, die bei 31 % der Patienten vorkamen. Wichtigster Erreger war Enterococcus faecium mit 43 %, gefolgt von Enterococcus faecalis (21 %) und Koagulase-negativen Staphylokokken (11 %). Gramnegative Erreger (Pseudomonas aeruginosa, Klebsiella oxytoca, Serratia marcescens, Bacteroides spp.) wurden nur vereinzelt isoliert. In einem Fall trat eine Blutstrominfektion durch einen MRSA-Keim auf.
In 25 % der Fälle war das Kriterium einer Gefäß- katheter-assoziierten Blutstrominfektion erfüllt. Bei diesen Fällen wurden als Verursacher Koagulase- negative Staphylokokken, E. faecium, Candida albicans, E. faecalis und wiederum ein MRSA-Keim isoliert.
Zusätzlich zum Lungenbefall durch SARS-CoV-2 trat in 21 Fällen (23 %) eine nosokomiale Pneumonie durch typische Krankenhauskeime auf. Häufigster Erreger war mit 8 Episoden Pseudomonas aeruginosa, gefolgt von MRSA (5 Episoden) und Aspergillus fumigatus (2 Episoden).
Weitere Infektionen waren eine Tracheobronchitis (9 Episoden, in 3 Fällen durch P. aeruginosa), Harnwegsinfektionen (7 Episoden, 5 davon durch Enterokokken) und Weichteilgewebsinfektionen (je eine Episode durch K. pneumoniae bzw. Enterobacter cloacae).
Risikofaktoren für tödlichen Verlauf. Nosokomiale Infektionen waren ein signifikanter Risikofaktor für einen letztlich tödlichen Verlauf. Unter den Überlebenden hatten nur 26 Patienten (29 %) eine nosokomiale Infektion, unter den verstorbenen Patienten dagegen 31 (60 %).
Weitere mit einem tödlichen Verlauf assoziierte Faktoren waren höheres Alter, ein auf 15,9 Punkte (versus 12,9) erhöhter APACHE-II-Score, ein ARDS bei der Übernahme und die Entwicklung eines septischen Schocks. Eine nosokomiale Infektion war bei 17 der 51 Patienten, die auf der Intensivstation verstarben, die Hauptursache für den tödlichen Verlauf.
Schlussfolgerung der Autoren
Die Autoren unterstreichen das hohe Risiko von COVID-19-Patienten, während ihres Intensivaufenthalts eine Blutstrominfektion zu erleiden. Auffällig war die häufige Beteiligung von Enterokokken als Verursacher. Dies stand im Gegensatz zum gewohnten Keimspektrum nosokomialer Blutstrominfektionen in Spanien, bei denen eher Staphylokokken als Leitkeime im Vordergrund standen.
Die Autoren spekulieren, dass der frühzeitige empirische Einsatz von Breitspektrum-Cephalosporinen bei den COVID-19-Patienten die Infektion mit Enterokokken gebahnt haben könnte. Sowohl Enterococcus faecalis als auch E. faecium sind bekannter-maßen gegen Cephalosporine resistent. Die Erreger stammen vermutlich aus der eigenen Darmflora der Patienten und werden durch die Antibiotikagaben selektiert.
Kommentar
In der Tat war auf der beschriebenen Intensivstation bei 120 von 140 (85 %) Patienten unmittelbar nach der Aufnahme eine antiinfektive Therapie mit Ceftriaxon (Cephalosporin der 3. Generation) erfolgt. Von diesen Patienten entwickelten im weiteren Verlauf 92 % eine nosokomiale Infektion, während die nicht mit Antiinfektiva prophylaktisch behandelten Patienten lediglich in 80 % der Fälle an einer zusätz- lichen Infektion erkrankten.
Auch das häufig zusätzlich eingesetzte Antibiotikum Azithromycin, von dem man sich zum damaligen Zeitpunkt eine vorteilhafte Wirkung auf den Infektionsverlauf mit SARS-CoV-2 erhoffte, war signifikant mit einem erhöhten nosokomialen Infektionsrisiko assoziiert.
Azithromycin hat wie andere Makrolide keine zuverlässige Enterokokkenwirkung. In der Summe ist den Autoren zuzustimmen, wenn sie aufgrund dieser Erfahrungen für einen differenzierten Einsatz von Antibiotika in der ungezielten Primärtherapie bei schwerer COVID-19-Infektion plädieren.
Beatmungsassoziierte Pneumonien traten eher seltener als zusätzliche Komplikation auf. Einen speziellen Blick auf dieses Problem warf kürzlich eine andere Autorengruppe aus dem Universitätsklinikum von Cambridge/England [2]. Die Autoren verglichen 81 auf der Intensivstation beatmete COVID-19-Patienten mit 144 Kontrollpatienten, die im gleichen Zeitraum aus anderen Gründen beatmet wurden. COVID-19-Patienten entwickelten doppelt so häufig eine Beatmungspneumonie wie Patienten mit anderen Grundkrankheiten. Als Inzidenzwert ausgedrückt lag die Rate der Beatmungspneumonien bei COVID-19-Patienten bei 28/1000 Beatmungstagen, bei Non-COVID-19-Patienten dagegen bei 13/1000 Beatmungstagen. Die nachgewiesenen Erreger differierten zwischen den beiden Patientengruppen nicht signifikant. Typische Erreger nosokomialer Pneumonien wie Enterobakterien, Staphylococcus aureus und Candida albicans wurden in Trachealaspiraten oder einer Bronchiallavage in ähnlicher Verteilung nachgewiesen.
Eine Besonderheit war das Auftreten einer invasiven Aspergillose bei den COVID-19-Patienten. Diese schwerwiegende Pilz-Superinfektion der Lunge trat in der Studie aus Madrid zweimal, in der Studie aus Cambridge dreimal auf. Das Auftreten von Aspergillosen wird von den Autoren aus Cambridge als Hinweis auf eine schwerwiegende pulmonale Immundysfunktion im Rahmen der COVID-19-Erkrankung interpretiert. Die Behandlung kann unter anderem mit dem Pilzmittel Amphotericin B oder Voriconazol erfolgen.
Zusammenfassend gilt, dass eine prophylaktische Antibiotikatherapie ohne Hinweis auf eine bakterielle Infektion bei einem COVID-19-positiven Intensivpatienten nicht empfohlen wird. Bei Patienten mit hochgradigem Verdacht oder dem Nachweis einer bakteriellen Superinfektion muss dagegen sofort leitliniengerecht eine kalkulierte Antibiotikatherapie begonnen werden. Bei einem fehlenden Erregernachweis und normwertigen Procalcitoninwert sollte im Sinne von „Antibiotic Stewardship“ die antiinfektive Therapie zügig wieder beendet werden. Nur ein rationaler und verantwortungsvoller Einsatz von Antibiotika verhindert Selektionsprozesse und Resistenzen bei den Bakterien.
[1] Bardi T et al. Nosocomial infections associated to COVID-19 in the intensive care unit: clinical characteristics and outcome. Eur J Clin Microbiol Infect Dis 2021. doi.org/10.1007//s10096–020–04142-w
[2] Maes M et al. Ventilator-associated pneumonia in critically ill patients with COVID-19. Crit Care 2021; 25: 25. doi.org/10.1186/s13054–021–03460–5