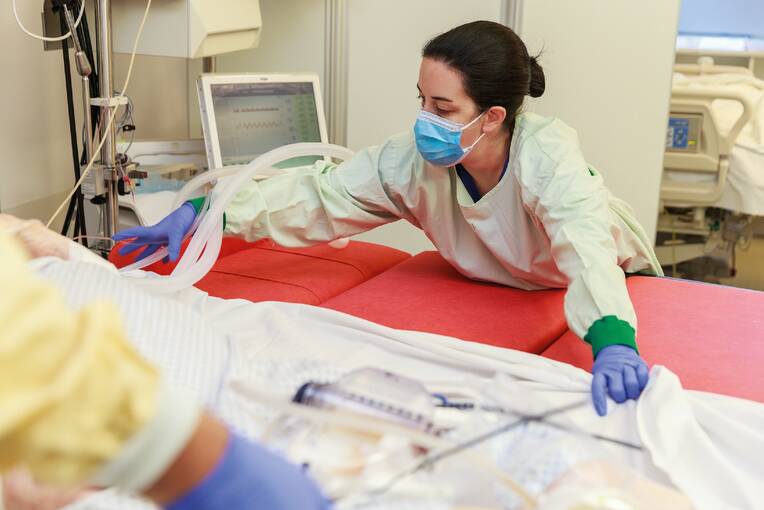
Übersicht. Die Frühmobilisierung von Intensivpatienten erfordert ein durchdachtes, vorsichtiges und interdisziplinäres Vorgehen. Sämtliche Bedingungen, unter denen die Mobilisierung erfolgt, müssen sorgsam abgewogen werden. Algorithmen, Checklisten und Instrumente zur Risikoeinschätzung sind hierzu überaus hilfreich.
Die Frühmobilisierung von Intensivpatienten ist mit erheblichen Vorteilen verbunden. Sie verkürzt die Dauer der Beatmung, den Aufenthalt auf der Intensivstation und die Behandlungstage im Krankenhaus. Sie reduziert zudem das Risiko für ein Delir und verringert die Dauer eines Delirs. Zudem verbessert die frühzeitige Mobilisierung die Selbstständigkeit und Rehabilitation des Patienten (Stiller 2013).
In der 2015 aktualisierten S2e-Leitlinie „Lagerungstherapie und Frühmobilisation zur Prophylaxe oder Therapie von pulmonalen Funktionsstörungen“ (DGAI 2015) wird die Bedeutung der Frühmobilisierung hervorgehoben und ihre Umsetzung eindeutig empfohlen. Die herausgebende Fachgesellschaft gibt hierzu keine allgemeinen Vorgehensweisen vor, sondern empfiehlt, stationsspezifische Algorithmen interprofessionell zu entwickeln.
Genau dies stellt eine große Herausforderung dar. Im Folgenden sollen daher Hilfen für die Entwicklung solcher Handlungsschemata vorgestellt werden.
Maßnahmenbündel empfohlen
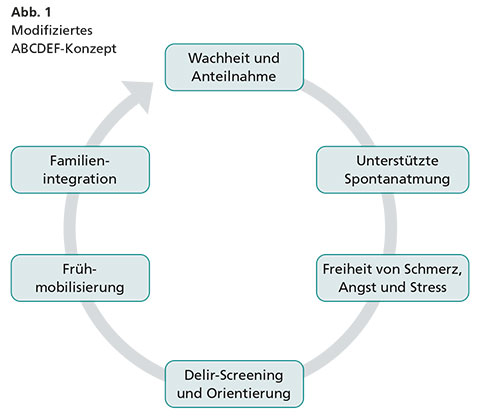
Frühmobilisierung wird als Teil eines Gesamtkonzepts verstanden und umgesetzt. Gut anwendbar ist beispielsweise das Modifizierte ABCDEF-Konzept (Abb. 1) von Balas et al. (2013). Dieses basiert auf dem klassischen ABCDE-Schema, das einen täglichen Aufwach- und Spontanatmungsversuch vorsah. Die Buchstaben stehen für „awakening“ (aufwachen), „breathing“ (atmen), „coordination“ (Koordination der Spontanatmungs- und Aufwachversuche), „delirium assessment and management“ (Delirmanagement) und „early mobilization and rehabilitation“ (Frühmobilisierung und Rehabilitation). Da Intensivpatienten heute aber eher nicht oder nur leicht sediert werden, wurde das ursprüngliche Schema überarbeitet. Das „F“ besteht dabei für Familienintegration.
Auch die aktualisierte S3-Leitlinie „Analgesie, Sedierung und Delirmanagement in der Intensivmedizin“ der Deutschen Gesellschaft für Anästhesiologie und Intensivmedizin (DGAI) und Deutschen Interdisziplinären Vereinigung für Intensiv- und Notfallmedizin (DIVI) empfiehlt ein solches Maßnahmenbündel (DGAI, DIVI 2015). Ziel ist der stress- und angstfreie Patient, der assistiert beatmet und regelmäßig auf ein Delir hin gescreent wird. Der wache Patient kann in Gegenwart seiner Familie an seiner Rehabi- litation und Mobilisierung aktiv teilhaben.
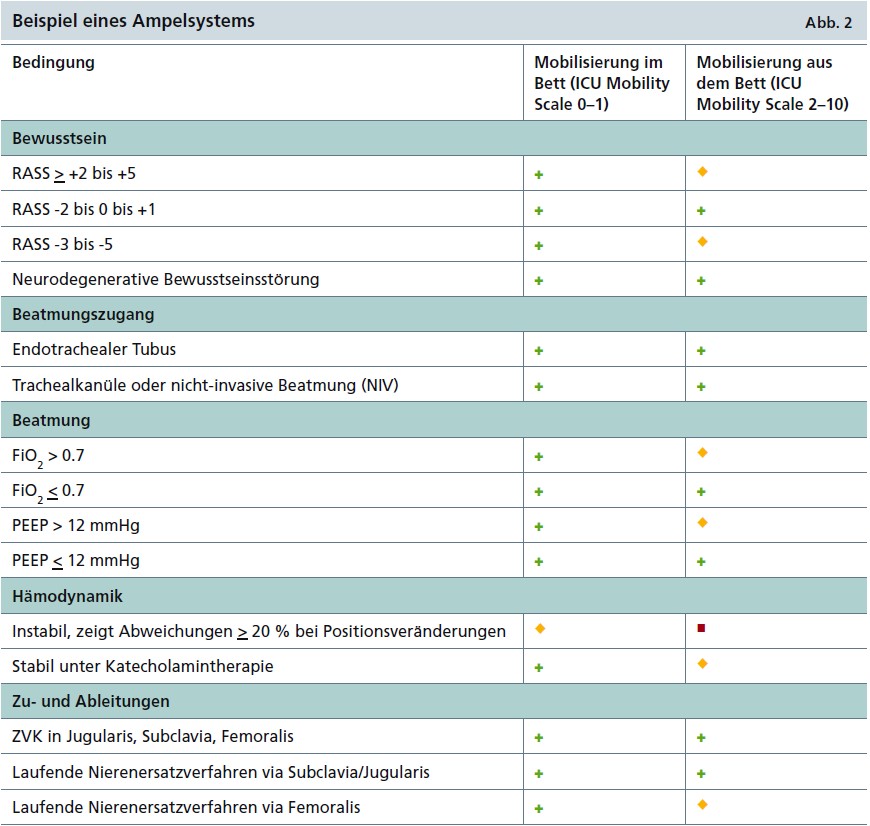
Ein- und Ausschlusskriterien: Laut der Leitlinie zur Frühmobi- lisierung können prinzipiell alle Intensivpatienten anhand von Sicherheitskriterien stufenweise mobilisiert werden. Sie gibt keine absoluten Kontraindikationen an, weist aber auf das erhöhte Risiko bei Patienten mit aktiven Blutungen oder unversorgten Frakturen hin. Eine Mobilisierung könne hier eher schaden als nutzen (DGAI 2015). Es wird daher empfohlen, für die jeweilige Intensivstationen ein Ampelsystem zur Frühmobilisierung zu entwickeln, das von den Patientengruppen sowie von den Strukturen und Prozessen abhängig ist (Hodgson et al. 2014). Die Ampelfarben – grün, gelb, rot – geben an, wie risikoreich die Mobilisierung des jeweiligen Patienten ist (Abb. 2).
- Grün gibt an, dass eine aktive Mobilisierung möglich ist. Die Vorteile überwiegen, das Risiko ist gering.
- Gelb gibt an, dass eine aktive Mobilisierung nur eingeschränkt möglich ist. Es besteht die Gefahr, dass die Risiken überwiegen. Daher muss vor jeder Mobilisierung eine individuelle Absprache getroffen werden
- Rot gibt an, dass keine aktive Mobilisierung möglich ist, da die Risiken die Vorteile überwiegen.
Es hat sich in der Praxis als vorteilhaft erwiesen, das Ampelsystem interprofessionell – unter Beteiligung von Medizinern, Physiotherapeuten, Pflegenden und anderen Berufsgruppen – zu entwickeln und an die jeweiligen Populationen, Kompetenzen und Bedingungen anzupassen.
Kategorien können hierbei beispielsweise das Bewusstsein des Patienten, Beatmungswerte, Hämodynamik sowie Zu- und Ableitungen sein. Spezifische Bedingungen sind abhängig von der Fachrichtung, zum Beispiel Frakturen in der Unfallchirurgie, Herzinfarkte in der Kardiologie und Hirndruck in der Neurologie.
Ein Ampelsystem (Abb. 2) stellt damit ein zentrales Element dar, um die Bedingungen, unter denen die Mobilisierung erfolgt, in verschiedenen Fachbereichen sorgsam abzuwägen. Nach erfolgter Implementierung kann sie in regelmäßigen Abständen zur Evaluation genutzt und auch möglicherweise weiter angepasst werden.
Sicherheitskriterien: Sicherheitsbedenken stellen eine häufige Barriere bei der Implementierung der Frühmobilisierung dar (Dubb 2016). Sind die Mitarbeiter ausreichend geschult und der Patient adäquat vorbereitet, ist die Rate an unerwünschten Ereignissen mit weniger als vier Prozent jedoch sehr gering. Eine unerwünschte Extubation ist mit weniger als einem Prozent ebenfalls sehr selten. Sicherheitskriterien sind notwendig, um Risiken frühzeitig erkennen und Gefahren abwenden zu können. Verschiedene Autoren verwenden absolute Grenzwerte – zum Beispiel Abfall der Sauerstoffsättigung auf unter 90 Prozent oder Überschreitung des systolischen Blutdrucks auf 180 mmHg. Eine relative Abweichung kann dennoch empfohlen werden, da sie der individuellen Patientensituation eher gerecht werden kann, etwa bei Abfall der Sauerstoffsättigung um fünf Prozent oder Anstieg/Abfall des systolischen Blutdrucks um mehr als 20 Prozent (Nessizius 2016).
Für die Herzfrequenz empfehlen Stiller et al. (2003) die altersadjustierte Obergrenze von 220 abzüglich des Alters. Unter Belastung auftretende Herzrhythmusstörungen gelten ebenfalls als unerwünschtes Sicherheitsereignis.
Frühmobilisierung soll für Patienten moderate Trainingseffekte haben, die auch dem Weaning zugute kommen. Um die Anstrengung des Patienten zu erfassen, empfiehlt sich die modifizierte Borg-Skala, die die subjektiv erlebte Anstrengung auf einer Skala von 0 („sehr leicht“) bis 10 („maximal anstrengend“) erfasst. Ein Abbruchkriterium ist bei einem Score von 7 oder mehr gegeben.
Die Beatmungstherapie wird üblicherweise an liegende Patienten angepasst. Während der Mobilisierung kann aufgrund eines höheren Stoffwechsels eine Anpassung der Beatmung erforderlich sein. Auf diese Weise kann eine Mobilisierung auch ab einem Score von 7 oder mehr auf der Borg-Skala möglich sein.
Die modifizierte Borg-Skala kann sowohl für Mobilisierungen wie auch Atemanstrengungen beziehungsweise Spontanatmungsversuche verwendet werden (Nessizius 2016). Weiterhin ist die Verwendung einer Checkliste vor der Mobilisation beatmeter Patienten zu empfehlen (Abb. 3).
Assessments: Zur Beurteilung der Fähigkeit zur Mobilisierung stehen verschiedene interprofessionelle Assessmentinstrumente zur Verfügung. Die Auswahl des Assessments richtet sich nach den Strukturen und Prozessen der jeweiligen Station. Beispiele für Assessments sind:
- Beim Stufenschema nach Morris (2008) wird die passive bis aktive Mobilisierung im Bett und außerhalb des Betts je nach Niveau des Bewusstseins und der motorischen Fähigkeiten durchgeführt.
- Die Kategorisierung nach Hanekom (2013) richtet sich nach der Verweildauer. Aktive Mobilisierung erfolgt bei einem Aufenthalt von unter fünf Tagen, Ausdauer- und Krafttraining wird bei fünf und mehr Tagen durchgeführt.
- Das Marburger Stufenmodell nach Filipovic (2012) definiert ein stufenweises Vorgehen ab dem ersten Tag auf der Intensivstation.
- Das Modell nach Nessizius (2014) kombiniert Konzepte der Frühmobilisierung und des Weanings.
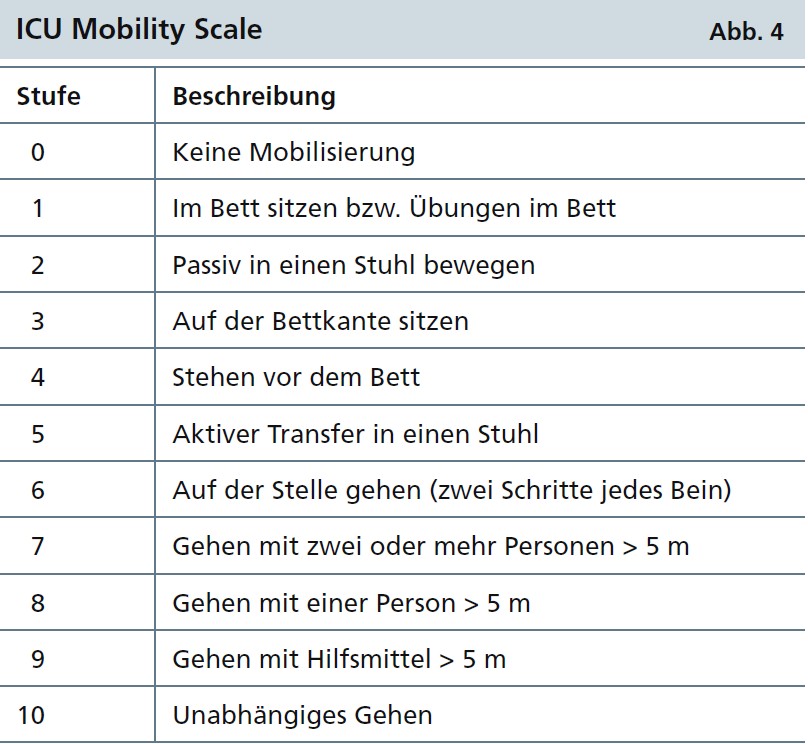
Stufenschema: Für die Planung, Dokumentation und Evaluation der Mobilisierung ist eine Skala der Mobilisierungsstufen wichtig. Hodgson et al. (2014) haben hierzu die ICU Mobility Scale entwickelt (Abb. 4).
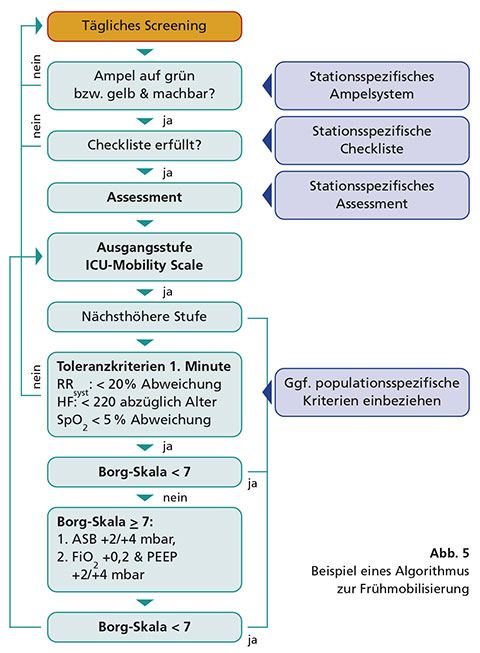
Die ICU Mobility Scale ist valide und zeigt eine gute Reliabilität. Sie kann daher für die Planung, Beschreibung und Dokumentation der Mobilisierung im Intensivbereich empfohlen werden. Zu beachten ist, dass hier der passive Transfer in einen Stuhl als niedrigere Mobilisierungsstufe definiert wurde als das Sitzen auf der Bettkante. Auch Mobilisierungen zum Sitzen innerhalb des Betts entsprechen einer niedrigeren Stufe als ein aktiver Transfer über den Stand in einen Stuhl. Algorithmen: Auch wenn bereits zahlreiche Algorithmen für die Frühmobilisierung veröffentlicht wurden, gibt es bislang keinen, der allgemeingültig ist und für alle Populationen und Bedingungen gilt. Auf der Basis der aktuellen Erkenntnisse wird ein Algorithmus empfohlen, der weiter an die jeweiligen Populationen und Bedingungen anzupassen ist. Einen exemplarischen Algorithmus zeigt Abbildung 5.
Gute Kommunikation nötig
Die Implementierung der Frühmobilisierung benötigt ausreichend Zeit. Um eine Kultur der Frühmobilisierung zu erreichen, sind die Identifikation von Barrieren und die Auswahl geeigneter Strategien wichtig (Dubb 2016).
Relevant sind hier eine unmissverständliche Kommunikationskultur und eine Definition der Zuständigkeiten, etwa bezüglich der Anordnung, Durchführung, Überwachung und Dokumentation. Weiterhin muss ausreichendes und qualitativ hochwertiges Equipment vorhanden sein, um Mobilisierung konkret umsetzen zu können. Eine Veränderung der Haltung der einzelnen Mitarbeiter kann viel Überzeugungsarbeit erfordern.
Wir sind zuversichtlich, dass die Frühmobilisation voraussichtlich als Indikator in die Qualitätsindikatoren der DIVI aufgenommen werden wird.
Es wird bezüglich der Dokumentation empfohlen, in der täglichen Routine folgende Parameter zu erfassen: der Atmungszugang (ETT, TK, NIV, Spontan), die höchste Stufe auf der ICU Mobility Scale, Borg-Skala, kategorisierte Barrieren und Sicherheitsereignisse.
Die Daten ermöglichen in Verbindung mit weiteren Routinedaten eine systematische Auswertung, Evaluation und Feedback an das Team und damit die Möglichkeit, Verbesserungspotenziale zu erkennen.
Zusammenfassend wird empfohlen, ein Maßnahmenbündel zu entwickeln, das einen interprofessionellen Algorithmus zur Frühmobilisierung einschließt. Der Algorithmus sollte folgende Aspekte enthalten (Nydahl 2016):
- tägliches Screening in Bezug auf Mobilität,
- definiertes Ampelsystem, um Vorteile und Risiken abzuwägen,
- Checkliste, die vor der Mobilisierung eingesetzt wird,
- Assessment, das vor der Mobilisierung durchgeführt wird,
- ICU-Mobility Scale, die abhängig von der Population und spezifischen Patientendaten Sicherheitskriterien für die Durchführung der Mobilisierung beinhaltet und mit der angestrebte Mobilisierungsziele definiert werden,
- subjektive Erleben der Patienten, das während der Mobilisierung berücksichtigt wird,
- Dokumentation des Erfolgs anhand der ICU Mobility Scale.
Balas MC, Vasilevskis EE, Olsen KM et al. (2014). Effectiveness and safety of the awakening and breathing coordination, delirium monitoring/management, and early exercise/mobility bundle. Crit Care Med 42: 1024–1036.
Dubb R, Nydahl P, Hermes C et al. (2016). Barriers and Strategies for Early Mobilization of Patients in Intensive Care Units. Ann Am Thorac Soc 5 (1): 724–730.
Hodgson CL, Stiller K, Needham DM et al. (2014). Expert consensus and recommendations on safety criteria for active mobilization of mechanically ventilated critically ill adults. Crit Care 18: 658.
Hodgson C, Needham D, Haines K et al. (2014). Feasibility and interrater reliability of the ICU Mobility Scale. Heart Lung 43: 19–24.
DGAI (2015). Lagerungstherapie und Frühmobilisation zur Prophylaxe oder Therapie von pulmonalen Funktionsstörungen. http:// www.awmf.org/uploads/tx_szleitlinien/001– 015l_S2e_Lagerungstherapie_Fr%C3%B Chmobilisation_pulmonale_Funktionsst%C 3%B6rungen_2015–04.pdf, Abruf: 6.5.2015
DGAI, DIVI (2015). S3-Leitlinie Analgesie, Sedierung und Delirmanagement in der Intensivmedizin (DAS-Leitlinie 2015). http:// www.awmf.org/uploads/tx_szleitlinien/001– 012l_S3_Analgesie_Sedierung_Delirmanage ment_Intensivmedizin_2015–08_01.pdf
Filipovic, S (2012). Vom ersten Tag an mobilisiert. Pflegen Intensiv 2: 22–27.
Hanekom S, Louw QA, Coetzee AR (2013) Implementation of a protocol facilitates evidence-based physiotherapy practice in intensive care units. Physiotherapy 99: 139–145.
Morris PE, Goad A, Thompson C et al. (2008) Early intensive care unit mobility therapy in the treatment of acute respiratory failure. Crit Care Med 36: 2238–2243.
Nessizius S. (2014) Aufgaben der Physiotherapie in der Intensivmedizin. Med Klin Intensivmed Notfmed 109: 547–554.
Nessizius S, Rottensteiner, C., Nydahl, P. (2016) Frührehabilitation in der Intensivmedizin. München: Elsevier. Im Druck.
Nydahl P, Dubb R, Filipovic S, Hermes C, Jüttner F, Kaltwasser A, Klarmann S, Mende H, Nessizius S, Rottensteiner C (2016). Entwicklung von Algorithmen zur Frühmobilisierung auf Intensivstationen. Medizinische Klinik – Intensivmedizin und Notfallmedizin. Im Druck.
Stiller K, Phillips, A. (2003). Safety aspects of mobilising acutely ill inpatients. Physiotherapy Theory & Practice 19: 239–257.
Stiller K (2013). Physiotherapy in intensive care: an updated systematic review. Chest 144: 825–847.
Die Autorengruppe: Peter Nydahl, MScN, Pflegeforschung, Universitätsklinikum Schleswig-Holstein, Campus Kiel; Rolf Dubb, B.Sc., Akademie der Kreiskliniken Reutlingen GmbH; Silke Filipovic, B.Sc., Leitung der Abteilung Physiotherapie, Universitätsklinikum Marburg; Carsten Hermes, Stationsleitung, interdisziplinäre Intensivstation, Fachkrankenpfleger für Anästhesie und Intensivpflege, Betriebswirt im Sozial- und Gesundheitswesen (IHK), HELIOS Klinikum Siegburg; F. Jüttner, Fachkrankenpfleger für Anästhesie und Intensivpflege, Bereichsleitung, Asklepios Paulinenklinik Wiesbaden; Arnold Kaltwasser, B.Sc., Akademie der Kreiskliniken Reutlingen GmbH; Silke Klarmann, Fachleitung, Zentrale Einrichtung Physiotherapie, Universitätsklinikum Schleswig-Holstein, Campus Kiel; Dr. Hendrik Mende, Facharzt für Anästhesie & Intensivmedizin, Klinik für Neurologie, Neurophysiologie, Frührehabilitation und Schlafmedizin, Christophsbad Göppingen; S. Nessizius, Physiotherapeut, Institut für Physikalische Medizin und Rehabilitation, Bereich Innere Medizin/Intensivstation, LKH-Universitätskliniken Innsbruck; C. Rottensteiner, MSc., Universitätsklinik für Physikalische Medizin und Rehabilitation Wien