Die Ein-Lungen-Ventilation ist für die Thoraxchirurgie unabdingbar. Für die seitengetrennte Beatmung während der Operation können Doppellumentubus oder Bronchusblocker zum Einsatz kommen. Der Beitrag beschreibt die Vor- und Nachteile beider Intubationstechniken.
Die Anfänge der heutigen Thoraxchirurgie lassen sich in den frühen Jahren des vergangenen Jahrhunderts finden. Zunächst limitierte das damalige Verfahren der Allgemeinanästhesie, bestehend aus volatiler Anästhetikagabe und dem Erhalt der Spontanatmung der Patientin oder des Patienten, jegliche Entwicklung einer Thoraxchirurgie, da der erforderliche Schnitt in den Thorax für den Patienten mit einem Pneumothorax sowie einem Kollaps der Lunge einherging und zur damaligen Zeit den Tod bedeutete [1]. Um dieser Pathophysiologie entgegenzuwirken, entwickelte der Chirurg Ferdinand Sauerbruch im Jahr 1904 eine Unterdruckkammer, um das Auftreten pulmonaler Komplikationen zu reduzieren [2]. Ein Jahr später erfand der Internist Ludolph Brauer dann die Überdruckbeatmung, die neben der Einführung der endobronchialen Intubation im Jahr 1928 durch Guedel [3] als eine der Sternstunden der Anästhesie gilt.
Die spätere Kombination beider Verfahren in Form der endotrachealen Überdruckbeatmung durch den schwedischen Chirurgen Clarence Crafoord um 1940 ermöglichte dann ab Mitte des vergangenen Jahrhunderts erste thoraxchirurgische Interventionen [4]. Seitdem führte der stetige medizinische Fortschritt zu einer Vielzahl an Weiterentwicklungen auf diesem Gebiet, sodass heutzutage unterschiedliche Hilfsmittel zur Verfügung stehen, um optimale Operationsbedingungen und eine sichere anästhesiologische Versorgung des Patienten zu gewährleisten.
Ein-Lungen-Ventilation
Ein fester Bestandteil ist in diesem Kontext die Anwendung der Ein-Lungen-Ventilation (ELV). Dabei werden linker und rechter Lungenflügel funktionell durch den Einsatz spezieller Doppellumentuben sowie moderner Medizintechnik voneinander getrennt. Dieses anästhesiologische Verfahren übernimmt nach entsprechender ärztlicher Indikationsstellung (Tab 1.)
in der modernen minimalinvasiven, robotergestützten oder videobasierten Thorax-, Abdominal- und Herzchirurgie eine wichtige Rolle. Denn erst durch den Einsatz einer seitengetrennten Beatmung lassen sich das Lungenvolumen der nicht ventilierten Seite reduzieren, intraoperativ störende Atemexkursionen des zu operierenden Lungenabschnitts vermeiden sowie ein Entweichen des applizierten Tidalvolumens über die einseitig eröffneten Luftwege oder das Lungenparenchym verhindern.
Dadurch wird der Operateurin oder dem Operateur schlussendlich ein optimaler Zugangsweg zum Operationsgebiet ermöglicht und die Grundlage für die weitere Freilegung der zu operierenden anatomischen Strukturen geschaffen [5].
Perioperative Vorbereitungen
Grundvoraussetzung sind – neben dem fachgerechten und sicheren Einsatz der zur Verfügung stehenden Hilfsmittel und Techniken zur Sicherung der Atemwege – die individuelle patientenbezogene Planung und Auswahl des Anästhesieverfahrens oder -vorgehens. Denn neben den iatrogenen Einflüssen, etwa infolge der ELV, müssen auch die häufig zusätzlich vorliegenden Begleit- oder Vorerkrankungen (zum Beispiel COPD, pulmonale Hypertonie oder Herzinsuffizienz) der thoraxchirurgischen Patienten in besonderem Maße mitberücksichtigt werden, da diese die hämodynamische Stabilität sowie die Beatmung zusätzlich beeinträchtigen können [5]. Eine ausreichende Präoxygenierung des Patienten, das Vorhalten optionaler Materialien für einen alternativen oder unerwartet schwierigen Atemweg sowie eine klare Kommunikation und Aufgabenverteilung im interprofessionellen Team schaffen Handlungssicherheit und optimale Startvoraussetzungen.
Zur Aufrechterhaltung der Anästhesie ist zwischen der totalen intravenösen Anästhesie (TIVA) oder dem Einsatz von Inhalationsanästhetika zu wählen. Zurzeit gibt es keinerlei Evidenz dazu, dass die Nutzung intravenöser Anästhetika im Vergleich zu Inhalationsanästhesien das Outcome der Patienten beeinflusst [7]. Dennoch wird häufig Propofol der Vortritt vor den volatilen Anästhetika gegeben, um die Umgebungsluft während Bronchoskopien oder Absaugmanövern nicht zu kontaminieren.
Einige Studien zeigten zudem, dass Propofol gegenüber den Inhalationsanästhetika in Bezug auf die Oxygenierung etwas überlegen war [8]. Andererseits weisen die volatilen Anästhetika einen bronchodilatativen Effekt auf, sodass sich positive Effekte auf überempfindliche oder obstruktive Bronchialsysteme ergeben können. Daher scheint es empfehlenswert, die Vor- und Nachteile der Verfahren abzuwägen und die Entscheidung individuell für den Patienten zu treffen [5].
Nach Festlegung des geeigneten Anästhesieverfahrens bedarf es weiterer Vorbereitungen, um gute Voraussetzungen zur adäquaten prä- und intraoperativen Überwachung des Patienten zu schaffen. Hierfür eignet sich unter anderem die Anlage eines arteriellen Zugangs zur Blutdruckmessung am „unten liegenden Arm“, der bei Patienten mit ausgeprägten kardio-pulmonalen Vorerkrankungen auch bereits vor Beginn der Narkoseeinleitung gelegt werden kann. Die direkt im Anschluss entnommene arterielle Blutgasanalyse (BGA) ermöglicht eine entsprechende objektive Beurteilung der Patientenausgangssituation.
Weiterhin sollte der Patient mit mindestens zwei peripheren Zugängen versorgt sowie mit einem Blasenkatheter instrumentiert werden. Das Monitoring vervollständigen EKG, Pulsoxymetrie, Kapnometrie und Temperaturmessung mittels Sonde (nasopharyngeal oder vesikal) [6]. Durch ein adäquates Wärmemanagement lassen sich zudem eine einsetzende Hypothermie und die damit einhergehende verschlechterte Perfusion der belüfteten Lunge vermeiden [9].
Da thoraxchirurgische Operationen mit starken Schmerzen einhergehen, ist auch eine adäquate postoperative Schmerztherapie im Vorfeld mitzuplanen. Ein multimodales Schmerzkonzept, bestehend aus einer Kombination aus Regionalanästhesieverfahren sowie systemischen und nicht medikamentösen Therapiekonzepten, kann hier helfen, Atelektasen und Sekretverhalte über eine schmerzbedingte Schonatmung zu vermeiden [10, 11]. Der thorakalen Periduralanästhesie kommt hierbei eine bedeutende Rolle zu, die mit guter Analgesie ein schnelles Erwachen, eine zügige Extubation sowie die suffiziente Spontanatmung des Patienten möglich macht.
Als Alternativen dazu sind auch paravertebrale oder interkostale (Katheter-)Blockaden möglich. Allerdings sind die interkostalen Verfahren der thorakalen Periduralanästhesie bezüglich der Analgesiequalität deutlich unterlegen [10]. Unterschätzt werden dürfen auch nicht die häufig auftretenden postoperativen Schulterschmerzen, die die Regionalanästhesieverfahren nicht abdecken können [11].
Atemwegssicherung mittels DLT
Zur Atemwegssicherung und anschließenden ELV stehen unterschiedliche Doppellumentuben in verschiedenen Größen zur Auswahl, die in Abhängigkeit zu Körpergröße und Geschlecht des Patienten auszuwählen sind (Tab. 2).
Um den Atemwegswiderstand möglichst gering zu halten und die fiberoptische Bronchoskopie zu erleichtern, ist die größtmögliche Größe des Doppellumentubus (DLT) zu wählen [10]. Ist der passende Tubus ausgewählt und die Applikation der Narkoseinduktionsmedikamente erfolgt, sind die Stimmbänder laryngoskopisch einzustellen. Während des gesamten Intubationsvorgangs gilt es, eine ausreichende Relaxierung des Patienten sicherzustellen.
Nach dem Passieren der Stimmritze wird der enthaltene Führungsstab zurückgezogen und der Tubus mit einer 90-Grad-Drehung, je nach verwendeter Ausführung, in den rechten oder linken Hauptbronchus vorgeschoben. Nach dessen Platzierung erfolgt die Blockung der trachealen Blockermanschette mit 5–10 ml Luft. Ist auskultatorisch beidseits ein Atemgeräusch vorhanden, erfolgt die Blockung des bronchialen Cuffs mit 2–3 ml Luft. Danach werden die beiden Tubuslumen wechselseitig nacheinander mithilfe einer Klemme abgeklemmt, um auskultatorisch und inspektorisch die korrekte Lage für die ELV zu verifizieren [5, 8].
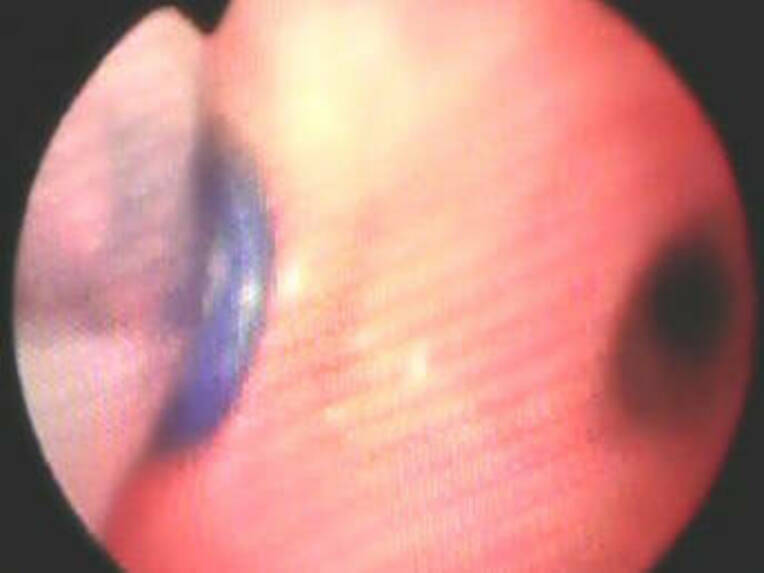
Aufgrund der hohen Anfälligkeit für Dislokationen oder des Risikos zur Verlegung pulmonaler Strukturen sollte initial, nach Abschluss des Intubationsvorgangs sowie bei jeder Umpositionierung des Patienten eine bronchoskopische Lagekontrolle erfolgen. Besonders bei der Nutzung der rechtsläufigen Tuben ist dieses aufgrund der potenziellen Gefahr einer Verlegung des rechten Oberlappens unerlässlich. Mit Einführung des Bronchoskops über das bronchiale Lumen lässt sich sicherstellen, dass die zusätzliche Öffnung am bronchialen Cuff am Abgang des rechten Oberlappens platziert ist. Bei der fiberoptischen Kontrolle durch den trachealen Schenkel ist bei korrekter Positionierung sowohl bei rechts- als auch bei linksläufigen Tuben ein Blick auf die Karina möglich und der Oberrand des bronchialen (blauen) Cuffs im entsprechenden Hauptbronchus erkennbar (Bild 1) [8, 10].
Techniken
Doppellumentubus. Der DLT stellt den aktuellen Goldstandard zur Separierung der Atemwege dar [5]. Insgesamt lassen sich in der Literatur hauptsächlich drei verschiedene DLT-Typen (Robertshaw-, Carlens- und White-Tubus) finden, die sowohl einen proximalen Cuff in der Trachea als auch einen distalen Cuff in einem Hauptbronchus aufweisen [13]. Ist der Robertshaw-Tubus als rechts- und linksläufiger Tubus erhältlich, so dient der Carlens-Tubus zur Intubation des linken und der White-Tubus zur Intubation des rechten Hauptbronchus. Die beiden letztgenannten Tuben unterscheiden sich zudem vom Robertshaw-Tubus durch einen sogenannten Karinasporn [6].
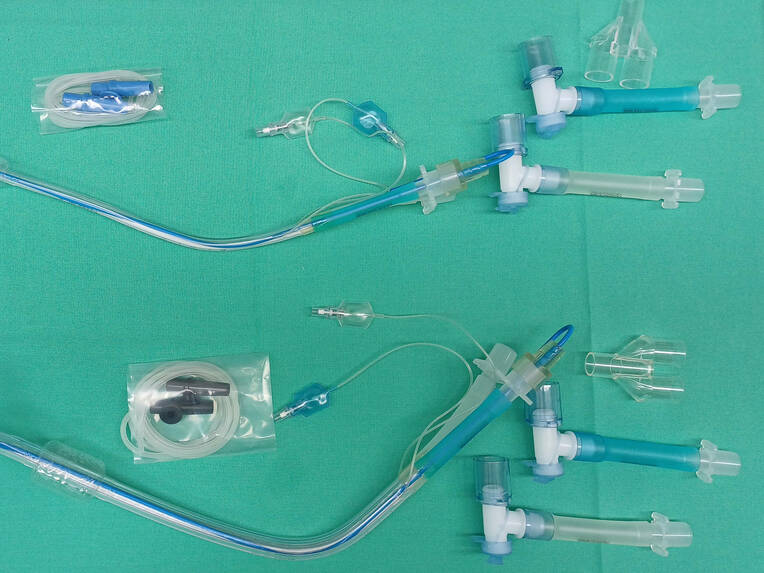
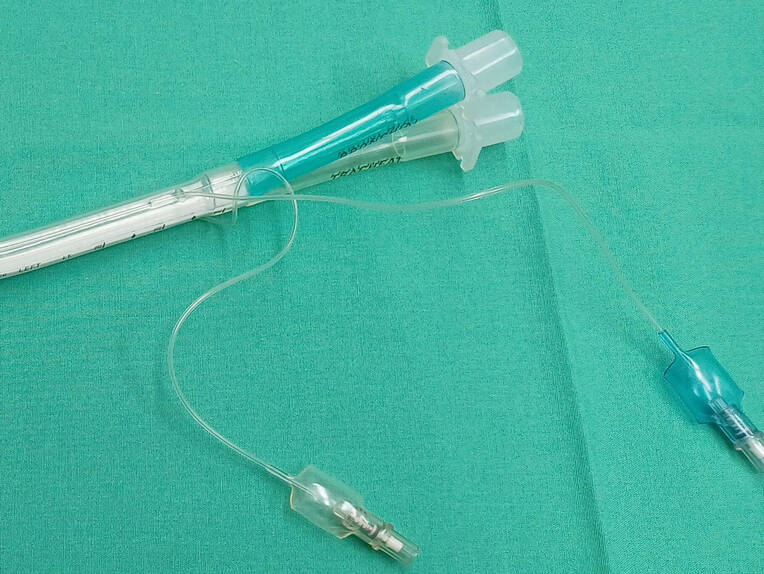
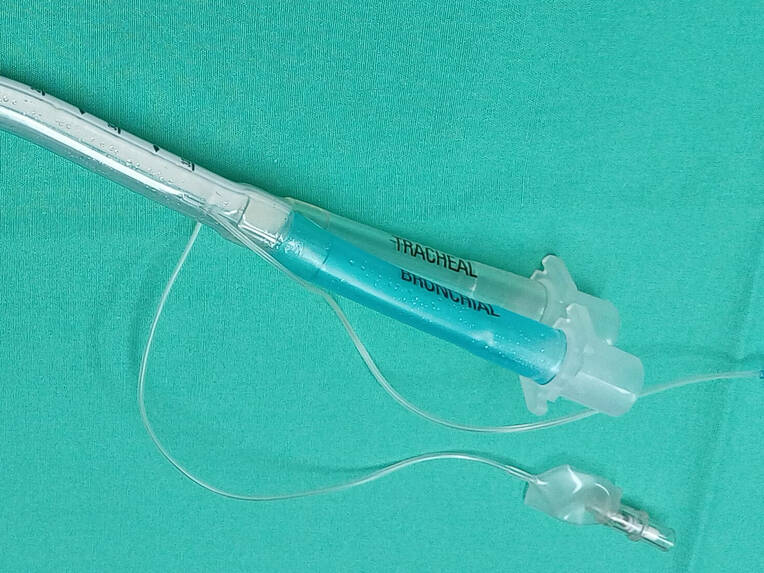
Der DLT nach Robertshaw ist derzeit der am häufigsten verwendete Tubus (Bilder 2 und 3) und in den Größen von 26 bis 41 Ch (Bild 4) erhältlich. Er verfügt über zwei Lumen: dem trachealen Lumen, gekennzeichnet durch die Verwendung von weißem Kunststoff, und dem bronchialen Lumen aus blauem Kunststoff [5, 8]. Da der anatomische Abgang des rechten Oberlappens deutlich näher an der Karina liegt als der Abgang des linken Oberlappens, werden bevorzugt linksläufige DLT genutzt.
Um unter bestimmten Umständen, zum Beispiel bei allen hilusnahen Operationen, dennoch einen rechtsläufigen DLT möglichst risikoarm zu nutzen und eine Verlegung des rechten Oberlappens zu vermeiden, besitzt der rechtsläufige Tubus eine zusätzliche Öffnung im bronchialen Schenkel (Bild 5) [5].
Bronchusblocker. Eine weitere Möglichkeit zur seitengetrennten Beatmung bieten sogenannte Bronchusblocker. Sie kommen häufig dann zum Einsatz, wenn die Einlage eines DLT aus unterschiedlichen Gründen (zum Beispiele Tumore im Mund-/Rachenbereich, thoraxchirurgische Eingriffe bei Kindern) erschwert oder unmöglich ist [5]. Auch hier stehen verschiedene Blockertypen zur Auswahl, wobei die drei am häufigsten eingesetzten Blocker der Univent-, der EZ- und der Arndt-Blocker sind.
Der Univent-Blocker ist ein Endotrachealtubus mit einem integrierten flexiblen Bronchusblocker. Zur Nutzung der beiden anderen Bronchusblocker-Typen ist zunächst ein endotrachealer Tubus zu positionieren. Im Anschluss daran lassen sich sowohl der EZ-Blocker, genauer: einer der beiden Cuffs am distalen Ende des Blockers, als auch der Arndt-Blocker korrekt positionieren. Der Arndt-Blocker (Bild 6) ist ein Katheter, der mit einem Cuff am distalen Ende ausgestattet ist. Er steht in unterschiedlichen Größen zur Verfügung [13]. Im Gegensatz zum DLT verfügen diese Katheter nicht über zwei separate Lumen, sondern weisen lediglich einen dünnen Arbeitskanal auf. Die genaue Platzierung aller Bronchusblocker erfolgt unter bronchoskopischer Sicht in den zu separierenden Hauptbronchus.
ELV in der Praxis
Die physiologische Balance von alveolärer Ventilation und pulmonaler Perfusion (V/Q-Verhältnis) können sowohl unterschiedliche pathophysiologische Veränderungen des Herzzeitvolumens (HZV) als auch Beeinträchtigungen der pulmonalen Ventilation negativ beeinflussen.
Abhängig von der zugrunde liegenden Ursache zeigt sich das Ungleichgewicht dann entweder in einer eingetretenen Hypoxämie oder in einer Hyperkapnie. Entwickelt sich die Hypoxämie primär aus einer eingeschränkten bis hin zu einer vollständig fehlenden Ventilation bei gleichzeitig normaler Lungenperfusion (Shunt) – etwa infolge Bronchusverlegung, Tumoren oder der iatrogenen ELV –, ist die Ursache der Hyperkapnie umgekehrter Natur. Hier bleibt die Ventilation in einem Lungenareal erhalten, jedoch erfolgt keine Perfusion (etwa durch eine Lungenarterienembolie), sodass eine Totraumventilation mit entsprechender Hyperkapnie die Folge ist [5].
Der Umgang mit negativen Einflüssen auf die Ventilation oder Perfusion im Bereich der Lunge oder deren Kompensation stellt eine weitere wesentliche Aufgabe des anästhesiologischen Teams während eines thoraxchirurgischen Eingriffs dar. Herausfordernd sind hierbei die dynamischen Einflüsse auf den Kreislauf oder die Lunge etwa infolge der ELV, der intraoperativen (Seiten-)Lagerung des Patienten oder der bestehenden (pulmonalen) Vorerkrankungen. Regelmäßige BGA-Kontrollen sowie eine engmaschige Anpassung der Beatmung können eine ausreichende Oxygenierung des Patienten sicherstellen und potenzielle Lungenschädigungen durch Volu- oder Barotraumen vermeiden [10, 12].
Als physiologisch einsetzende Kompensationsmöglichkeit des Körpers gilt zudem der Euler-Liljestrand-Reflex oder die hypoxisch-pulmonale Vasokonstriktion (HPV) während der ELV. Infolgedessen werden schlecht ventilierte Lungenabschnitte durch eine reaktive pulmonale Vasokonstriktion weniger stark perfundiert, wohingegen gut ventilierte Bereiche durch die einsetzende Vasodilatation von einer besseren Durchblutung profitieren. Dadurch nehmen im Verlauf das Shuntvolumen ab und die Oxygenierung zu [14].
Weiterhin lassen sich Volu- und Barotraumen mit einer lungenprotektiven Beatmung vermeiden, wenn ein Tidalvolumen von 5–6 ml/kgKG angestrebt und ein entsprechender Positive End-Expiratory Pressure (PEEP, positiv-endexpiratorischer Druck) zwischen 5 cmH2O bis etwa 12 cmH2O, in Abhängigkeit der patientenabhängigen Lungencompliance, zur Anwendung kommt. Insbesondere Patienten mit Adipositas oder restriktiven Lungenerkrankungen können hier von einem höheren PEEP profitieren [15].
Während der lungenprotektiven Beatmung unter ELV kann es ebenfalls akzeptabel sein, vorübergehend höhere CO2-Werte und somit eine permissive Hyperkapnie zu tolerieren. Allerdings existieren dazu keine klaren Empfehlungen zu den Grenzwerten für pH und Kohlendioxidpartialdruck (pCO2). Auch zur Nutzung eines bestimmten Beatmungsmodus während der ELV liegt keine eindeutige Evidenz vor, sodass bisher lediglich eine verbesserte Oxygenierung bei Verwendung einer druckkontrollierten Beatmung nachgewiesen ist [12]. Hierfür sollten die inspiratorische Sauerstofffraktion (FiO2) zwischen 0,5 bis 0,8 liegen [10] und Beatmungsspitzendrücke von über 30 mbar vermieden werden [8].
Zur regelhaften Einschätzung einer adäquat angewandten Beatmung sind regelmäßige Blutgaskontrollen indiziert [16]. Lässt sich hierbei eine drohende Hypoxämie unter der ELV detektieren, so sind unterschiedliche Maßnahmen zur Kompensation möglich. Diese reichen von einer Lagekontrolle zum Ausschluss einer Fehllage über die Bronchialtoilette, der Erhöhung der FiO2 auf 1,0 sowie dem Rekrutierungsmanöver bis hin zur PEEP-Erhöhung auf die beatmete Lunge [15].
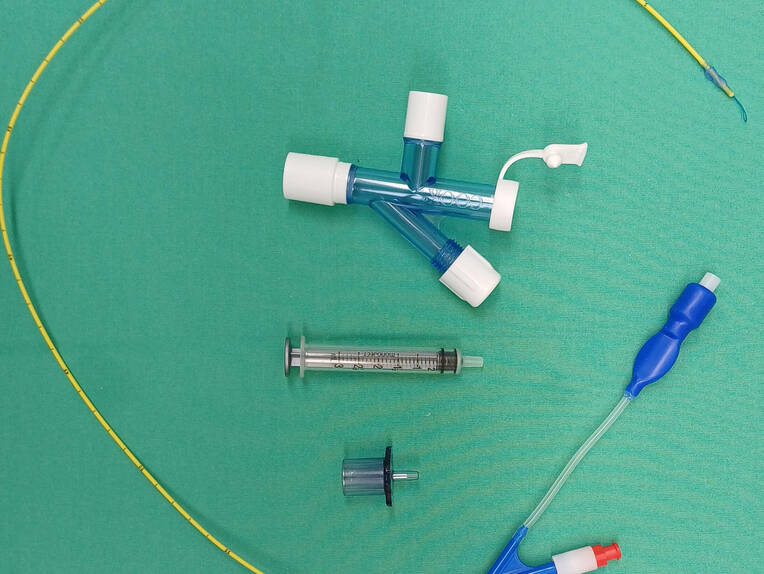
Ist auf diese Weise keine Besserung der Oxygenierung festzustellen, so lässt sich ergänzend ein positiver Atemwegsdruck (CPAP, continuous positive airway pressure) auf die nicht ventilierte Lunge anwenden [11]. Hierfür eignet sich ein zweischrittiges Vorgehen: Zunächst wird Sauerstoff mit einem Flow von 1–2 l/ min. über das deaktivierte Tubuslumen appliziert, sodass eine sogenannte apnoeische Oxygenierung erfolgt und die Sauerstoffkonzentration im Blut ansteigen kann. Reicht dies allein nicht aus, lässt sich über ein zusätzlich angeschlossenes PEEP-Ventil ein ergänzender positiver Atemwegsdruck auf die nicht ventilierte Lunge ausüben (Bild 7) [5]. Neben einer verbesserten Oxygenierung geht damit jedoch auch eine potenzielle Verschlechterung der operativen Gegebenheiten einher [11].
Eine weitere alternative Maßnahme besteht in der zwischenzeitlich erneut durchzuführenden Zwei-Lungen-Ventilation, die allerdings nur in enger Rücksprache mit den Operateuren erfolgen kann, da dafür die Operation zu unterbrechen ist [12].
[1] Brodsky JB, Lemmens HJM. The history of anesthesia for thoracic surgery. Minerva Anesthesiology 2007; 73 (10): 513–524
[2] Sauerbruch F. Die Chirurgie der Brustorgane. 3. Aufl. Springer Verlag, Berlin; 1928
[3] Guedel AE, Waters RM. A new intratracheal catheter. Anesthesia & Analgesia 1928; 7 (4).
[4] Schilling T, Hachenberg T. Atemwegsmanagement in der Thoraxchirurgie. In: Dörgers V, Byhahn C (Hrsg.). Atemwegsmanagement. Springer. 2023; 90–107
[5] Defosse J, Hardt K. Anästhesiologische Aspekte thoraxchirurgischer Eingriffe. In: Hoffmann H, Ludwig C, Passlick B (Hrsg.). Thoraxchirurgie. Springer. 2023; 145–154
[6] Busch C, Heck M, Fresenius M. Anästhesie in der Thoraxchirurgie. In: Heck M, Fresenius M, Busch C (Hrsg.). Repetitorium Anästhesiologie. Für die Facharztprüfung und das Europäische Diplom. 9. komplett überarb. Aufl. Deutschland. Springer; 2023; 631–643
[7] Niedmers H, Defosse JM, Wappler F et al. Anästhesiologisches Management bei operativen Eingriffen am Thorax – eine Auswertung aus dem Deutschen Thoraxregister. Der Anaesthesist 2022; 8 (71); 608–617. doi: 10.1007/s00101–022–01093-z
[8] Kleen M, Zwißler B. Anästhesie in der Thoraxchirurgie. In: Rossaint R, Werner C, Zwißler B (Hrsg.). Die Anästhesiologie. 4. Aufl. Heidelberg: Springer; 2019; 1299–1325
[9] Wiechert N. Ein-Lungen-Ventilation: Narkoseverfahren mit Risiken. PflegenIntensiv 2017; 2 (17): 62–65
[10] Klein U, Hapich A. Anästhesie in der Thoraxchirurgie. In: Wilhelm W (Hrsg.). Praxis der Anästhesiologie – konkret, kompakt, leitlinienorientiert. 1. Aufl. Deutschland: Springer; 2018: 991–1008
[11] Neuner M, Edrich T, Gerner P. Anästhesie in der Thoraxchirurgie – Perioperatives Management. Wiener klinisches Magazin 2015; 4 (18); 104–113. doi: 10.1007/s00740–015–0065–2
[12] Loop T. Einlungenventilation. Anästhesiologie und Intensivmedizin 2020; 61: 579–586. doi: 10.19224/ai2020.579
[13] Larsen R. Thoraxchirurgie. In: Larsen R, Fink T, Müller-Wolff T (Hrsg.). Larsens Anästhesie und Intensivmedizin für die Fachpflege. 10. Auflage. Deutschland. Springer; 2022; 401–408
[14] Henzler D. Anästhesiologische Beurteilung des Patienten: Respiratorisches System. In: Rossaint R, Werner C, Zwißler B (Hrsg.). Die Anästhesiologie. 4. Aufl. Heidelberg: Springer; 2019; 51–88
[15] Meggiolaro KM, Wulf H, Feldmann C et al. Atemwegsmanagement zur Seitentrennung der Lunge bei thorakalen Eingriffen – Ein Update. Der Anaesthesist 2018; 67: 555–567. doi: 10.1007/s00101–018–0470–1
[16] Striebel HW. Anästhesie in der Thoraxchirurgie. In: Striebel HW (Hrsg.). Anästhesie Intensivmedizin und Notfallmedizin. 10. aktual. Aufl. Stuttgart: Thieme; 2020; 340–342