Traumafolgestörungen sind eine häufige Langzeitfolge intensivmedizinischer Behandlungen und werden als Teil des Post Intensive Care Syndrome, kurz PICS, begriffen. Das Erleben traumatischer Ereignisse führt zu Symptomen, die fast alle Bereiche des täglichen Lebens beeinflussen. Daher gewinnen auch die psychischen Folgen intensivmedizinischer Behandlungen zunehmend an Relevanz.
Patientinnen und Patienten (im Folgenden: Patienten) auf der Intensivstation (ITS) sind kritisch krank – ein Begriff, für den es keine einheitliche Definition gibt. Er schließt Erkrankungen ein, die einen lebensbedrohlichen Zustand hervorrufen. Assoziiert sind beispielsweise Polytraumata, Multiorganversagen oder Sepsis [1]. Obwohl die Behandlung auf einer ITS häufig die einzige Option darstellt, um das Überleben zu sichern, geht diese auch mit einer Reihe von Langzeitkomplikationen und gravierenden Folgen einher.
Neben körperlichen Einschränkungen wie dem auf der Intensivstation erworbenen Schwächesyndrom (ICU-aquired Weakness Syndrome), das sich durch das gemeinsame Auftreten einer Critical-Illness-Polyneuropathie (CIP), einer Critical-Illness-Myopathie (CIM) und einer Störung der neuromuskulären Überleitung definiert, stellen auch psychische und neurobiologische Störungen ein potenzielles Risiko dar [2]. Dank der Fortschritte und Entwicklungen in der Medizin steigt die Zahl der Patienten, die kritische Erkrankungen überleben. Dementsprechend gewinnen die Folgen intensivmedizinischer Behandlungen zunehmend an Relevanz [3]. Die psychischen und neuropsychiatrischen Folgen sind vielfältig, rücken aber häufig neben den lebensbedrohlichen Erkrankungen und medizinischen Behandlungen in den Hintergrund.
Ein Versuch, diese Folgen intensivmedizinischer Behandlungen zusammenzufassen und zu benennen, ist das Post Intensive Care Syndrome (PICS). Dieses wird als Sammeldiagnose verstanden, die eine Reihe von Symptomen und Langzeitkomplikationen einer Intensivtherapie zusammenfasst. Unterschieden wird in physische Beeinträchtigungen (pulmonale, neuromuskuläre und physische Funktion), kognitive Beeinträchtigungen (Exekutivfunktion, Gedächtnis, Aufmerksamkeit, Gesichtsfeldeinschränkungen und Verarbeitungsgeschwindigkeit) sowie in Folgen für die mentale Gesundheit (Angststörungen, Depressionen und Posttraumatische Belastungsstörungen, PTBS). Jede dieser Folgen geht mit einer Verminderung der Lebensqualität einher. Mechanismen, die diese neuropsychiatrischen Folgen vollumfassend erklären, gibt es bislang nicht. Vermutet wird ein Zusammenspiel aus Stoffwechselveränderungen, Hypoxiephasen und vorbestehenden psychischen Erkrankungen [3, 11].
Psychische Traumatisierung und Traumafolgestörungen
Der Begriff des Traumas wird im Alltag fast inflationär genutzt [12]. Selten ist in diesen Fällen das körperliche oder psychische Trauma mit pathologischem Krankheitswert gemeint. Ein Trauma oder ein traumatisches Ereignis zeichnet sich durch die „Diskrepanz zwischen der subjektiv erlebten Bedrohung für sich oder andere und den individuellen Bewältigungsstrategien“ [13] aus. Es ist ein „belastendes Ereignis oder eine Situation kürzerer oder längerer Dauer, mit außergewöhnlicher Bedrohung oder katastrophenartigem Ausmaß, die bei fast jedem eine tiefe Verzweiflung hervorrufen würde“ [14] (Textkasten: Traumafolgestörungen: Beispiel und Datenlage).
- Traumafolgestörungen: Beispiel und Datenlage
„Sie waren gefüllt mit Szenen, die mit großer andauernder Angst zu tun hatten: Ich wurde verfolgt, man wollte meine Organe, Krankenschwestern unterhielten sich über dubiose Dinge und bedrohten mich, ich hörte Dschungelgeräusche und war immer liegend ans Bett gefesselt. Mein Sohn starb, weil er in der Welt meiner Fantasie im Auto warten musste, weil gerade keine Besuchszeit war und er den Motor laufen lassen musste, weil es im Winter ja so kalt war […]. Und ich fragte mich ständig: Warum hilft mir denn keiner? Isolation pur“ [4].
Mit diesen Worten beschreibt eine Patientin rückblickend ihre Erinnerungen an ihren Aufenthalt auf der Intensivstation (ITS). Wie dieser Patientin geht es einer Vielzahl von Menschen, die nur mit einer intensivmedizinischen Behandlung überleben können. Von den im Jahr 2017 rund 2,13 Mio. intensivmedizinisch Behandelten waren ca. 430.500 auf eine mechanische Beatmung angewiesen [5]. Die Lebenszeitprävalenz der PTBS liegt in der Allgemeinbevölkerung Deutschlands bei 1,5–2,3 % [6]. Die Angaben zu Inzidenz und Prävalenz von Traumafolgestörungen nach intensivmedizinischer Behandlung schwanken stark. Studien berichten von einer Inzidenz von bis zu 64 % [7].
Traumafolgestörungen werden differenziert nach akuter Belastungsreaktion, PTBS und Anpassungsstörung [14]. Entsprechend der Internationalen statistischen Klassifikation der Krankheiten und verwandter Gesundheitsprobleme (International Statistical Classification of Diseases and Related Health Problems, ICD-10) und dem diagnostischen und statistischen Leitfaden psychischer Störungen (Diagnostic and Statistical Manual of mental Disorders, DSM-V) beschreibt die North American Nursing Diagnosis Association (NANDA) die Pflegediagnose „Posttraumatisches Syndrom“ als eine „anhaltende, fehlangepasste Reaktion auf ein traumatisches, überwältigendes Ereignis“ [15].
In diesem Artikel verwendet die Autorin den Begriff Traumafolgestörungen übergeordnet für alle Störungsbilder, die sich unter den bereits beschriebenen Diagnosen F43. (Reaktionen auf schwere Belastungen und Anpassungsstörungen) subsumieren lassen [14]. Der Fokus liegt auf der komplexesten Form, der PTBS.
Kriterien einer PTBS. Im Rahmen der DSM-V sind diagnostische Kriterien formuliert, die für die Diagnose PTBS erfüllt sein müssen [14]:
- Direktes Erleben eines oder mehrerer traumatischer Ereignisse oder das Erleben solcher Ereignisse bei anderen Personen
- Intrusionen, dissoziative Reaktionen (z. B. Flashbacks)
- Vermeidung von Reizen, die mit dem traumatischen Ereignis in Verbindung gebracht werden (z. B. Orte, Personen etc.)
- Veränderung von Stimmung, dissoziative Amnesie in Bezug auf das Trauma, anhaltende negative Assoziationen, Interessenverlust, verminderte Teilnahme an Aktivitäten, Gefühl der Entfremdung
- Reizbarkeit und Wutausbrüche, riskantes oder selbstzerstörerisches Verhalten, übermäßige Wachsamkeit (Hypervigilanz), Schreckreaktionen, Konzentrationsstörungen oder Schlafstörungen
In Situationen, in denen ein Mensch potenziell mit dem Tod rechnen muss, kommt es im Gehirn zu einer Notreaktion. Diese zunächst einmal physiologische Reaktion des menschlichen Körpers führt zu einer fehlerhaften Abspeicherung des während des Ereignisses Erlebten. Diese fehlerhaft abgespeicherte Information zeichnet sich später im klinischen Bild der Traumafolgestörung ab [13].
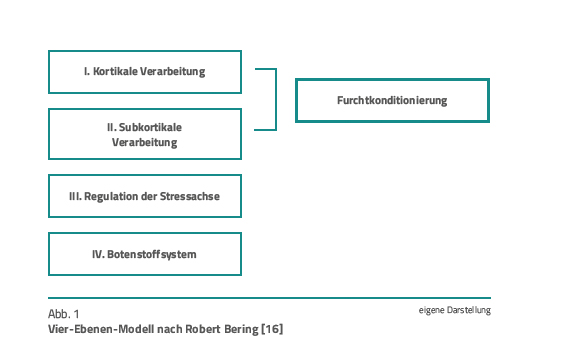
Furchtkonditionierung. Ein Mechanismus in der Pathophysiologie von Traumafolgestörungen ist die Furchtkonditionierung. Furcht und Angst sind Emotionen des Individuums, die das Überleben in gefährlichen Situationen sicherstellen sollen und sind demnach in jedem Menschen verankert [16]. Die Furchtkonditionierung scheint einen elementaren Teil der Entstehung und der Aufrechterhaltung der PTBS als spezifische Form der Traumafolgestörung darzustellen, da sie als Erklärungsansatz für die Symptomatik der Wiedererlebung (Intrusion, Flashbacks etc.) gelten. Im Rahmen der Furchtkonditionierung werden die sensorischen Eindrücke in der Amygdala mit einem unkonditionierten Stressor kombiniert. Das Gehirn verarbeitet diese Reize auf kortikaler und auf subkortikaler Ebene. Die subkortikale Ebene scheint primär für die Analyse von Reizen zuständig zu sein, die im Unterbewusstsein des Individuums einsetzen. Aufgrund dessen ist die furchtkonditionierte Reaktion dem Individuum nicht bewusst. Dies gilt als Erklärungsansatz für die nicht steuerbaren Wiedererlebenssymptome [17].
Psychopathologie des Traumatisierungsprozesses. Ist der Körper einem traumatischen Erlebnis ausgesetzt, gehen die Reaktion und die Prozesse im Körper über eine duale Stressreaktion (Textkasten: Duale Stressreaktion) hinaus. Um die Psychopathologie des Traumatisierungsprozesses anhand der neurobiologischen Grundlagen zu beschreiben, bieten sich zwei Modelle an, die sowohl die unterschiedlichen Ebenen des zentralen und peripheren Nervensystems darstellen als auch den prozesshaften Verlauf des Krankheitsbilds miteinschließen [10]:
- Duale Stressreaktion
Das Erleben von Stress oder stressbehafteten Situationen löst im menschlichen Körper zwei spezifische Reaktionen aus, die sich in einer typischen Stressantwort präsentieren [8]. Im Rahmen der ersten Reaktion kommt es zu einer Aktivierung der Amygdala und des Hypothalamus. Dies bewirkt innerhalb verschiedener vegetativer Zentren eine Ausschüttung des Katecholamins Noradrenalin. Die Folge ist eine erhöhte Aufmerksamkeit und Verhaltensbereitschaft. Zusätzlich wird das sympathische Nervensystem aktiviert, was ebenfalls zu einer vermehrten Ausschüttung von Katecholaminen aus der Nebennierenrinde führt [8].
Im menschlichen Körper ereignen sich eine Reihe von Anpassungsreaktionen: Die Gefäße in der Haut, der Muskulatur, im Gehirn und im viszeralen System kontrahieren, der Körper beginnt zu schwitzen, es entsteht eine Gänsehaut, die Glukoseaufnahme wird erhöht (Energiebereitstellung), die Leber steigert zusätzlich die Glukoneogenese, die Herzfrequenz und der Blutdruck steigen, die Pupillen und Ziliarmuskeln weiten sich und es kommt zur Bronchodilatation [9].
Die zweite Reaktion beschreibt die Hypothalamus-Hypophysen-Nebennierenrinden-Achse (HHNA/HPA-Achse). Diese setzt einige Minuten nach der ersten Reaktion ein [8]. Der Körper setzt den sog. Cortico-Releasing-Faktor (CRF) frei, um Adrenocorticotropin (ACTH) zu synthetisieren, was die Ausschüttung von Kortisol zur Folge hat. Die erhöhte Bereitstellung von Kortisol soll als eine Art Filter in der Stresssituation fungieren und somit einer Überforderung durch Sinneseindrücke entgegenwirken [10]. Nachdem das stressauslösende Ereignis nicht mehr auf den Körper einwirkt, nehmen auch die Stresssymptome ab [8].
- Das Vier-Ebenen-Modell nach Bering orientiert sich an den neurophysiologischen Grundlagen (Abb. 1).
- Das Verlaufsmodell der psychischen Traumatisierung nach Fischer und Riedesser umfasst verschiedene Phasen:
- Prätraumatische Antezedenzbedingungen
- Traumatische Situation
- Reaktion und traumatischer Prozess
Die Phase „Reaktion und traumatischer Prozess“ setzt ein, wenn nach der traumatischen Exposition kein Erholungszustand eintritt. In diesen Schritt lassen sich die neurobiologischen Grundlagen, also das Vier-Ebenen-Modell nach Bering, integrieren. Ein akutes Psychotrauma entsteht immer dann, wenn ein Individuum in einer traumatischen Situation nicht adäquat reagieren kann. In der Phase der akuten Traumatisierung kommt es zu einer vermehrten Ausschüttung von Botenstoffen im zentralen und peripheren Nervensystem, was wahrscheinlich eine Fehlfunktion im Hippocampus-Temporallappensystem zur Folge hat. Das Gehirn speichert die traumatischen Erinnerungen fehlerhaft ab, sodass diese im Gedächtnis als zusammenhangslose Sinneseindrücke vorliegen und nicht bewusst abrufbar sind [10].
Risikofaktoren für Traumafolgestörungen auf der ITS
Risikofaktoren für Traumafolgestörungen auf der ITS sind vielfältig und betreffen verschiedenste Bereiche im interdisziplinären Versorgungsprozess. Werden Risikofaktoren rechtzeitig erkannt, lassen sich deren Einflüsse minimieren oder ihr Effekt mittels geeigneter Interventionen abschwächen.
„Prätraumatische und biografische Risikofaktoren“ beeinflussen vermutlich die Manifestation von Traumafolgestörungen. Nennenswerte Faktoren sind zum einen das weibliche Geschlecht [18, 19], der sozioökonomische Status [19, 20] sowie vorbestehende psychische Erkrankungen (Angststörungen, Depressionen, PTBS) [21, 22, 23].
Auch wenn prätraumatische und biografische Risikofaktoren im Rahmen der intensivmedizinischen Behandlung nicht beeinflussbar oder modifizierbar sind, ist ihre Rolle in der Entwicklung einer PTBS nicht zu vernachlässigen. Identifizierte Risiko- und Schutzfaktoren, die auch prätraumatische und biografische Faktoren mit einschließen, sind im Hinblick auf die Prognose und Interventionsplanung von Bedeutung [19].
Auch „Wahrnehmungsassoziierte Risikofaktoren“ und existenzielle Erfahrungen haben offenbar einen Einfluss auf die Entwicklung einer PTBS. Von besonderer Bedeutung könnte hier das Erleben von Schmerzen bzw. die Erinnerung an Schmerzen sein [20]. Auch peritraumatischer Schmerz, der insbesondere bei der Versorgung von polytraumatisierten Patienten eine Rolle spielt, hat einen Einfluss auf die Entwicklung von Traumafolgestörungen. Erklärt wird dieser Effekt dadurch, dass peritraumatischer Schmerz zu mehr negativen Bewertungen innerhalb des Traumagedächtnisses führt und dadurch mehr Stress mit dem Trauma verbunden ist [24]. Darüber hinaus könnten weitere Erinnerungen wie Albträume und Halluzinationen, Panik und Angst sowie Atemnot einen relevanten Einfluss haben [25].
Im Zusammenhang mit der Art und dem Umfang der Erinnerungen scheinen Sedierung und Analgesie zu stehen. Tief sedierte (ein Grenzwert z. B. anhand der Richmond Agitation and Sedation Scale [RASS] wird nicht definiert) Patienten berichten häufig von einer Amnesie während ihrer Zeit auf der ITS, von Schwierigkeiten, sich an wichtige Sequenzen stressbelasteter Situationen zu erinnern, sowie von verstörenden/beunruhigenden Erinnerungen und Wahnvorstellungen [26]. Wahnvorstellungen beziehen sich auf Ereignisse auf der ITS, die Patienten falsch interpretiert haben (z. B. medizinisches Personal versucht, sie durch Injektionen zu töten). Diesen Sicherheitsverlust beschreiben sie als besonders traumatisch [23]. Über das Gefühl der Hilflosigkeit und des Kontrollverlusts geht die von Patienten geäußerte Todesangst hinaus [27, 28, 29].
Eine maschinelle Beatmung beschreiben Patienten als stressigen, invasiven und erschreckenden Vorgang, der mit der Unfähigkeit zu atmen einhergeht und den sie mit Angst assoziieren [30]. 42,4 % der beatmeten Patienten berichten, Erinnerungen an Atemnot zu haben [31]. Untersuchungen zeigen, dass diese stressbehaftete Situation der Beatmung als signifikanter Einflussfaktor für eine PTBS anzusehen ist [30].
Ein weiterer Risikofaktor sind vermutlich „Krankheitsassoziierte Faktoren“, die sich insbesondere durch die Schwere der Erkrankung und die dadurch erforderlichen Maßnahmen definieren [32]. Mit der zunehmenden Schwere der Erkrankung steigt auch die Wahrscheinlichkeit, dass sich die Aufenthaltsdauer verlängert, die ebenfalls mit einer PTBS assoziiert ist [20, 25, 31].
Perspektiven für die klinisch-pflegerische Praxis
Vermeidung einer Sedierung. Die Intensivmedizin bevorzugt zunehmend flach sedierte, wache Patienten [33]. Die S3-Leitlinie „Analgesie, Sedierung und Delirmanagement in der Intensivmedizin“ empfiehlt eine Sedierung nur dann, wenn auch eine tatsächliche medizinische Indikation vorliegt. Wenn keine Kontraindikation vorliegt (z. B. Hirndrucksymptomatik), ist ein RASS von 0 bis -1 anzustreben. Grundlage dafür stellt immer eine ausreichende Analgesie dar [34].
Derzeit liegen nur eingeschränkt aussagekräftige Ergebnisse zu günstigen Sedierungspraktiken und zu einer PTBS vor. Kress et al. konnten in ihrer Untersuchung zu verschiedenen Sedierungspraktiken nachweisen, dass eine tägliche Unterbrechung der Sedierung die PTBS-Inzidenz senken kann [35]. Die Ergebnisse der S3-Leitlinie weisen hingegen darauf hin, dass eine tägliche Sedierungsunterbrechung einer protokollbasierten Sedierung grundsätzlich nicht überlegen ist [34].
Forschungsergebnisse zeigen, dass tief sedierte häufiger als weniger tief sedierte Patienten eine PTBS entwickeln [40]. Nicht sedierte Patienten sind signifikant kürzer auf eine mechanische Beatmung angewiesen und haben eine verkürzte Aufenthaltsdauer [41]. Die Vermeidung einer Sedierung könnte demnach eine Exposition mit potenziellen Risikofaktoren minimieren. Ohne eine Sedierung können Patienten Bedürfnisse wie Durst, Schmerzen oder Ängste äußern, sodass das Krankenhauspersonal adäquat auf diese eingehen kann [42].
Um auch bei intubierten Patienten ohne Sedierung eine Tubustoleranz zu gewährleisten, wird die sog. Analgesie-First-Strategie empfohlen. Als Co-Adjuvantien sind Alpha-2-Agonisten (z. B. Clonidin) und Dexmedetomidin einsetzbar. Nichtmedikamentöse Maßnahmen zur Erhöhung der Tubustoleranz sind das Erleben des Atmen-Könnens, die Mobilisierung und die Gegenwart von Angehörigen [33].
Schmerzmanagement. Das Erleben von Schmerzen stellt offenbar einen signifikanten Risikofaktor dar [20]. Die S3-Leitlinie empfiehlt für die ITS ein opioid-basiertes Schmerzmanagement mit der adjuvanten Applikation von Nicht-Opioid-Analgetika (und bei Bedarf Co-Analgetika). Eine patientenkontrollierte Analgesie sollte auch auf der ITS bevorzugt werden [34]. Für das Monitoring der Analgesie ist die Anwendung eines Selbst- und eines Fremdeinschätzungsinstruments zu empfehlen [34]. Die frühzeitige Applikation von Morphin als analgetische Substanz scheint insbesondere bei schwer verunfallten Patienten eine Reduktion der PTBS-Inzidenz und auch der Stärke der Symptome bewirken zu können [42, 43].
Psychologische Intervention. Patienten auf der ITS sind häufig stark belastet und befinden sich in einer psychischen Ausnahmesituation. Empfehlenswert ist deshalb die kontinuierliche Anwesenheit einer Psychologin bzw. eines Psychologen sowie ein regelmäßiges Screening der psychischen Symptome [44]. Sollte kein psychologischer Dienst auf der Station selbst angesiedelt sein, sollten innerhalb des Hauses Strukturen bestehen, die es ermöglichen, zeitnah eine psychologische Unterstützung für den Patienten anzufordern.
Darüber hinaus sollte eine Möglichkeit zur Krisenintervention bestehen [37]. Die angewendeten psychologischen Interventionen sollten immer nach individuellem Bedarf erfolgen. Es können sowohl Entspannungs- und Imaginationsübungen Anwendung finden als auch psychoedukative Maßnahmen zur Verarbeitung traumatischer Ereignisse (dies dürfte insbesondere bei Patienten mit einem Polytrauma oder nach einem Suizidversuch sinnvoll sein).
Zusätzlich lässt sich auch die Technik des Refraimings nutzen, bei der der psychologische Dienst das Ziel verfolgt, durch gezielte Fragen einen Perspektivwechsel des Patienten anzustreben. Insbesondere bei Wahrnehmungseinschränkungen oder kognitiven Defiziten scheint eine Realitätsorientierung einen Benefit für den Patienten darzustellen [37].
Die Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin (DIVI) empfiehlt eine Kombination verschiedener supportiv-unterstützender Interventionen. Patienten sollten Sicherheit vermittelt und die Möglichkeit geboten werden, über belastende Ereignisse zu sprechen und somit das Geschehene aufzuarbeiten und entstandene Erinnerungslücken zu schließen [45].
Intensivtagebuch. Eine Möglichkeit der Frühintervention bei Patienten, die an Bewusstseinseinschränkungen leiden, ist das Intensivtagebuch [38]. Während des gesamten stationären Aufenthalts führen Pflegepersonen, weitere versorgende Akteure sowie die Angehörigen ein Tagebuch, in dem sie besondere Ereignisse und Entwicklungen dokumentieren [46]. Es gibt Hinweise darauf, dass diese Maßnahme die Entwicklung einer PTBS eindämmen kann [39]. Die Tagebücher ermöglichen die Korrektur fehlender oder irrealer, aber als real wahrgenommener Ereignisse und unterstützen die Förderung des Kohärenzsinns [38].
Studien zur Wirksamkeit solcher Intensivtagebücher sind bislang kaum vorhanden. Allerdings: Die Symptome von Angst- und depressiven Störungen lassen sich reduzieren. Zum aktuellen Zeitpunkt gestaltet sich die methodische Untersuchung der Wirkung von Intensivtagebüchern schwierig, da einheitliche Vorgaben zu deren Umsetzung und Gestaltung fehlen (z. B. wie viele Einträge werden täglich verfasst, wer sollte diese Einträge schreiben etc.). Auch zu möglichen Nebenwirkungen gibt es zum aktuellen Zeitpunkt noch keine Ergebnisse [38].
Posttraumatische Beschwerden. Eine besondere Bedeutung kommt auch der hausärztlichen Versorgung zu. Die Symptome der PTBS treten innerhalb der ersten sechs Monate nach dem traumatischen Ereignis auf. Zu diesem Zeitpunkt sind die meisten Patienten bereits entlassen und befinden sich wieder im häuslichen Umfeld [47]. Zu empfehlen ist das aktive Ansprechen auf mögliche Symptome, da Patienten mit posttraumatischen Beschwerden womöglich ein Vermeidungsverhalten verinnerlicht haben [39]. Mit einer verzögerten oder fehlenden Diagnosestellung verschiebt sich auch der Beginn der adäquaten Therapie. Ein mögliches Fokus-Screening ist der Primary-Care-PTSD-Screen [39].
- Möglichkeiten zur Reduktion von Traumafolgestörungen auf der ITS
- Erfassung prätraumatischer und biografischer Risikofaktoren [18, 20, 21, 22]
Fehlende Standards
Die Besonderheit des Settings ITS besteht darin, dass kritisch kranke Patienten im Fokus stehen. Die intensivmedizinische Behandlung ist demnach zwingend notwendig, um deren Überleben zu sichern, sodass die Exposition mit den identifizierten Risikofaktoren häufig nicht vermeidbar ist. Die klinische Forschung in der Intensivmedizin stellt ein sehr sensibles Handlungsfeld dar. Mit fehlenden Standards geht eine reduzierte Vergleichbarkeit der Ergebnisse einher (z. B. durch unterschiedliche Sedierungspraktiken). Darüber hinaus einschränkend wirkt die fehlende Datenlage in der Pflegewissenschaft, sodass die pflegewissenschaftliche Perspektive und pflegerische Maßnahmen nur eingeschränkt abbildbar sind.
[1] Oehmichen F, Pohl M. Chronisch kritisch krank: Langzeitfolgen von Sepsis und multipler Organdysfunktion. In: Werdan K, Müller-Werdan U, Schuster HP et al. (Hrsg.). Sepsis und MODS. Berlin, Heidelberg: Springer; 2016: 343–356
[2] Pohl M, Mehrholz J. Begriffsbestimmung: Critical-Illness-Polyneuropathie und Critical-Illness-Myopathie. Neuroreha 2013; 5 (1): 10–16
[3] Tempel M, Pfeifer M. Das Post Intensive Care Syndrome. Eine neue Entität? Deutsche Medizinische Wochenschrift 2013; 138 (23): 1221–1224
[4] Fangmeyer M. „Ich traute der realen Welt nicht mehr“: Eine Intensivpatientin erzählt. Physiopraxis 2013; 11 (04): 54–57
[5] Statistisches Bundesamt. Behandlungsfälle in der intensivmedizinischen Versorgung in Deutschland in den Jahren 2010 bis 2017; 2018. Erhoben durch: Destatis – Grunddaten der Krankenhäuser 2017
[6] Deutscher Bundestag. Sachstand: PTBS – Zahlen sowie Aspekte geschlechterspezifischer Behandlungsangebote; 2016 Aktenzeichen: WD 9 – 3000 – 069/16
[7] Parker AM, Sricharoenchai T, Raparla S et al. Posttraumatic Stress Disorder in critical Illness Survivors – A Metaanalysis. Critical Care Medicine 2015; 43 (1): 1121–1129
[8] Seidler GH, Laszig P, Micka R et al. Aktuelle Entwicklungen in der Psychotraumatologie – Theorie und Krankheitsbilder. Gießen: Psychosozial-Verlag; 2006
[9] Gerrig RJ, Zimbardo PG. Psychologie. 18. aktualisierte Aufl. Deutschland: Pearson; 2008
[10] Bering R. Neurobiologie der Posttraumatischen Belastungsstörung. In: Fischer G, Schay P. Psychodynamische Psycho- und Traumatherapie. VS Verlag für Sozialwissenschaften; 2008: 99–112
[11] Rawal G, Yadav S, Kumar R. Post-intensive care syndrome: An overview. Journal of Translational Internal Medicine 2017; 5 (2): 90–92
[12] Schay P, Liefke I. Sucht und Trauma: Integrative Traumatherapie in der Drogenhilfe. Wiesbaden: VS Verlag für Sozialwissenschaften; 2009
[13] Pausch MJ, Matten SJS. Trauma und Traumafolgestörung. In: Medien, Management und Öffentlichkeit. Wiesbaden: Springer-Verlag; 2018
[14] Dilling H, Freyberger HJ. ICD-10: Taschenführer zur ICD-10-Klassifikation psychischer Störungen: Nach dem Pocket Guide von J. E. Cooper. Bern: Hogrefe; 2016
[15] Doenges ME, Moorhouse MF, Murr AC. Pflegediagnosen und Pflegemaßnahmen. Bern: Hans Huber; 2013
[16] Baumann C. Psychologische und genetische Einflussfaktoren auf die Furchtkonditionierung und die Generalisierung konditionierter Furcht. Dr. rer. Nat. Diss., Julius-Maximilians-Universität Würzburg Sektion Neurowissenschaften; 2018. Zugriff: 01.07.2020
[17] Maercker A. Psychologische Perspektiven und Therapiekonsequenzen. In: Maercker A, Rosner R (Hrsg.). Psychotherapie der posttraumatischen Belastungsstörungen: Krankheitsmodelle und Therapiepraxis störungsspezifisch und schulenübergreifend. Stuttgart: Thieme Verlag; 2006
[18] Girard TD, Shintani AK, Jackson JC et al. Risk factors for post-traumatic stress disorder symptoms following critical illness requiring mechanic ventilation: a prospective cohort study. Critical care 2007; 11 (1): R28
[19] Becker-Nehring K, Witschen I, Bengel J. Schutz- und Risikofaktoren für Traumafolgestörungen: Ein systematisches Review. Zeitschrift für Klinische Psychologie und Psychotherapie 2012; 41 (3): 148–165
[20] Myhren H, Ekeberg O, Toien K et al. Posttraumatic stress, anxiety and depression symptoms in patients during the first year post intensive care unit discharge. Critical care 2010; 14 (1): R14
[21] Patel MB, Jackson JC, Morandi A et al. Incidence and Risk Factors for Intensive Care Unit-related Post-traumatic Stress Disorder in Veterans and Civilans. American Journal of Respiratory and Critical Care Medicine 2015; 139 (12): 1373–1381
[22] Bienvenu OJ, Gellar J, Althouse BM et al. The Journal of Nervous and Mental Disease 2017; 205 (10): 780–787
[23] Jones C, Bäckman CC, Capuzzo M et al. Precipitants of post-traumatic stress disorder following intensive care: a hypothesis generating study of diversity in care. Intensive Care Medicine 2007; 33: 978–985
[24] Norman SB, Stein MB, Dimsdale JE, Hoyt DB. Pain in the aftermath of trauma is a risk factor for post-traumatic stress disorder. Psychological Medicine 2008; 38: 533–542
[25] Hauer D, Weis F, Kruseneck T et al. Traumatic memories, post-traumatic stress disorder and serum cortisol levels in long-term survivors of the acute respiratory distress syndrome. Brain Research 2009; 1293: 114–120
[26] Aitken LM, Bucknall T, Kent B et al. Sedation protocols to reduce duration of mechanical ventilation in the ICU. Cochrane Systematic review 2016; 72 (2): 261–272
[27] Hepp U, Moergeli H, Buchi S et al. Post-traumatic stress disorder in serious accidental injury: 3-year-follow-up study. The British Journal of Psychiatry 2008; 192: 376–283
[28] Wintermann GB, Brunkhorst FM, Petrowski K et al. Stress disorders following prolonged critical illness survivors of severe sepsis. Critical Care Medicine 2015; 43 (6): 1213–1222
[29] Wintermann GB, Rosendahl J, Weidner K et al. The Journal of Nervous and Mental Disease 2017; 205 (10): 780–787
[30] Wade D, David R, Howell H et al. Identifying clinical and acute psychological risk factors for PTSD after critical care: A Systematic review. Minerva Anestesiologica 2013; 79 (8): 944–963
[31] Hauer D, Weis F, Kruseneck T et al. Traumatic memories, post-traumatic stress disorder and serum cortisol levels in long-term survivors of the acute respiratory distress syndrome. Brain Research 2009; 1293: 114–120
[32] Needham DM, Scales DC, Laupacis A et al. A systematic review of the Charlson comorbidity using Canadian administrative databases: a perspective on risk adjustment in critical care research. Journal of Critical Care 2005; 20 (1): 12–19
[33] Nydahl P, Dubb R, Hermes C et al. Tubustoleranz: Checkliste reduziert Unsicherheiten. PflegenIntensiv 2016; 4: 20–23
[34] Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin (DGAI) und Deutsche Interdisziplinäre Vereinigung für Intensiv und Notfallmedizin (DIVI). S3-Leitlinie Analgesie, Sedierung und Delirmanagement in der Intensivmedizin (DAS-Leitlinie 2015). AWMF-Register Nr.: 001/012
[35] Kress JP, Gehlbach B, Lacy M et al. The long-term psychological effects of daily sedative interruption on critically ill patients. American Journal of Respiratory and Critical Care Medicine 2003; 168 (12): 1457–1461
[36] Baron R, Binder A, Biniek R et al. Evidence and consensus based guideline for the management of delirium, analgesia, and sedation in intensive care medicine: Revision 2015 (DAS-Guideline 2015) – short version. German Medical Science 2015; 13: 1–42
[37] Deffner T. Konzeptuelle Überlegungen für die psychologische Arbeit auf ITSen. Anästhesiologie, Intensivmedizin, Notfallmedizin und Schmerztherapie 2017; 58: 248–258
[38] Nydahl P, Fischill M, Deffner T et al. Intensivtagebücher senken Risiko für psychische Folgestörungen: Systematische Literaturrecherche und Metaanalyse. Medizinische Klinik – Intensivmedizin und Notfallmedizin 2019; 114 (1): 68–76
[39] Schmidt K, Mühlberg J, Brunkhorst FM et al. Die Betreuung des Intensivpatienten ist mit der Entlassung nicht zu Ende: Post-ICU-Care. Intensiv News 2016; 1: 26–28
[40] Porhomayon J, El-Solh AA, Adlparvar G et al. Impact of Sedation on Cognitive Function in Mechanically Ventilated Patients. Lung 2016; 194: 43–52
[41] Strøm T, Martinussen T, Toft P. A protocol if no sedation for critically ill patients receiving mechanical ventilation: a randomised trial. The Lancet 2010; 375: 475–480
[42] Universitätsklinikum Freiburg. Wache ITS: Bei vollem Bewusstsein. Das Magazin: Behandlung – Forschung – Lehre 2016; 2: 3–4
[43] Saxe GN, Stoddard FR, Courtney D et al. Relationship between acute Morphine and the course of PTSD in Children with burns. Journal of the American Academy of Child & Adolescent Psychiatry 2009; 40 (8): 915–921
[44] Deffner T, Schönle J, Neyer FJ et al. Erfassung des psychischen Befindens von Patienten auf der ITS: Vorschlag für eine deutsche Version des Intensive Care Psychological Assessment Tool. Medizinische Klinik – Intensivmedizin und Notfallmedizin 2020; 2: 140–147
[45] Kluge S, Heringlake M, Janssens U et al. DIVI Jahrbuch 2019/2020: Fortbildung und Wissenschaft in der interdisziplinären Intensivmedizin und Notfallmedizin – Schwerpunkt: „Psychische Belastung und Resilienz“. Berlin: Medizinisch Wissenschaftliche Verlagsgesellschaft; 2019
[46] Gawylatta R, Wintermann GB et al. PTBS nach Intensivtherapie. Medizinische Klinik-Intensivmedizin und Notfallmedizin 2019; 114: 9–14
[47] Starostzik C. Seelentrauma auf der ITS: PTBS bei jedem fünften Patienten. MMW: Fortschritte der Medizin 2013; 155 (30): 30