Katheter-assoziierte Infektionen Rund 20 Prozent aller auf Intensivstationen erworbenen Infektionen sind Gefäßkatheter-assoziierte Sepsen. Präventions- maßnahmen müssen darauf abzielen, deren Auftreten komplett zu vermeiden.
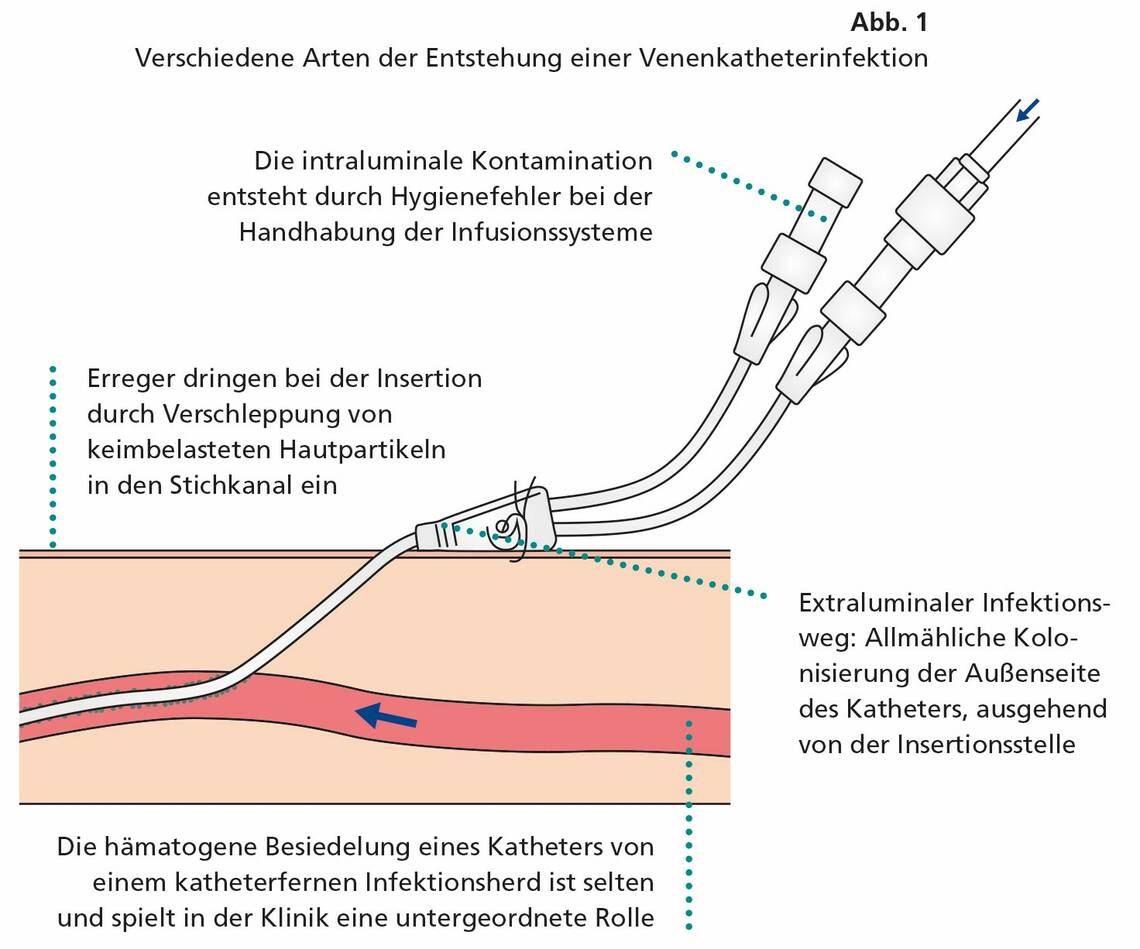
Voraussetzung für die Prävention Gefäßkatheter-assoziierter Infektionen ist die genaue Analyse der Infektionswege. Es sind vier Entstehungswege bekannt (Abb. 1):
- Die Erreger können bei der Insertion durch Verschleppung von keimbelasteten Hautpartikeln in den Stichkanal eindringen.
- Die Infektion erfolgt über die nachfolgende, allmähliche Kolonisierung der Außenseite des Katheters, ausgehend von der Insertionsstelle. Dieser Entstehungsweg wird als extraluminale Kontamination bezeichnet.
- Die intraluminale Kontamination entsteht durch Hygienefehler bei der Handhabung der Infusionssysteme, besonders aufgrund unzureichender Händedesinfektion beim Öffnen von Dreiwegehähnen.
- Ein seltener Entstehungsweg, der in der Klinik eine untergeordnete Rolle spielt, ist schließlich die hämatogene Besiedelung eines Katheters von einem katheterfernen Infektionsherd.
Die Bedeutung der ersten drei Infektionswege hängt stark von der Liegedauer der Katheter ab. Die Einschleppung von Bakterien zum Zeitpunkt der Insertion ist offenbar quantitativ so gering, dass sie sich erst nach mehrwöchiger Liegedauer in Form erhöhter Sepsis-Raten klinisch manifestiert. Bei kurzer Liegedauer von wenigen Tagen haben diese Wege, obwohl bereits gebahnt, eine nur geringe klinische Relevanz.
Die Rolle des luminalen Wegs wiederum hängt ganz von der Art des Umgangs mit den Systemen ab. Bei Verwendung von Handschuhen und Verzicht auf Sprechen bei Manipulationen am System spielt dieser Weg nur eine geringe Rolle.
Gezielt vorbeugen
Veränderungen des Hygieneverhaltens sowie eine verbesserte Organisation beim Legen und beim Umgang mit Kathetern gehören zu den grundlegenden Maßnahmen zur Infektionsprävention. Eine zentrale Bedeutung kommt der Einhaltung einer korrekten Händehygiene vor und nach jeder Manipulation am Katheter und den Komponenten des Infusionssystems zu.
Daneben sollte die Indikation des Katheters täglich neu überprüft werden.
In diesem Zusammenhang ist auch die Notwendigkeit, mehrere Lumina zu befahren, täglich zu hinterfragen. Wenn einzelne Lumina nicht mehr benötigt werden, sollte der Katheter so rasch wie möglich gezogen und an anderer Stelle ein neuer Katheter mit einer angepassten Zahl von Lumina neu gelegt werden. Ein „Stilllegen“ von Lumina für mehr als 24 Stunden ist zu vermeiden (1). Wenn eine Neuanlage zu risikoreich ist, müssen die nicht mehr benötigten Lumina durch sogenannte „Offenhalte“-Infusionen bedient werden.
Die sogenannten fünf Präventionsmaßnahmen sind Bestandteile des sogenannten Michigan-Bündels, einem an zahlreichen US-Kliniken zeitgleich implementierten Bündelprogramm, das über einen Zeitraum von fünf Jahren zu einer mehr als dreifachen Senkung der Rate Katheter-assoziierter Septikämien führte (2, 3).
Zu den fünf Präventionsmaßnahmen zählen:
- maximale sterile Barrieremaßnahmen beim Legen von zentralen Kathetern
- Vermeidung der Arteria femoralis als Insertionsstelle
- Desinfektion der vorgesehenen Insertionsstelle mit einem Chlorhexidin-haltigen Mittel
- Händehygiene beim Umgang mit dem Katheter,
- sofortige Entfernung von Kathetern bei nicht mehr vorliegender Indikation.
Dieses Bündelprogramm wurde zeitgleich an zahlreichen US-amerikanischen Krankenhäusern implementiert. In einem Zeitraum von fünf Jahren hat es zu einer mehr als dreifachen Senkung der Rate Katheter-assoziierter Septikämien geführt (2, 3).
Dass die Kombination mehrerer der oben genannten Einzelmaßnahmen und/oder weiterer Präventionsansätze in Form von sogenannten Bündeln die Rate Katheter-assoziierter Septikämien signifikant reduziert, konnte kürzlich in einer Meta-Analyse von klinischen Studien aus den letzten 25 Jahren belegt werden (4).
Neue Medizinprodukte verwenden
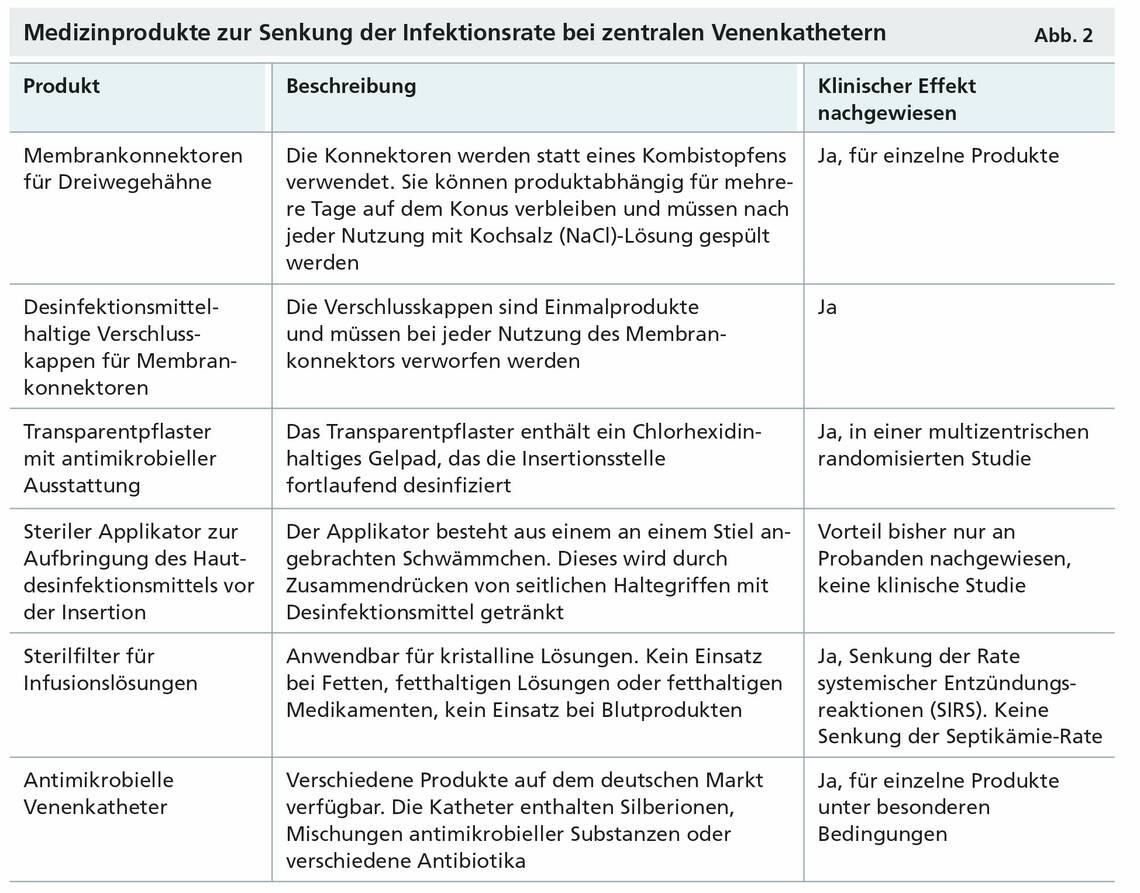
Neben den genannten Faktoren, die auf ein korrektes Hygieneverhalten abzielen, wurden in den vergangenen Jahren zahlreiche Medizinprodukte zur Anwendung am und im Katheter entwickelt (Abb. 2). Es handelt sich hierbei um Produkte, die die Desinfektion der Haut an der Insertionsstelle sowie von Dreiwegehähnen beziehungsweise „Hubs“ erleichtern.
Zudem existieren technische Entwicklungen, die die aseptische Anwendung von Parenteralia unterstützen. Im Einzelnen sind aufzuzählen:
- ein steriler Applikator zum Auftragen eines Alkohol-Chlorhexidin-Gemischs an der Insertionsstelle des Katheters (vor der Insertion),
- ein Transparentverband für die Insertionsstelle, der ein Chlorhexidin-haltiges Gelpad enthält,
- ein alkoholgetränktes Fertigtüchlein für die Desinfektion von Dreiwegehähnen und eine für den gleichen Zweck entwickelte Einweg-Verschlusskappe.
Zu allen genannten Produkten existieren Kohorten- oder günstigstenfalls randomisierte klinische Studien, die einen präventiven Effekt belegen.
Als Beispiel für eine sehr sinnvolle Art der klinischen Prüfung sei das Vorher-Nachher-Vorher-Konzept angeführt, das bei der klinischen Prüfung der oben bereits erwähnten antimikrobiellen Verschlusskappe für Dreiwegehähne angewandt wurde. Diese Verschlusskappe enthält ein mit 70 Prozent Isopropanol getränktes Schwämmchen, das bakterielle Kontaminationen auf Zuspritzöffnungen desinfizierend beseitigt.
Die Effektivität dieser Verschlusskappe wurde in einer klinischen Dreiphasen-Studie geprüft. In der Vorphase vor Einführung der Verschlusskappe betrug die Rate Venenkatheter-assoziierter Septikämien 1,43 pro 1 000 Venenkathetertage, nach Einführung ging sie auf 0,69 zurück. Nach Rückumstellung auf die konventionelle manuelle Desinfektion von Dreiwegehähnen stieg die Rate wieder auf 1,31 pro 1 000 Kathetertage an (5).
Antimikrobielle Katheter sinnvoll?
Eines der am häufigsten verwendeten und am längsten auf dem Markt existierenden Produkte sind antimikrobiell ausgestattete Venenkatheter. Ihre Entwicklung beruhte auf der Überlegung, dass jeder Venenkatheter-assoziierten Infektion eine Kolonisation des Katheters vorausgeht. Diese lässt sich für mindestens zwei bis drei Wochen unterdrücken, wenn der Katheter mit antimikrobiellen Substanzen ausgestattet ist.
Bei längerer Liegedauer werden die Substanzen meist ausgewaschen, sodass der Katheter dann seinen speziellen Effekt verliert und immer mehr einem „Normalkatheter“ gleicht. Da die Katheter deutlich teurer sind als Katheter ohne antimikrobielle Ausstattung, erhebt sich immer wieder die Frage, ob sie tatsächlich klinisch wirksam sind und ob sich aus ihrem Einsatz bei Gesamtbetrachtung aller Kosten ein Kostenvorteil ergibt.
In zwei kurz hintereinander an der Universitätsklinik Santa Cruz in La Laguna/Teneriffa durchgeführten Studien (8, 9) überprüften Intensivmediziner daher die Wirksamkeit und Kosteneffizienz antimikrobieller Katheter. Bei der ersten Studie handelte es sich um eine prospektive klinische Untersuchung an kardiochirurgischen und medizinischen Intensivpatienten (8). Die Patienten wurden entweder mit nicht antimikrobiell ausgestatteten Standard- Venenkathetern (Arrow, Firma Arrow, Reading/USA) oder mit dem CHSS-Katheter (ArrowguardR blue plus, ebenfalls Firma Arrow) versorgt. Die Abkürzung steht für: CH=Chlorhexidin (ein hautverträgliches Desinfektionsmittel), S = Silberionen (diese sind antimikrobiell wirksam), S = Sulfadiazin (ein Sulfonamid, also ein antibakteriell wirksames Chemotherapeutikum). Die drei Bestandteile sollen in der Kombination besser wirken, weil das anti- mikrobielle Spektrum erweitert wird. Die Bezeichnung „Plus“ bei dem antimikrobiellen Katheter bedeutet, dass er nicht nur außenseitig beschichtet, sondern bis zur Innenseite durchgängig mit den antimikrobiellen Substanzen imprägniert ist. Welcher Kathetertyp verwendet wurde, entschieden jeweils die vor Ort verantwort- lichen Ärzte. Die Diagnose einer Venenkatheter-assoziierten Sepsis wurde aufgrund folgender Kriterien gestellt, die jeweils alle erfüllt sein mussten:
- Positive Blutkultur von einer peripheren Abnahmestelle
- Zeichen der systemischen Infektion (z. B. Fieber, Schüttelfrost, Blutdruckabfall)
- Keine offensichtliche andere Quelle der Infektion außer dem Katheter
- Positive Katheter-Ausrollkultur mit ≥15 Kolonien pro Kathetersegment, dabei Nachweis des gleichen Erregers wie in der Blutkultur (beurteilt anhand der Spezies und des Antibiogramms).
Im Vergleich zu nicht antibakteriell ausgestatteten Kontroll- kathetern zeigte sich für CHSS-Katheter in beiden Studien ein signifikanter präventiver Effekt. CHSS-Katheter waren mit einer „Null-Rate“ Venenkatheter-assoziierter Septikämien assoziiert. Der Kostenvorteil war besonders deutlich, wenn die Basisrate Venenkatheter-assoziierter Septikämien relativ hoch war (5,04 pro 1 000 Katheterliegetage in der ersten Studie). Auch in der zweiten Studie, in der die Katheter-assoziierte Septikämie-Rate mit 2,12 Episoden pro 1 000 Venenkatheterliegetage niedrig war, ergab sich jedoch noch ein geringer Kostenvorteil.
Die aktuelle Leitlinie der US-amerikanischen Infektiologen- und Hygienegesellschaften (10) empfiehlt den Einsatz von antimikrobiellen Kathetern, wenn:
- der einrichtungsintern fest- gelegte Zielwert der Venenkatheter-assoziierten Sepsis-Rate trotz Anwendung aller routinemäßig empfohlenen Präventionsmaßnahmen über längere Zeiträume nicht erreicht wur-de,
- es sich um Patienten mit sehr schwierigen Venenverhältnissen und bereits in der Vergangenheit wiederholt aufgetretenen Kathetersepsen handelt,
- die Patienten ein hohes Risiko haben, im Falle einer Kathetersepsis ernsthafte Komplikationen zu erleiden (z. B. eine Endokarditis oder Gefäßprotheseninfektion bei Zustand nach Klappen- oder Aortenoperation).
Vorsicht bei Membrankonnektoren
Produkte mit strittiger Wirksamkeit hinsichtlich der Infektionsprävention sind die sogenannten Membrankonnektoren, die dem Verschließen von Dreiwegehähnen dienen. Eine kürzlich publizierte Simulationsstudie an zahlreichen kommerziell erhältlichen Modellen zeigte, dass einige Produkte das Eindringen von Bakterien in das Katheterlumen effektiv über bis zu sieben Tage verhindern, während andere nach mehrfacher Benutzung ihre hygienische Barrierefunktion zunehmend verlieren (6).
Die letztgenannte Studie sollte daher beachtet werden, wenn die Verwendung eines solchen Konnektors in Erwägung gezogen wird. Modelle mit integrierter Nachspülfunktion sollten möglichst vermieden werden, da sie eine flüssigkeitsgefüllte Kammer enthalten, in der sich Erreger vermehren können (7). Ebenso wird die Verwendung von Inline-Sterilfiltern immer noch kontrovers diskutiert. Ihre Verwendung macht jedoch unbedingt Sinn, um die Partikelbelastung des Intensivpatienten zu reduzieren. Fetthaltige Lösungen und Blutprodukte müssen jedoch in jedem Fall proximal des Filters, also patientenseitig, appliziert werden.
Helfen Octenidin- getränkte Waschtücher?
Seit einigen Jahren wird auf vielen Intensivstationen in den USA ein neues Konzept zur Infektionsprävention umgesetzt.
Es beinhaltet den Verzicht auf ein mikrobiologisches Screening neu aufgenommener Intensivpatienten. Stattdessen werden alle Patienten, unabhängig von ihrem Besiedlungsstatus, täglich mit Chlorhexidin-getränkten Waschtüchern abgerieben. In einer Studie auf Intensivstationen an der Ostküste der USA wurde mit diesem Vorgehen eine Reduktion nosokomialer Blutstrominfektionen um 31,1 Prozent nachgewiesen (11).
Im Gegensatz zu den USA, wo Chlorhexidin für die Anwendung in „Arzt“-Seifen und Hautdesinfektionsmitteln ubiquitär verbreitet ist, werden in Deutschland vielfach Präparate auf der Basis von Octenidin-Dihydrochlorid, kurz Octenidin, verwendet.
Aus diesem Grund überprüfte das Institut für Hygiene und Umweltmedizin der Charité – Universitätsmedizin Berlin, ob sich gleichartige Effekte auch einstellen, wenn mit Octenidin-haltigen Waschtüchern gewaschen wird.
Bei Gesamtbetrachtung aller 17 Intensivstationen zeigte sich in der Interventionsperiode keine Absenkung der Rate nosokomialer Blutstrominfektionen. Die Rate neu erworbener Besiedlungen beziehungsweise Infektionen mit MRSA ging von 0,97 auf 0,70 pro 1000 Patientenliegetage zurück. Dieser Wert erreichte das Signifikanzniveau (p=0,05). Bei den übrigen (multi)resistenten Zielerregern ließ sich kein signifikanter Effekt darstellen.
Wurden medizinische und chirurgische Intensivstationen getrennt betrachtet, so zeigte sich ein signifikanter Rückgang nosokomialer Blutstrominfektionen auf medizinischen Stationen von 5,03 auf 3,98 Episoden pro 1 000 Patiententage (Reduktion um 21 %, p=0,02).
Der Effekt beruhte vorwiegend auf einer Reduktion von Blutstrominfektionen durch Koagulase-negative Staphylokokken (KNS). Die klinischen MRSA-Nachweise wurden auf diesen Stationen ebenfalls signifikant reduziert, von 1,23 auf 0,65 pro 1000 Patientenliegetage (p = 0,006). Auf den chirurgischen Stationen war demgegenüber kein Einfluss der Waschungen auf nosokomiale Blutstrominfektionen und klinische MRSA-Nachweise darstellbar (12).
Gesamtkonzept erforderlich
Der Einsatz aller genannter Interventionen sollte im Rahmen eines organisierten Konzepts erfolgen. Dieses muss allen beteiligten Mitarbeitern vorgestellt und durch Schulungen eingeübt werden. Hierfür eignen sich auch Posterkampagnen und Lehrvideos.
Die Ermittlung der eigenen Rate Katheter-assoziierter Sepsen sollte in standardisierter Form durch das Hygienefachpersonal erfolgen. Die ermittelten Daten sind mit Referenzraten – in Deutschland etwa mit Daten des KISS-Systems – zu vergleichen und in regelmäßigen Abständen an das Stationsteam zurückzumelden.
Die Unterstützung aller genannten Maßnahmen durch die Leitung der Abteilung trägt signifikant zum Erfolg aller Hygienekampagnen bei (4).
(1) Kommission für Krankenhaushygiene und Infektionsprävention. Prävention Gefäßkatheter-assoziierter Infektionen. Bundesgesundheitsbl 2002; 45: 907–924
(2) Pronovost P et al. An intervention to decrease catheter-related bloodstream infection in the ICU. N Engl J Med 2006; 355: 2725–2732
(3) Pronovost PJ et al. Sustaining reductions in catheter related bloodstream infections in Michigan intensive care units: observational study. Brit Med J 2010; 340: c309 (online)
(4) Ista B et al. Effectiveness of insertion and maintenance bundles to prevent central-line-associated bloodstream infections in critically ill patients of all ages: a systematic review and meta-analysis. Lancet Infect Dis February 18, 2016 (online)
(5) Wright MO et al. Continuous passive disinfection of catheter hubs prevents contamination and bloodstream infection. Am J Infect Control 2013; 41: 33–38
(6) Casey A et al. An in vitro comparison of microbial ingress into 8 different needleless iv access devices. J Infusion Nursing 2015; 38: 18–25
(7) Rupp ME et a. Outbreak of bloodstream infection temporally associated with the use of an intravascular needleless valve. Clin Infect Dis 2007;44: 1408–1414
(8) Lorente L et al. Chlorhexidine-silver sulfadiazine-impregnated venous catheters save costs. Am J Infect Control 2014; 42: 321–324
(9) Lorente L et al. Efficiency of chlorhexidine-silver sulfadiazine-impregnated venous catheters at subclavian sites. Am J Infect Control 2015; 43: 711–714
(10) Marschall J et al. Strategies to pevent central line–associated bloodstream infections in acute care hospitals: 2014 update. Infect Control Hosp Epidemiol 2014; 35: 753–771
(11) Climo MW et al. Effect of daily chlorhexidine bathing on hospital-acquired infection. New Engl J Med 2013; 368: 533–542
(12) Gastmeier P et al. An observational study of the universal use of octenidine to decrease nosocomial bloodstream infections and MDR organisms. J Antimicrob Chemother 2016; doi10.1093 (online)