Sie ist Alltag auf jeder Intensivstation: die Blutgasanalyse. In erster Linie gibt sie Aufschluss über die im Blut gelösten Gase, was eine Bewertung der Lungenfunktion zulässt. Doch es lassen sich noch viele weitere wertvolle Informationen gewinnen.
Welches Blut für die Blutgasanalyse (BGA) genutzt wird, hängt in erster Linie davon ab, welche Information gewonnen werden soll.
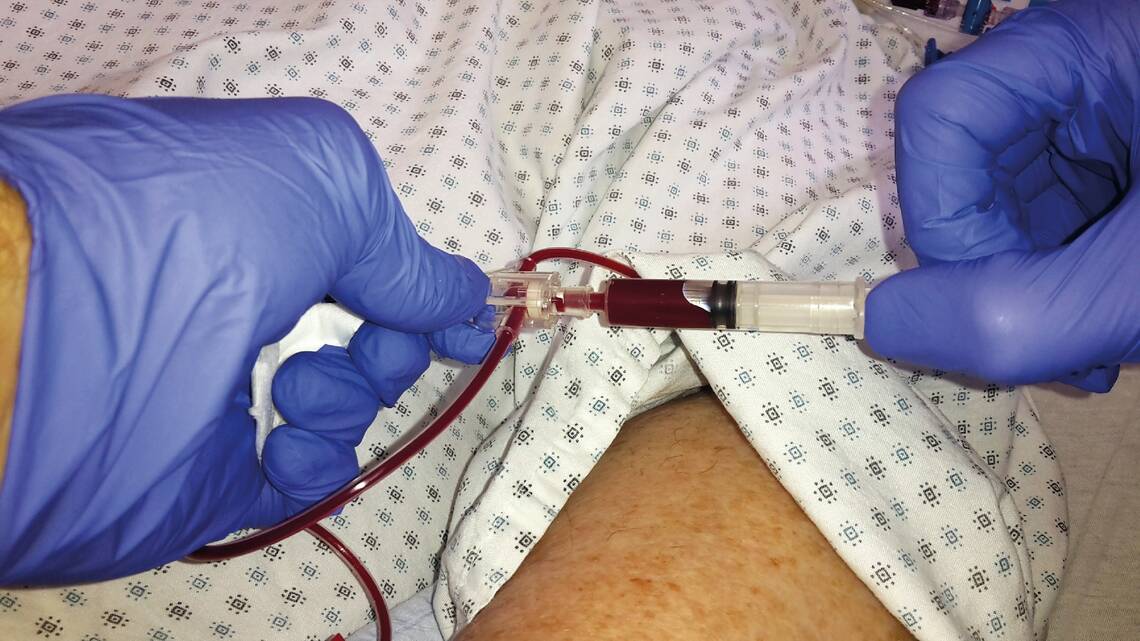
Um eine Aussage über die Lungenfunktion zu erhalten, wird normalerweise eine arterielle Probe benötigt. Hierzu wird entweder eine periphere Arterie punktiert oder die Probe wird aus einem liegenden arteriellen Katheter entnommen. Das arterielle Blut stammt „frisch“ aus der linken Kammer und wurde von dort aus in den Körper gepumpt, bis hin zur Stelle der Probeentnahme.
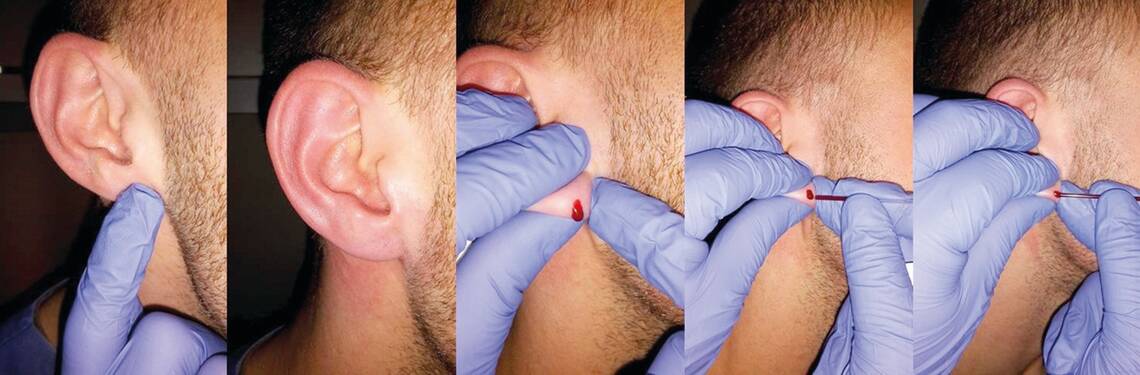
Auch der pH-Wert wird am ehesten aus einer arteriellen Probe bestimmt, da das Kohlendioxid soeben aus dem Kreislauf entfernt wurde. Liegt kein arterieller Katheter, wird häufig auf arterialisierte Proben aus Kapillarblut zurückgegriffen. Denn eine arterielle Punktion ist sowohl schmerzhaft als auch technisch anspruchsvoll. Kapillarblut kann aus dem Ohrläppchen oder der Fingerbeere gewonnen werden.
Vor der Entnahme wird die Punktionsstelle erwärmt oder mit einer durchblutungsfördernden Salbe eingerieben, zum Beispiel mit Finalgon®. Nach etwa zehn Minuten Einwirkzeit ist das Blut „arterialisiert“. Dann entsprechen die darin gelösten Elektrolyte, Gase und der pH-Wert durch die wärmeinduzierte Gefäßerweiterung in etwa arteriellem Blut. Die Probe wird in extra dafür vorgesehene heparinisierte Glas- kapillare aufgenommen. Dabei sollte das Entnahmegewebe nicht zu sehr gequetscht werden, da sonst zu viel Kalium aus den Zellen geschwemmt werden kann.
Elektrolyte, Blutzucker, Laktat, Hämoglobin und Hämatokrit können problemlos aus jeder Probe bestimmt werden; hier spielt der Punktionsort eine untergeordnete Rolle.
Informationen über den Flüssigkeitshaushalt gewinnt man am ehesten aus einer zentralvenös gewonnenen Blutprobe. Ist der zentralvenöse Sauerstoffgehalt gesenkt, kann dies als Zeichen für eine reduzierte Sauerstoffversorgung gewertet werden. Entweder ist zu wenig Sauerstoff verfügbar oder die Sauerstoffträger – das Blut – zirkulieren nicht häufig genug, was auf einen Flüssigkeitsmangel schließen lässt. Die Blutprobe sollte dann zeitnah nach der Entnahme zur Analyse gebracht werden.
Neben dem Punktionsort ist entscheidend, ob der Patient zum Zeitpunkt der Probenentnahme spontan atmet oder beatmet wird. Eine BGA sollte immer – wenn es der Patient toleriert – ohne Sauerstoffapplikation erfolgen. Denn nur so kann die tatsächliche Funktion der Lunge beurteilt werden.
Mit der BGA lässt sich auch die Effektivität der Sauerstofftherapie überprüfen. Auf dem BGA-Ausdruck wird der Sauerstoffgehalt als inspiratorischer Sauerstoffanteil, kurz FiO2, angegeben. Eine FiO2 von 0,2 Liter bedeutet, dass die Messung bei Raumluft mit einem Sauerstoffanteil von 21 Prozent erfolgte. Eine FiO2 von 1,0 bedeutet, dass der Patient bei der Messung 100 Prozent reinen Sauerstoff eingeatmet hat.
Was die BGA verrät
Im intensivmedizinischen Alltag lassen sich über die BGA weitere vielfältige Informationen generieren, die für die Behandlung der Patienten wichtig sind.
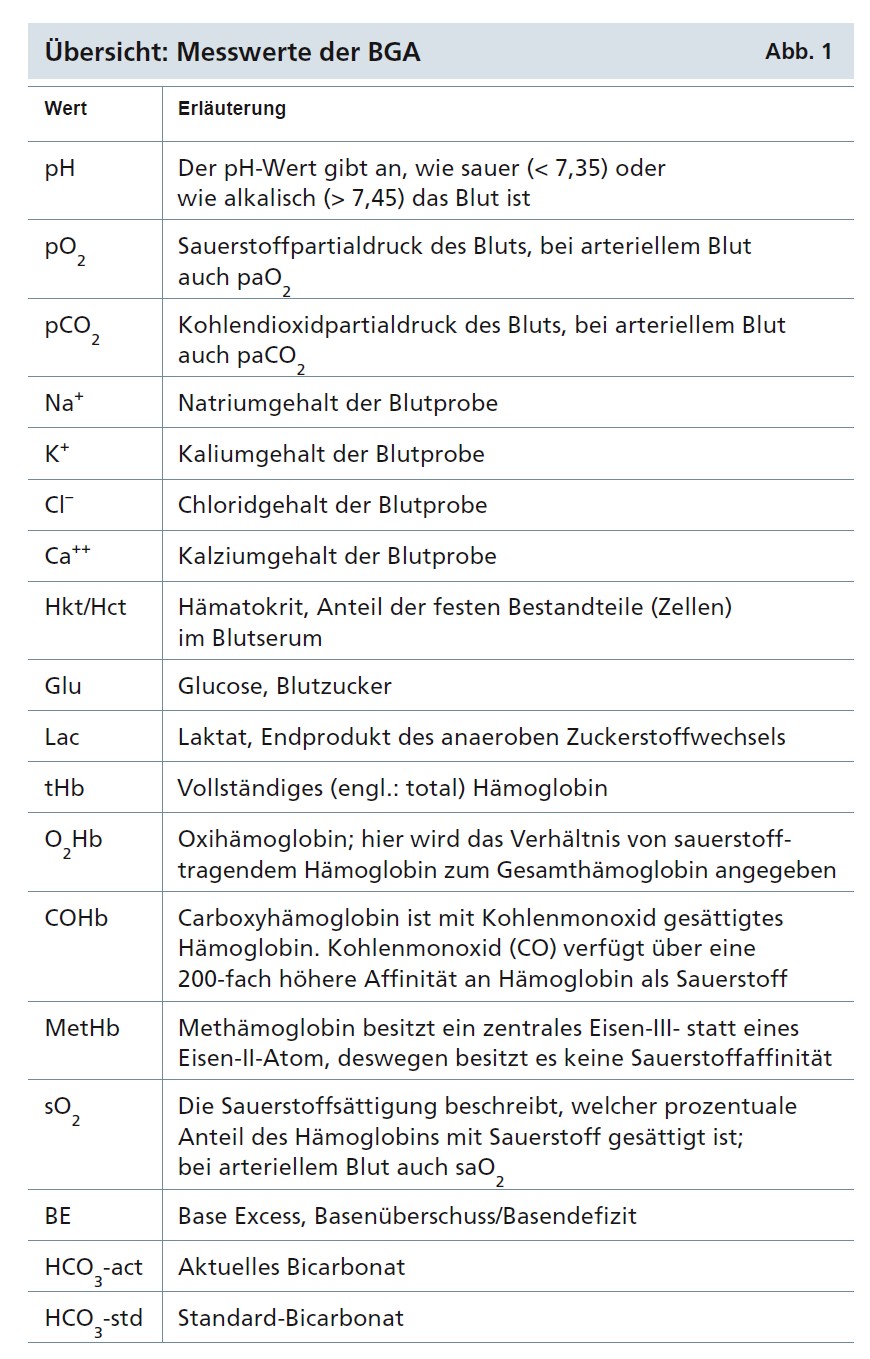
Atemstörungen: Die Blutgaswerte ermöglichen eine sofortige Einschätzung der Lungenfunktion. Hierzu zählen der partielle Sauerstoffdruck, der als pO2 angegeben wird, und der partielle Kohledioxiddruck, der sich hinter dem Kürzel pCO2 verbirgt. Weichen die Werte von den normalen Sauerstoff- und Kohlendioxid-Partialdrücken ab, ist dies in der Regel immer durch eine Veränderung der Atmung oder Beatmung erklärbar. Krankheitsbedingte Veränderungen werden in partielle und globale Ateminsuffizienzen unterteilt. Partiell steht für eine teilweise, global für eine vollständige Atemstörung.
Als respiratorische Partialinsuffizienz bezeichnet man eine isolierte Senkung des Sauerstoffpartialdrucks. Verursacht werden kann die sogenannte Hypoxämie durch Lungenödeme, -emphyseme, -fibrosen oder -embolien. Krankheitsbedingt diffundiert dann entweder nur noch ein Teil des Sauerstoffs durch die Alveolen oder aber die Kapillaren werden weniger durchblutet. Durch die Applikation von Sauerstoff kann der Partialdruck normalerweise adäquat erhöht werden.
Führt die Applikation nicht zur Erhöhung des Partialdrucks, ist von einer anatomischen Veränderung auszugehen: Möglich ist etwa ein Loch im Herzvorhof. Durch dieses Loch im rechten Herzvorhof fließt das sauerstoffarme Blut direkt in den linken Vorhof. Die zusätzliche Sauerstoffgabe führt nicht zur Verbesserung, da das Blut die Lunge damit umgeht.
Von einer respiratorischen Globalinsuffizienz spricht man bei vorliegender Hypoxämie mit gleichzeitiger Hyperkapnie, also einem erhöhten Kohlendioxidwert im Blut. Ursache hierfür ist in der Regel ein verminderter Atemantrieb, ausgelöst beispielsweise durch ein Schädel-Hirn-Trauma, eine Opiatvergiftung, ein Versagen der Atemmuskulatur bei Muskelerkrankungen oder Lungenkrankheiten im fortgeschrittenen Stadium, zum Beispiel bei einer Chronisch obstruktiven Bronchitis (COPD).
Eine besondere Aussage über die Lungenfunktion trifft der sogenannte Oxygenierungsindex oder Horovitz-Quotient. Dieser berechnet sich aus dem arteriellen Sauerstoffpartialdruck (paO2) und dem inspiratorischen Sauerstoffanteil (FiO2). Beim gesunden Menschen beträgt dieser Quotient um die 500 mmHg. Errechnet sich ein Wert zwischen 200 und 300, liegt eine leichte, zwischen 100 und 200 eine moderate und unter 100 eine schwere Lungenfunktionsstörung vor.
Veränderungen im Säure-Basen-Haushalt: Die BGA zeigt neben Atembeeinträchtigungen auch Veränderungen im Säure-Basen-Haushalt an. Während in der Chemie ein pH-Wert von 7,0 als „pH-neutral“ bezeichnet wird, liegt der mittlere pH-Wert des Bluts bei 7,4. Bei Werten unter 7,35 gerät das Blut in den sauren Bereich, was als Azidose bezeichnet wird. Bei Werten über 7,45 wird das Blut basisch, auch Alkalose genannt. Azidosen führen zu reduzierter Aktivität des Zentralen Nervensystems (ZNS) und zu geringerer Sympathikusaktivität. Anfangs wirkt der Patient lethargisch und desorientiert, später komatös. Bei einer Alkalose sinkt der Kaliumspiegel im Blut, der zerebrale Blutfluss ist eingeschränkt. Es kommt zu einer Übererregbarkeit des ZNS, gesteigerten Reflexen und eventuell zu Krämpfen.
Die Veränderungen des pH-Werts unterliegen einem Zusammenspiel von Kohlendioxid (CO2), Wasser (H2O) und Bikarbonat (HCO3-). Das Kohlendioxid muss sich im Blut an Wasser binden, wodurch Kohlensäure (H2CO3) entsteht. Zerfällt diese Verbindung, entstehen Protonen (H ) und Bikarbonat. Je mehr freie Protonen in einer Flüssigkeit vorhanden sind, desto niedriger also saurer ist der pH-Wert.
Am Säure-Basen-Haushalt sind neben der Lunge auch Niere und Leber beteiligt. Die Leber wandelt anfallendes Bikarbonat zu Harnstoff um, der über den Urin ausgeschieden wird. Reduziert die Leber also die Harnstoffproduktion, verfügt der Körper über mehr Bikarbonate, um anfallende Protonen zu eliminieren. Die Niere kann anfallende Protonen auch direkt eliminieren.
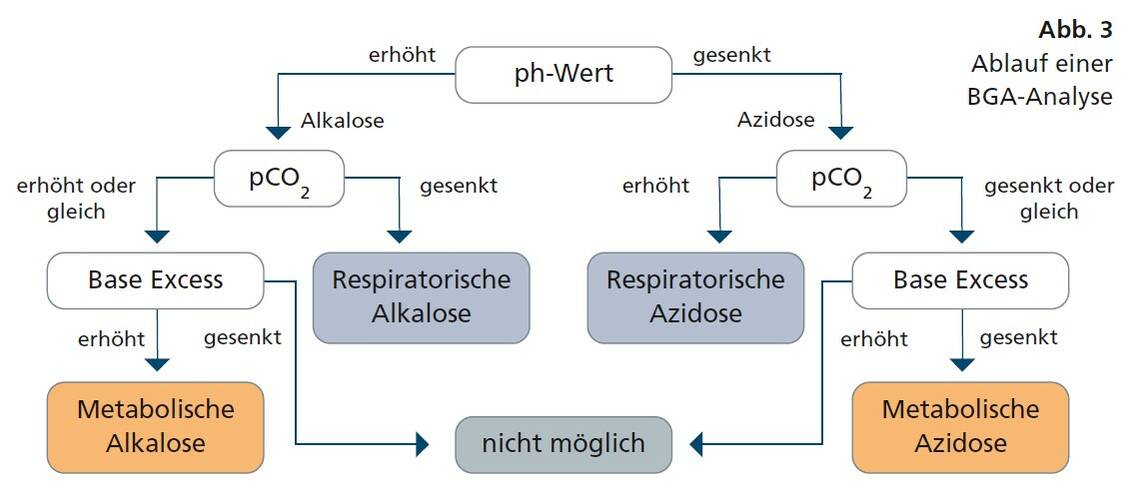
Neben der Differenzierung von Azidose und Alkalose werden die Veränderungen des pH-Werts auch anhand ihrer Ursache unterschieden. Liegt als Ursache eine Atembeeinträchtigung vor, spricht man von einer respiratorischen Störung. Diese ist am ehesten durch eine Veränderung des Kohlendioxid-Partialdrucks zu erkennen. Wird die Veränderung des pH-Werts durch Stoffwechselprozesse ausgelöst, spricht man von einer metabolischen Störung. Sie sind primär durch Veränderungen des Bikarbonat-Werts zu erkennen.
Respiratorische Störungen: Die Hyperventilation ist eine beispielhafte Ursache für eine Erhöhung des pH-Werts. Dabei wird über die Lunge vermehrt CO2 abgeatmet, der pCO2 sinkt und es kann weniger Kohlensäure (H2CO3) gebildet werden. Infolgedessen stehen dem Körper weniger Protonen und Bikarbonate zur Verfügung. Der pH-Wert steigt, es entsteht eine respiratorische Alkalose. Ein Gegenbeispiel ist Hypoventilation nach Opiatintoxikation. Die Opiate reduzieren den Atemantrieb, CO2 wird vermindert abgeatmet und reichert sich an. Der pCO2 steigt, es entstehen vermehrt Kohlensäure und deren Zerfallsprodukte. Dementsprechend sinkt der pH-Wert, wodurch es zu respiratorischen Azidose kommt. Sind pCO2 und pH gegensinnig verändert, handelt es sich also um eine respiratorische Störung.
Metabolische Störungen: Eine metabolische Alkalose wird durch Ansammlung von Basen oder den Verlust von Säuren verursacht. Ein Beispiel hierfür ist der Verlust von Magensäure durch Erbrechen. Die metabolische Azidose wiederum entsteht durch ein Überangebot von Säuren oder einen Mangel an Basen. Hierfür kommen eine Laktat- oder Ketoazidose, beispielsweise bei Diabetikern, infrage. Sind pCO2, pH-Wert und Base Excess (BE) gleichsinnig verändert, handelt es sich um eine metabolische Störung.
Kombinierte Störungen: Tritt eine pH-Wert-Veränderung im Blut auf, versucht der Organismus, diese wieder zu neutralisieren. Respiratorische Störungen werden ausgeglichen, indem der Körper versucht, mehr oder weniger Bikarbonate oder Protonen auszuscheiden. Metabolische Störungen werden durch eine schnellere oder langsamere Atmung ausgeglichen. Bei neutralem pH-Wert spricht man von einer kompensierten, sonst von einer teilkompensierten Störung. Grundsätzlich erfolgen die respiratorischen Kompensationsmechanismen schneller als die metabolischen. Außerdem besteht die Möglichkeit kombinierter respiratorischer und metabolischer Azidosen oder Alkalosen. In diesen Fällen begründen sich die pH-Wert-Veränderungen sowohl metabolisch als auch respiratorisch. Hier ist der Körper in einer dringenden Notfallsituation, da der Kompensationsmechanismus ausgefallen ist. Bei normalem pH-Wert und verändertem pCO2 und/oder Base Excess (BE) liegt eine kombinierte Störung vor. Der BE beschreibt die Abweichung der Basen vom Normalzustand. Ist der BE verändert, muss von einer metabolischen Störung ausgegangen werden. Bei einem normalem BE liegt eine respiratorische Störung vor. Ein erhöhter pH-Wert kann nicht logisch mit einem verminderten BE überein gebracht werden. Ebenso wenig ein gesenkter pH-Wert mit einem erhöhten BE.
Die Sauerstoffsättigung muss mit Blick auf die zugrunde liegende Blutprobe bewertet werden. Bei der arteriellen Probe sollten – ein ausreichender pulmonaler Gasaustausch vorausgesetzt – 90 bis 96 Prozent des Hämoglobins mit Sauerstoff gesättigt sein. Bei einer zentralvenösen Blutprobe sollte der Wert noch bei 70 bis 75 Prozent liegen. Der Sauerstoffverbrauch läge hier bei 25 bis 30 Prozent. Würde das Gewebe mehr Sauerstoff benötigen, käme es jedoch nicht zur weiteren Ausschöpfung des vorbeifließenden Bluts. Der erhöhte Bedarf würde zunächst durch eine Erhöhung des Sympathikotonus und damit des Herzzeitvolumens ausgeglichen. Erst wenn die Steigerung des Herzzeitvolumens ausgereizt ist, beginnt die zentralvenöse Sättigung zu sinken. Umgekehrt bedeutet dies auch, dass bei gleichbleibendem Sauerstoffverbrauch eine gesenkte zentralvenöse Sauerstoffsättigung immer mit einer unphysiologischen Veränderung des Herzzeitvolumens einhergeht.
Gemessen oder berechnet?
Der pH-Wert und die Partialdrücke werden mit speziellen Elektroden direkt gemessen. Die meisten BGA-Geräte verfügen aktuell über eine sogenannte Oximetriemessung, um auch das Gesamthämoglobin, die verschiedenen Hämoglobinunterformen und die Sauerstoffsättigung direkt zu ermitteln. Durch die Analyse der gemessenen Werte sind die BGA-Geräte in der Lage, das Standardbikarbonat (HCO3-) und den Base Excess zu berechnen. Elektrolyte, Blutzucker und Laktat werden ebenfalls direkt durch sogenannte ionenselektive Elektroden gemessen. Zur Berechnung bestimmter Werte muss das Gerät zusätzlich den Luftdruck messen. Außerdem werden Körpertemperatur und Probenquelle zur korrekten Berechnung abgefragt. Sollten identische Werte gemessen und berechnet werden, empfiehlt sich immer in erster Linie die Betrachtung der gemessenen Werte.
Kosten nicht vergessen
Die BGA ist ein hervorragendes Mittel zur akuten Beurteilung der Lungenfunktion und des Säure-Basen-Haushalts. Umso schneller entsteht die Versuchung, auch einfache Bestimmungen, zum Beispiel des Hb-Werts oder der Elektrolyte, mittels einer BGA durchzuführen. Hier lauert der Teufel jedoch im Detail. Je nachdem, ob das Krankenhaus über ein eigenes Labor verfügt oder ob diese Diagnostik von einem externen Labor übernommen wird, fallen unterschiedliche Kosten an. Hier sollte immer eine gründliche Abwägung erfolgen, ob eine sofortige Vor-Ort-Diagnostik zwingend nötig ist oder ob die Laborwerte nicht doch abgewartet werden können.
Abdulla, W. (2007): Interdisziplinäre Intensivmedizin, 3. Auflage, München, Jena: Urban & Fischer
Menche, N. (2014): Pflege heute. 6. Auflage, München, Jena: Elsevier, Urban & Fischer
Roewer, N.; Thiel, H. (2013): Taschenatlas Anästhesie, 5. Auflage, Stuttgart: Thieme
Schaefer, R.; Kosch, M. (2005): Störungen des Säure-Basen-Haushalts – Rationale Diagnostik und ökonomische Therapie. Deutsches Ärzteblatt 102 (26), A1896–1899
Ullrich, L.; Stolecki, D.; Grünewald, M. (2010): Thiemes Intensivpflege und Anästhesie, 2. Auflage, Stuttgart: Thieme