Übersichtsartikel Eine aktuelle Studie aus Deutschland zeigt: Trotz aller medizinischen Fortschritte ist Sepsis nach wie vor eine lebensbedrohliche Erkrankung, insbesondere bei Patienten auf Intensivstationen. Die Sepsissterblichkeit ist sehr hoch. Um möglichst viele Menschenleben zu retten, kommt der Früherkennung der Sepsis die größte Bedeutung zu. Pflegende haben hier aufgrund des häufigen Patientenkontakts eine wichtige Bedeutung.
Anfang der 1970er-Jahre berichteten McCabe und Mitarbeiter erstmals über die erschreckend hohe Häufigkeit und Mortalität der Sepsis in den USA und erkannten diese als bedeutsames gesundheitspolitisches Problem (1). Dass sich daran wenig geändert hat, zeigt eine aktuelle epidemiologische Studie aus Deutschland: Im Rahmen der INSEP-Studie („Incidence of severe sepsis and septic shock in German intensive care units“) wurde das Auftreten von schwerer Sepsis und septischem Schock auf 129 Intensivstationen unterschiedlicher Fachdisziplinen in 95 Kliniken in Deutschland untersucht. Für das untersuchte Kollektiv von 11 883 Patienten konnte eine schwere Sepsis oder ein septischer Schock bei 1 503 Patienten (12,6 %) nachgewiesen werden. 860 Sepsisfälle (57,2 %) waren nosokomial und 643 (42,7 %) ambulant assoziiert. Die häufigsten Infektionen betrafen den Respirationstrakt (46,6 %), das Abdomen inklusive Gastrointestinaltrakt (28,7 %) und das harnableitende System (12,6 %).
Die Inzidenz der Sepsis betrug 11,76 pro 1 000 Intensivbehandlungstage. Die Letalität, die mit schwerer Sepsis und septischem Schock einherging, betrug 34,4 Prozent. Ein Multiorgandysfunktionssyndrom trat häufig bei Patienten mit schwerer Sepsis und septischem Schock auf (2).
Damit ist die Sepsis mit ihren unterschiedlichen Ausprägungsgraden hinsichtlich der Erkrankungsschwere trotz aller medizinischen Fortschritte in den vergangenen Jahren nach wie vor eine lebensbedrohliche Erkrankung mit annähernd gleichbleibender Letalität in deutschen Kliniken. Jährlich erkranken weltweit 20 bis 30 Millionen Menschen an Sepsis, was alle drei bis vier Sekunden zu einem Todesfall führt (3).
Pathophysiologie der Sepsis
Die Sepsis und der septische Schock werden entsprechend der 3. Internationalen Konsensus Konferenz als lebensbedrohliche Organdysfunktionen definiert, die durch eine fehlregulierte Wirtsantwort auf eine Infektion hervorgerufen werden. Dabei handelt es sich um eine lebensbedrohliche Erkrankung, bei der die Reaktion des Körpers auf eine Infektion zu einer Schädigung der eigenen Gewebe und Organe führt (4).
Mit Verschlechterung der Makro- und Mikrozirkulation und Zunahme zellulärer und metabolischer Störungen steigt das Risiko irreversibler Endorganschäden mit Multiorganversagen und Tod des Patienten. Die Pathogenese des septischen Multiorganversagens unterscheidet sich dabei nicht fundamental von nicht-infektiösen Schockursachen. Die Virulenz des Erregers, Komorbiditäten des Patienten, Lebensalter und Ernährungszustand haben Einfluss auf das Sterberisiko.
Die Epidermis und die Schleimhäute des Verdauungssystems, der Atemwege und der Harnwege stellen in der Regel wirkungsvolle Barrieren gegen pathogene Eindringlinge dar. Überwinden Erreger diese, steht das angeborene Immunsystem mit den Makrophagen, dendritischen Zellen, Monozyten, neutrophilen Granulozyten und natürlichen Killerzellen in der zweiten Reihe. Sie registrieren über verschiedene Rezeptorklassen ein breites Spektrum an Zucker- und Fettsäuremolekülen, sogenannte „pathogen-associated molecular patterns (PAMP)“, wie sie in Endo- und Exotoxinen oder auf der Oberfläche gewöhnlicher Erreger zu finden sind.
Eine ähnliche Kaskade kann durch Moleküle ausgelöst werden, die zum Beispiel aus zerstörtem oder nekrotischem Gewebe nach Trauma, bei Verbrennung, Pankreatitis oder nach Ischämie/Reperfusion freigesetzt werden – sogenannte „damage-associated molecular patterns (DAMP)“ (5). Je nach molekularer Struktur des Antigens produzieren Neutrophile und Makrophagen ein Zytokinmuster ähnlich einer Signatur, die mit Hilfe der dentritischen Zellen zur schnellen Immunantwort des adaptiven Immunsystems führt, das heißt zur Produktion von Immunglobulinen durch B-Plasmazellen sowie pro- und anti-inflammatorischen Zytokinen der T-Zellen (Th1, Th2) (6). Dieses führt zu einer kaskadenartigen Aktivierung von Gerinnungsfaktoren, Plättchenaktivierung, akute Phase-Proteinen, Stresshormonen, dem Arachnidonsäure- und Bradykinin-Kallekrein-System, die wiederum ein komplexes Netzwerk bilden. In der schweren Sepsis kommt es zu einem gestörten Gleichgewicht von pro- und antiinflammatorischen Mechanismen. Während in der frühen Phase eine überschießende pro-inflammatorische Immunantwort den Patienten akut gefährdet, kommt es in der späten Phase der Sepsis aufgrund von Apoptose und Anergie der Th1-Zellen häufig zu einem anti-inflammatorischen, immunsuppressiven Status (7).
Bakterielle Erreger vermehren sich unabhängig von ihrer Eintrittspforte im Gewebe oder in der Blutstrombahn. Ihre eingeschwemmten Endotoxine (Lipopolysaccharid) oder Exotoxine provozieren das klinische Bild einer Sepsis. So kann etwa die Invasion der Mikroorganismen in Media und Adventitia der Gefäße, die in der Subkutis verlaufen, zu einer nekrotisierenden Vaskulitis führen. Zytokine vermitteln zudem eine Steigerung der Gefäßpermeabilität und eine verstärkte Adhäsion von Leukozyten. Diese Prozesse unterstützen die Inflammationsreaktion im Gewebe. Weiterhin lösen sie Fieber aus und regen die Produktion von Akutphase-Proteinen an. Beeinflusst wird dieses Geschehen vermutlich auch durch eine Vielzahl weiterer Faktoren, wie der Virulenz der Erreger, der Komorbidität, des Ernährungszustands (Malnutrition oder Adipositas) sowie des Lebensalters der Patienten.
Die Entwicklung einer schweren Sepsis mit Übergang in einen septischen Schock mit Multiorgandysfunktionssyndrom (MODS) ist mit einer hohen Sterblichkeit behaftet. In Abhängigkeit von der Anzahl betroffener Organsysteme beträgt die Krankenhausletalität bei einfachem Organversagen circa 40 Prozent und beim drei- oder mehrfach Organversagen bis zu 80 Prozent (8).
Auch wenn die pathophysiologischen Mechanismen des MODS im Detail noch nicht vollständig aufgeklärt sind, wird die dysregulierte Aktivierung der Blutgerinnung als ursächlich angesehen. Dabei bewirkt der durch Entzündungsmediatoren induzierte Endothelzellschaden eine Gerinnungsaktivierung mit der Bildung von Mikrothromben, die zu diffusen Verschlüssen des peripheren Gefäßbettes führen, wodurch die systemische Entzündungsreaktion weiter verstärkt wird. Daraus resultiert eine fortschreitende Minderdurchblutung, die zu schwerwiegenden Einzel- oder Mehrfachorganversagen führen kann.
Insgesamt zeigen sich äußerst heterogene Ausprägungen einer Sepsis, schon allein aufgrund der vielen Grunderkrankungen, aus denen sie sich entwickeln kann. Nach wie vor fehlen einfache und eindeutige klinische Diagnosekriterien oder spezifische Laborparameter. Dementsprechend schwer fällt die Abgrenzung von anderen Krankheitsbildern sowie die Unterscheidung der verschiedenen Schweregrade einer Sepsis. Die Pathogenese der Sepsis ist somit ein durchaus kontrovers diskutierter Gegenstand der aktuellen Forschung. Um neue Ansatzpunkte und Strategien für die Therapie der Sepsis entwickeln zu können, ist ein fundamentales Verständnis der Ursachen und der Pathophysiologie des Multiorganversagens erforderlich.
Infektionen sind häufig die Ursache
Die Sepsis ist eine häufige Todesursache, und es ist zu erwarten, dass die Mortalität tendenziell eher weiter zunimmt. Gründe dafür sind (9):
- die allgemein steigende Lebenserwartung von Patienten,
- die deutliche Zunahme der Überlebenszeit chronisch kranker Menschen,
- die verbesserten Möglichkeiten der Intensivtherapie,
- die zunehmende Invasivität vieler diagnostischer und operativer Eingriffe,
- der zunehmende unkritische Einsatz von Antibiotika,
- die zunehmende Antibiotikaresistenz.
Die wichtigsten Eintrittspforten für die Erreger sind bei Krankenhauspatienten chirurgische Wunden, Urin- und Gefäßkatheter sowie alle anderen artifiziellen Zugänge. Allgemeine Faktoren wie Alter, Cortisonbehandlung, Diabetes oder konsumierende Grunderkrankungen sind prädisponierende Faktoren für eine Sepsis. Patienten mit einer schweren Neutropenie sind für Infektionen besonders anfällig. Bakterien aus oberflächlichen, lokalen Läsionen können in den Körper eindringen und zu einem septischen Geschehen führen. Allerdings kann über die Ursache der Infektionsquelle – endogen oder exogen – nur eine Aussage gemacht werden, wenn eine epidemiologische Untersuchung durchgeführt wurde. Kann eine endogene Infektion ausgeschlossen werden, müssen bei der Suche nach einer exogenen Quelle auch Ärzte und Pflegende in die Abklärungen einbezogen werden.
Nach der Untersuchung von Martin et al. waren in den USA von 1979 bis 1987 gram-negative Bakterien vorherrschend verantwortlich für das Entstehen einer Sepsis (10). Der Anteil gram-positiver Bakterien- sowie Pilzinfektionen nimmt seither stetig zu. So wurden im Jahr 2000 52,1 Prozent der septischen Krankheitsbilder durch gram-positive Erreger und nur noch 37,6 Prozent durch gram-negative Bakterien verursacht, was einem Anstieg der Inzidenz gram-positver Infektionen von 26,3 Prozent pro Jahr entspricht. Die Anzahl durch Pilzorganismen bedingter Sepsisfälle hat sich im Zeitraum von 1979 bis 2000 um 207 Prozent erhöht (10).
In einer einjährigen prospektiven Studie zur Erfassung von schweren Infektionen in einem deutschen Universitätsklinikum wurden 1997 bei 315 Patienten in 77,8 Prozent der Fälle nosokomiale Infektionen als Ursache gefunden. Nosokomiale Infektionen aufgrund intravasaler Fremdkörper waren am häufigsten (31 % aller Fälle). Über 70 Prozent der Patienten waren mit teilweise sehr lange liegenden Kathetern versorgt, und viele von ihnen waren entweder in intensivmedizinischer Betreuung oder standen unter Immunsuppression, was in beiden Fällen ein großes Infektionsrisiko darstellt. Die Sepsis-Inzidenz betrug 10,1 Fälle pro 1 000 aufgenommene Patienten.
Die hohe Inzidenz wird auf einen großen Anteil hämatologisch-onkologischer Patienten mit 22,5 Prozent zurückgeführt. Solide maligne Tumoren traten bei 18 Prozent der Patienten auf; insgesamt sieben Prozent der Patienten waren vor ihrer Aufnahme polytraumatisiert oder befanden sich in einem Zustand nach kardiopulmonaler Reanimation. Der Immunstatus dieser Patienten war ebenso beeinträchtigt wie der von 28 Prozent der Patienten, die eine immunsuppressive Therapie erhielten (11).
Alte Patienten besonders gefährdet
Die Epidemiologie der Sepsis bei älteren Patienten wurde in zwei US-amerikanischen Übersichtsarbeiten dargestellt (12, 13). Danach ist die Sepsis beim älteren Patienten nicht nur häufiger, sie haben auch ein anderes Erregerspektrum im Vergleich zu jüngeren Personen. Ältere Patienten über 65 Jahre erkranken 1,31-mal häufiger an einer Sepsis durch gram-negative Bakterien als jüngere Patienten mit Sepsis. Während bei jüngeren Patienten Staphylococcus aureus der häufigste Sepsiserreger ist, steht bei älteren Personen mit außerhalb des Krankenhauses erworbener Sepsis Escherichia coli an der ersten Stelle der Infektionserreger. Weitere häufig vorkommende gram-negative Erreger sind Enterobacter spp., Klebsiellen und Pseudomonas aeruginosa.
Die Ursache wird darin gesehen, dass bei älteren Personen oft ein liegender Harnblasenkatheter und eine dadurch verursachte Bakteriurie den Ausgangspunkt der Sepsis darstellen. Leibovici et al. untersuchten in einer Studie die Unterschiede im Erregerspektrum zwischen 60- und 79-jährigen und Patienten, die 80 Jahre und älter waren. Die Harnwege waren bei 50 Prozent der über 80-Jährigen die Eintrittspforte der Sepsis, im Vergleich zu lediglich 34 Prozent bei 60- bis 79-Jährigen (14).
Alle Bereiche des Immunsystems sind von den altersbedingten Veränderungen betroffen, wobei reduzierte Zellzahlen sowie Funktionsverluste bzw. gestörte Balancen das Auftreten von Infektionen erleichtern. Im Alter weisen neutrophile Granulozyten und Makrophagen nur noch eine reduzierte Phagozytosekapazität auf. Die Produktion von Immunmediatoren wie IL-1 oder TNFα durch die Makrophagen ist vermindert, auch die natürlichen Killerzellen verlieren mit dem Alter an Funktion, was die Zunahme der Sepsis bei diesen Patienten begründen kann. Das Alter gilt auch als unabhängiger Risikofaktor für das Auftreten einer Sepsis und das Versterben im Verlauf (15).
Nicht nur in den USA, auch in Deutschland gilt es als gesichert, dass in den nächsten Jahrzehnten der Anteil an älteren und alten Patienten durch die Demografie ansteigen wird. Somit sind auch weiter steigende Fallzahlen für Sepsis und septischen Schock zu erwarten. Ältere Patienten reagieren auf eine systemische Infektion mit einer weniger starken Entzündungs- und Abwehrreaktion. Stattdessen kommt es oft zu initial durchaus noch dezenten Organdysfunktionen, wie beispielsweise einer Eintrübung des Bewusstseins oder einer akuten Verwirrtheit, die gelegentlich sogar an ein Delir denken lässt. Durch die Kapillarschädigung in der Lungenstrombahn kann es zu einer Störung des Gastaustauschs kommen. Klinisch macht sich diese in einer Erhöhung der Atemfrequenz bemerkbar. Fieber und Leukozytose können dagegen bei diesen Patienten oft fehlen.
Neue internationale Sepsisdefinition
Der seit Jahrzehnten gebräuchliche Begriff der Septikämie beschränkte das Krankheitsbild auf fieberhafte klinische Zustände, bei denen eine positive Blutkultur vorlag. Im Jahr 1992 wurde der Bezug auf die Blutkultur als Diagnosekriterium verlassen. Stattdessen wurde durch den Intensivmediziner Roger Bone der Begriff des SIRS (Systemic Inflammatory Response Syndrome, systemische inflammatorische Reaktion) geprägt (16). Ein SIRS lag vor, wenn zwei oder mehr der folgenden Entzündungszeichen nachgewiesen wurden:
- Fieber oder Hypothermie (Körpertemperatur über 38 °C oder unter 36 °C)
- Tachykardie (Herzfrequenz über 90/min)
- Tachypnoe (Atemfrequenz über 20/min) oder PaCO2 unter 4,3 kPa (unter 32 mmHg)
- Leukozyten > 12 x 109/l (Leukozytose) oder < 4 x 109/l (Leukopenie) oder mehr als 10 % Stabkernige.
Eine Sepsis wurde nach Bone angenommen, wenn mindestens zwei SIRS-Kriterien erfüllt waren und zusätzlich der Nachweis einer Infektion erfolgt war oder der hochgradige Verdacht bestand. Eine schwere Sepsis war definiert als Sepsis plus Organversagen, wie etwa eine septische Enzephalopathie mit Vigilanzminderung und akuter Verwirrtheit, Dysfunktion von Nieren oder Lunge, arterielle Hypotension oder dergleichen. Ein septischer Schock erforderte die Kriterien der arteriellen Hypotension trotz adäquater Flüssigkeitszufuhr und die Notwendigkeit des Einsatzes eines Vasopressors zur Stabilisierung des Blutdrucks.
Die neue Sepsisdefinition wurde auf Initiative der Fachgesellschaften durch eine Arbeitsgruppe von 19 Klinikern und Grundlagenwissenschaftlern vorbereitet. An der Endfassung des Dokumentes arbeiteten Wissenschaftler von 31 weiteren Fachgesellschaften mit, die auch für die kürzlich erschienene Publikation mit verantwortlich zeichneten (4). In der Publikation begründen die Autoren die Notwendigkeit einer Neufassung der Sepsisdefinition. In der Internationalen Literatur und in der Liste der ICD-Codes (international code of diagnoses) finden sich zahlreiche verschiedene Begriffe und Codes zum Thema Sepsis. So wird unter anderem von septischem Syndrom, Systemic inflammatory Response Syndrome (SIRS), septic response oder Septikämie gesprochen.
Diese Begriffe werden oft für im Detail unterschiedliche Krankheitsbilder verwendet. Da ein singulärer diagnostischer Marker zum Nachweis der Sepsis fehlt, wird ein klinischer Kriterienkatalog benötigt, auf den sich die internationale wissenschaftliche Gemeinschaft einigen kann. Nach neueren pathophysiologischen Erkenntnissen liegt bei einer Sepsis immer eine Organdysfunktion vor. Dysfunktionen eines oder mehrerer Organe können zu Beginn des septischen Geschehens noch maskiert sein, bestimmen jedoch entscheidend die weitere Prognose. Die Aufnahme des Kriteriums „Organdysfunktion“ schien der Arbeitsgruppe daher für eine zukünftige Sepsisdefinition unabdingbar.
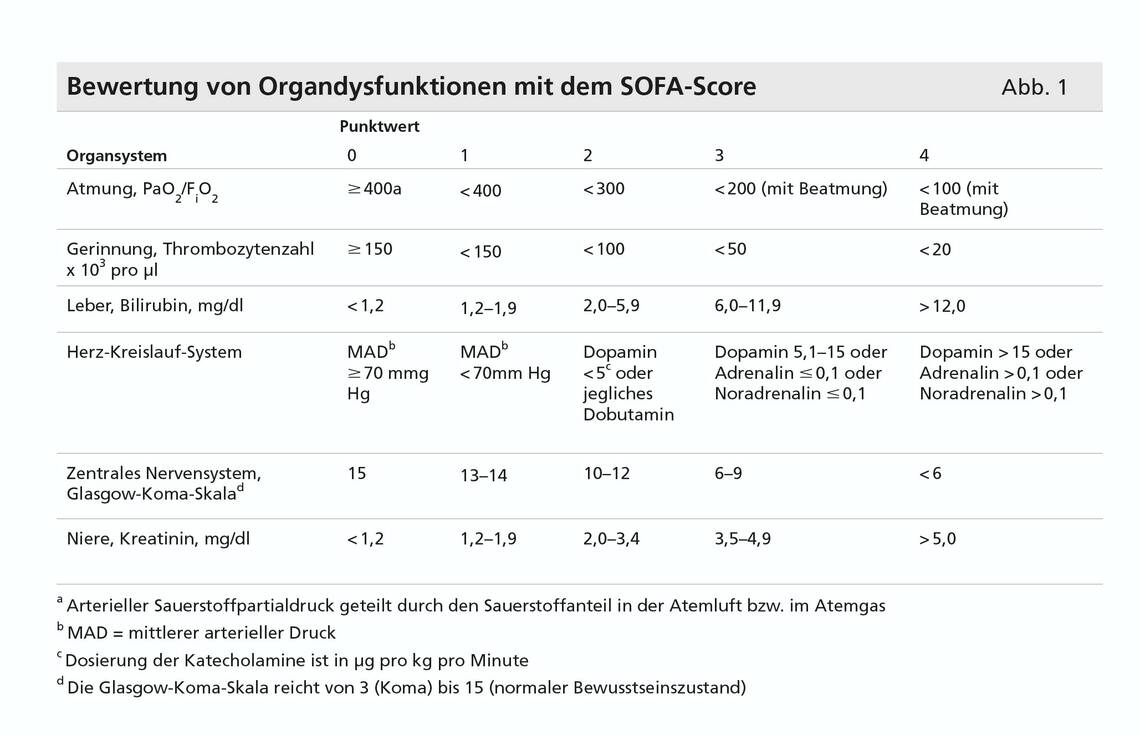
Die Arbeitsgruppe evaluierte verschiedene Möglichkeiten, um das Vorliegen von Organdysfunktionen objektiv zu erfassen. Sie kam zu der Auffassung, dass sich der seit den 1990er-Jahren etablierte SOFA-Score („Sepsis-related Organ Failure Assessment“) am besten dafür eignet. Es handelt sich um einen intensivmedizinischen Punkte-Score, der die in Abbildung 1 aufgeführten Parameter umfasst. Ab einem Punktwert von 2 im SOFA-Score steigt die Mortalität von Intensivpatienten nach Literaturerfahrungen auf circa zehn Prozent an. Dieser Wert ist höher als die Letalität eines akuten erstmaligen Herzinfarkts. Damit ist ein SOFA-Punktwert von 2 und höher in Verbindung mit den Zeichen einer akuten Infektion nach Auffassung der Autoren geeignet, eine schwere Sepsis von einer systemischen Inflammation abzugrenzen.
Früherkennung hat größte Bedeutung
Die Sepsis wird häufig zu spät diagnostiziert, weil Symptome wie Fieber, Tachykardie und beschleunigte Atmung und/oder Laborwerte wie Leukozytose/CRP unspezifisch sind, bei Patienten und medizinischem Personal häufig noch Unkenntnis und Unsicherheiten zur Sepsis besteht und anerkannte Behandlungsrichtlinien unzureichend umgesetzt werden. Bei Kindern bestehen häufig nur geringe Symptome, die sich dann plötzlich dramatisch verschlechtern. Bei älteren Menschen verläuft die Sepsis häufig larviert mit schleichendem Verlauf. Es zeigen sich oftmals kaum oder nur gering ausgeprägte klinische Symptome. Das Kardinalsymptom Fieber ist in über 30 Prozent der bakteriellen Infektion beim älteren Patienten nicht vorhanden (15). Infolgedessen führt die spätere Erkennung zu einer verzögerten Therapie und dem höheren Risiko von Komplikationen und Tod. Während das klinische Personal der Intensivstation häufig in der Erkennung geschult ist und Ärzte mit dem SOFA-Score zur Erfassung von Organdysfunktionen vertraut sind, ist im ambulanten Bereich und auf Normalstationen das Risiko, eine Sepsis zu verkennen, groß. Dabei kommt den Pflegekräften auf den Normalstationen eine Schlüsselfunktion bei der frühzeitigen Erkennung einer Sepsis zu, da sie den intensivsten Kontakt zu Patienten mit Allgemeininfekten haben.
Pflegewissenschaftliche Studien beschäftigen sich daher in den letzten Jahren mit der Frage, ob Pflegende Zeichen einer Sepsis frühzeitig erkennen können oder ob bestimmte klinische Konstellationen für sie schwierig zu interpretieren sind (17). Auf der Basis von 800 000 Patientenakten aus 177 Krankenhäusern wurde daher von Seymour et al. (18) ein Quick- SOFA-Score (qSOFA) entwickelt und validiert, der mit wenigen Kriterien die Erkennung einer Sepsis durch geschultes medizinisches Personal verbessern soll (Abb. 2). Bei einem Verdacht auf eine Sepsis oder klinischen Anzeichen für ein „septisches“ Geschehen muss sofort ein Arzt informiert werden. Jede neu aufgetretene akute Verwirrtheit sollte bis zum Beweis des Gegenteils an eine Sepsis denken lassen!
Schnell und zielorientiert handeln
Bei jedem Verdacht auf Sepsis müssen unabhängig von der Höhe der Körpertemperatur Blutkulturen abgenommen werden. Die Abnahme sollte vor Behandlungsbeginn oder am Ende eines Antibiotika-Dosierungsintervalls erfolgen. Mittels strikt aseptischer Gefäßpunktion sind mindestens 2 x 2, besser 3 x 2 Blutkulturpaare aus verschiedenen Entnahmeorten zu gewinnen. Neben der Anzahl der Blutkulturpaare (aerob und anaerob) ist auch die ausreichende Menge von 8–10 ml Blut pro Flasche (bei Erwachsenen) für eine erfolgreiche Erregerdetektion von Bedeutung. Bei Verdacht auf Endokarditis erhöht die Entnahme von zahlreichen Blutkulturen über einen Zeitraum von mehreren Stunden die Wahrscheinlichkeit der Keimidentifizierung.
Die Intensität der weiteren mikrobiologische Diagnostik richtet sich nach dem vermuteten Fokus, wie Liquorpunktion bei Meningitis, Atemwegssekret bei schwerer Pneumonie oder Gewebeproben und Abstriche bei Wundinfektionen.
Um ein rasches, strukturiertes Handeln zu erleichtern, führten Rivers und Mitarbeiter aus dem Universitätsklinikum von Detroit/USA ein standardisiertes Vorgehen für die ersten sechs Stunden nach der Diagnosestellung eines septischen Schocks ein. Die vorgeschlagenen Maßnahmen wurden 2012 von der internationalen Sepsiskampagne (Surviving Sepsis Campaign, SSC) mit leichten Modifikationen übernommen (Abb. 3). Im Wesentlichen sieht das Rivers-Konzept vor, die parenterale Gabe von Flüssigkeit und die Maßnahmen zur Optimierung des Sauerstoffangebots an festen physiologischen Zielwerten auszurichten. Für das Bündel werden heute üblicherweise die Begriffe „early goal directed therapy“ (EGDT, dt.: „frühe zielorientierte Therapie“) oder „Maßnahmenbündel der ersten sechs Stunden“ verwendet.
Zwei kürzlich publizierte Metaanalysen zeigten, dass ein wissenschaftlicher Beleg für das Konzept nach wie vor aussteht. Die erste dieser Metaanalysen wurde im April 2015 von Zhang und Mitarbeitern aus der Universitätsklinik von Sichuan in Westchina durchgeführt. Die Autoren recherchierten die verfügbare internationale Literatur aus einschlägigen medizinischen Datenbanken. Für den Zeitraum 2001 bis 2014 konnten sie zehn randomisierte kontrollierte Studien mit 4 157 Patienten auswerten. Einschlusskriterium in die Studie waren ein neu diagnostizierter septischer Schock oder eine schwere Sepsis. Der primäre Endpunkt war die Beeinflussung der Mortalität durch das Maßnahmenbündel innerhalb der ersten sechs Stunden (EGDT). Sekundäre Endpunkte waren die Dauer des Intensivaufenthalts und die Dauer der maschinellen Beatmung, der Einsatz von Katecholaminen und die Gabe von Bluttransfusionen. Die Metaanalyse ergab, dass Patienten, die eine EGDT erhielten, in den ersten sechs Stunden signifikant häufiger mit inotropen Substanzen behandelt wurden, häufiger parenterale Flüssigkeit sowie signifikant häufiger Erythrozyten-Konzentrate erhielten als Patienten unter Standardtherapie. Trotz dieser offensichtlich intensivierten frühzeitigen Therapiemaßnahmen kam es jedoch in den EGDT-Gruppen nicht zu einer deutlich geringeren Mortalität (19).
Eine zweite Metaanalyse zu dieser Thematik erschien 2015 (20). Die Autoren betrachteten lediglich fünf randomisierte Studien mit hoher methodischer Qualität. Auch sie konnten zeigen, dass die Krankenhausmortalität nicht signifikant zwischen den EGDT-behandelten und konventionell behandelten Gruppen differierte. Insgesamt kamen die Autoren jedoch zu der Schlussfolgerung, dass durch eine frühzeitige, zielorientierte Therapie des septischen Schocks das intensivmedizinische Management deutlich strukturierter abläuft. Da in beiden Metaanalysen ein Trend zu einer vorteilhaften Beeinflussung der Mortalität erkennbar war, befürworteten die Autoren daher den weiteren Einsatz dieses Maßnahmenbündels. Zusammenfassend ist die monozentrische Studie von Rivers sicher eine Meilensteinstudie zur frühen Therapie der schweren Sepsis und des septischen Schocks. Ihre Ergebnisse sind aber nicht ohne weiteres auf den klinischen Alltag zu übertragen. Die Zielparameter der EGDT (ZVD, MAD und ScvO2) sind willkürlich und nicht hinreichend durch klinische Studien validiert.
Aktuelle Daten belegen keinen Schaden, aber auch keinen Nutzen durch die EGDT. Eine durch klinische Erfahrung und Beurteilung geleitete Therapie ist in ihren Ergebnissen mit der EGDT vergleichbar. Eine möglichst frühzeitige protokollbasierte Diagnostik und Therapie, wie sie in den Sepsis-Bundles umgesetzt wird, sollte kontinuierlich weiterentwickelt und an die aktuellen Erkenntnisse angepasst werden.
Lactat-Clearance als Erfolgsmarker?
Aufgrund von Mikrozirkulationsstörungen mit eingeschränktem Sauerstofftransport durch die Gefäßmembranen kommt es bei der schweren Sepsis zu einer Sauerstoffunterversorgung wichtiger Organe und der Muskulatur auf zellulärer Ebene. Die Folge ist eine Zunahme des anaeroben Glucose-Abbaus, die an einem Anstieg des Plasma-Lactatwerts erkannt werden kann. Ein Plasma-Lactatwert von≥ 4 mmol/l (18 mg/dl) ist typisch für eine schwere Sepsis. Während Rivers und Mitarbeiter in ihren Studien den Plasma-Lactatwert zwar bestimmten, aber nicht als Zielparameter in das therapeutische Management einschlossen, integrierten nachfolgende Studiengruppen das Ziel einer Absenkung des Lactatwerts innerhalb der ersten Stunden der Sepsistherapie ebenfalls in ihren initialen Maßnahmenkatalog.
In einer Studie aus der Universitätsklinik in Hebei/China, konnte kürzlich an zwei kleinen Gruppen von je 25 Patienten der Erfolg der frühen Sepsistherapie unter Berücksichtigung der beiden Zielgrößen, Lactat-Clearance und zentralvenöse Sauerstoffsättigung, ermittelt werden (21). In der einen Gruppe wurde eine zentralvenöse Sauerstoffsättigung von über 70 Prozent als therapeutisches Ziel angesehen, in der anderen Gruppe wurde die Therapie mittels stündlich bestimmter Plasma-Lactatwerte gesteuert. Zielwert war eine Absenkung des initial gemessenen Lactatwerts um mindestens zehn Prozent in den ersten drei Stunden.
Es konnte gezeigt werden, dass sich die 28-Tage-Mortalität in den beiden Gruppen nicht signifikant unterschied. Der Lactatwert wurde von diesen Autoren daher als Alternative für die zentralvenöse Sauerstoffsättigung angesehen. Auch nachfolgende Autoren kamen zu der Überzeugung, dass sich die Lactat-Clearance als Marker für die Therapiesteuerung in den ersten Stunden eignet (22). Der Lactatwert sollte hierfür nach drei Stunden erneut ermittelt werden. Eine Pro- und Kontra-Diskussion zeigte aber, dass vermutlich beide Marker bestimmt werden müssen und sich am besten gemeinsam zur Therapiesteuerung eignen (23, 24).
Antibiotikatherapie so früh wie möglich
Da die Antibiotikatherapie so früh wie möglich eingeleitet werden sollte, können die Ergebnisse mikrobiologischer Kulturen nicht abgewartet werden. Selbst Schnelltests wie die molekulare Blutkultur, zum Beispiel der SeptiFast-Test, haben eine Bearbeitungszeit von zwei bis drei Stunden. Ihr Ergebnis kann somit allenfalls genutzt werden, um eine begonnene Therapie frühzeitig zu deeskalieren. Primär müssen jedoch Antibiotika oder Antibiotikakombinationen eingesetzt werden, die das zu erwartende Erregerspektrum einschließlich möglicher Erregerresistenzen optimal erfassen. Bei der Erhebung der Anamnese müssen somit die speziellen Risikofaktoren des Patienten für eine Infektion mit (multi-)resistenten Erregern abgefragt oder von Angehörigen eruiert werden.
Unbedingt ist auch eine gezielte Reiseanamnese zu erheben, zum Beispiel Aufenthalt in Malariagebieten. Bei der klinischen Untersuchung sollte größte Sorgfalt verwendet werden, den Sepsisherd möglichst organbezogen einzugrenzen. Die Antibiotikawahl sollte jedoch in jedem Fall den weiteren Ergebnissen aus der klinischen Diagnostik angepasst werden. Das Ansprechen auf die Antibiotikatherapie kann spätestens am Folgetag durch den klinischen Verlauf sowie die Entwicklung des Procalcitonin-Werts (PCT) beurteilt werden. Die Steuerung der Dauer einer antibiotischen Therapie bei kritisch kranken Patienten mit bakteriellen Infektionen kann durch den Biomarker Procalcitonin (PCT) unterstützt werden. Die Anwendung von PCT wird in den internationalen Sepsisleitlinien und in den deutschen Leitlinien zur Sicherung rationaler Antibiotika-Anwendung im Krankenhaus empfohlen. Verschiedene Studien und Metaanalysen konnten die effektive Verkürzung der antibiotischen Therapiedauer durch Anwendung von PCT-Protokollen ohne negative Effekte für das klinische Outcome der Intensivpatienten zeigen (24, 25, 26).
Millionen Sepsis-Todesfälle sind vermeidbar
Mit der Verabschiedung einer für alle Mitgliedsstaaten der Vereinten Nationen (United Nations, UN) verbindlichen Resolution „Verbesserung von Prävention, Diagnose und Management der Sepsis“ hat im Mai 2017 die Weltgesundheitsorganisation (World Health Organization, WHO) dem Problem Sepsis eine hohe Priorität eingeräumt. Die Sepsis-Resolution der WHO geht davon aus, dass die Mehrzahl der weltweit mindestens sechs Millionen Sepsis-Todesfälle pro Jahr vermeidbar ist.
Die WHO fordert die Mitgliedstaaten der UN dringend auf, Maßnahmen zur Senkung der sepsisbedingten Letalität umzusetzen, die geeignet sind, die Prävention, Diagnose und das Management der Sepsis zu verbessern. Konkrete Forderungen der Resolution sind (27):
- Verbesserung der Früherkennung durch die Nutzung des Wortes Sepsis,
- Steigerung der Aufmerksamkeit und Aufklärung über die Frühsymptome von Sepsis in allen medizinischen und gesellschaftlichen Bereichen,
- Steigerung der Impfraten bei Risikopopulationen gegen Influenza, Pneumokokken und andere Infektionen, die zur Sepsis führen können,
- Vermeidung von behandlungsassoziierten/nosokomialen Infektionen im Krankenhaus, in Pflegeeinrichtungen und im ambulanten Bereich durch Optimierung der Vorbeugungsmaßnahmen,
- Optimierung der Therapie mit Antibiotika durch gezielten, zeitgerechten Einsatz und Reduzierung von Antibiotikaresistenzen durch Vermeidung von missbräuchlicher Verordnung,
- Entwicklung effektiver Strategien zum Umgang mit Patienten, die mit multiresistenten Keimen infiziert sind, und effektives Management von Erregerausbrüchen multiresistenter Keime,
- Weiterentwicklung effektiver Vorbeugungs- und Eindämmungsstrategien für Pandemien und Epidemien,
- Nutzung und Verbesserung des ICD-Klassifikationssystems, um die Entwicklung der Sepsishäufigkeit und -sterblichkeit sowie der Antibiotikaresistenz zu verfolgen,
- Förderung der Sepsisforschung sowie Entwicklung von innovativen, effektiven Diagnostika und Therapeutika,
- Schaffung von geeigneten Versorgungsstrukturen für Überlebende einer Sepsiserkrankung.
Zusammenfassung: Die Sepsis-Mortalität hat sich in den vergangenen Jahren trotz Verbesserung antiinfektiver und intensivmedizinischer Therapien nicht wesentlich verändert und ist weiterhin beängstigend hoch.
Es ist herausfordernd, die Diagnose Sepsis zu stellen, da kein singulärer klinischer und Labor-Parameter zur Verfügung steht, der eine Sepsis im Frühstadium voraussagen könnte. Die Früherkennung der Sepsis durch eine entsprechende Vigilanz für das lebensbedrohliche Krankheitsbild mit der Identifikation des Infektfokus, dessen Sanierung und frühzeitiger Antibiotikatherapie sowie eine zügige zielorientierte Stabilisierung der Hämodynamik sind wesentliche Kernelemente der erfolgreichen Therapie.
Die Vorbeugung von nosokomialen Infektionen ist für viele Patienten entscheidend, da die meisten Fälle von Sepsis bis zum septischen Schock auf solche Infektionen zurückzuführen sind. Eines der vorrangigen Ziele ist die Senkung der Rate nosokomialer Infektionen durch Intensivierung von Hygienemaßnahmen; die primäre Vermeidung von Infektionen ist die Basis für eine Reduktion des Antibiotikaeinsatzes und damit ein fundamentaler Beitrag zur Verminderung des Antibiotikaresistenzproblems! Vor allem für Intensivpflegepatienten sollten daher alle effektiven Prophylaxe- und Therapiestrategien ausgeschöpft werden.
(1) Heublein S, Hartmann M, Hagel S, Hutagalung R, Brunkhorst FM (2013). Epidemiology of sepsis in German hospitals derived from administrative databases. 6th International Congress on Sepsis and Multiorgan Dysfunction, September 4–6 2013, Weimar. Infection 41 (1): Supp
(2) Marx G and the INSEP-Study Group (2015). Incidence of severe sepsis and septic shock in german intensive care units – the INSEP study. Intensive Care Medicine Experimental 3; Suppl 1: A223
(3) Welt Sepsis Deklaration (2013)
(4) Singer M, Deutschman CS, Seymour CW et al (2016). The Third International Consensus definitions for sepsis and septic shock (sepsis3). JAMA 315: 801–810
(5) Ildikó László, Domonkos Trásy, Zsolt Molnár, and János Fazakas. (2015) Sepsis: From Pathophysiology to Individualized Patient Care. Journal of Immunology Research. dx.doi.org/10.1155/ 2015/510436
(6) Russell, JA (2006). Management of Sepsis. N Engl J Med 355: 1699–1713
(7) Hotchkiss RS, Karl IE. The pathophysiology and treatment of sepsis. (2003) N Engl J Med. 348 (2):138–50
(8) Baue AE, Durham R, Faist E (1998). Systemic Inflammatory Response Syndrome (SIRS), Multiple Organ Dysfunction Syndrome (MODS), Multiple Organ Failure (MOF): Are we winning the battle? Shock 10:79–89
(9) Walmrath D, Grimminger F, Seeger W (2001). Schwere Sepsis – neue Therapieverfahren. Internist 42: 1619–1630
(10) Martin GS, Mannino DM, Eaton S, Moss M (2003). The epidemiology of sepsis in the United States from 1979 through 2000. N Engl J Med 348:1546–54
(11) Kainer DJ (1997). Sepsis im Universitätsklinikum Ulm – eine prospektive Studie zur computergestützten Infektionserfassung Dissertation zur Erlangung des Doktorgrades der Medizin der Medizinischen Fakultät der Universität Ulm
(12) Girard TD, Opal SM, Ely EW (2005). Insight into severe sepsis in older patients: From epidemiology to evidence-based management. Clin Infect Dis 40: 719–727
(13) Girard TD, Ely EW (2007). Bacteremia and sepsis in older adults. Clin Geriatr Med 23:633–647
(14) Leibovici L, Pitlik SD, Konisberger H, et al (1993). Bloodstream infections in patients older than eighty years. Age Ageing 22: 431–442
(15) Martin GS, Mannino DM, Moss M (2006). The effect of age on the development and outcome of adult sepsis. Crit. Care Med. 1:15–21
(16) Bone RC et al (1992). Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. Chest 101:1644–1655
(17) Santos PS, Tristram D (2015) A practical guide to the diagnosis, treatment and prevention of neonatal infections. Pediatr Clin North Amer 62:491–508
(18) Seymour CW, Liu VX, Iwashyna TJ, Brunkhorst FM et al (2016). Assessment of Clinical Criteria for Sepsis: For the Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA 315(8):762–74
(19) Zhang L, Zhu, G, Han L et al (2015). Early goal-directed therapy in the management of severe sepsis and septic shock in adults: a meta-analysis of randomized controlled trials. BMC Med 3;13:71
(20) Rusconi AM, Bossi I, Lampard JG, Szava-Kovats et al (2015). Early goal-directed therapy versus usual care in the treatment of severe sepsis and septic shock: a systematic review and meta-analysis. Intern Emerg Med 10:731–43
(21) Yu B, Tian HY, Hu ZJ, Zhao C et al (2013). Comparison of the effect of fluid resuscitation as guided either by lactate clearance rate or by central venous oxygen saturation in patients with sepsis. Zhong Hua Wei Jong Bing 25:578–83
(22) Jones AE (2011). Point: should lactate clearance be substituted for central venous oxygen saturation as goals of early severe sepsis and septic shock therapy? Yes. Chest 140:1406–8
(23) Rivers EP, Elkin R, Cannon CM (2011). Counterpoint: should lactate clearance be substituted for central venous oxygen saturation as goals of early severe sepsis and septic shock therapy? No. Chest 140:1408–13
(24) Zimmerli W, Trampuz A (2003). Pathogenese und Therapie der Sepsis. Schweiz Med Forum 35:811–818
(25) Koleff MH (2014). What can be expected from antimicrobial de-escalation in the critically ill? Intensive Care Med 40: 92–95
(26) Hohn A, Heising B, Schütte JK et al (2016). Procalcitonin-guided antibiotic treatment in critically ill patients. Langenbecks Arch Surg Online
(27) Rüdel H, Schwarzkopf D, Reinhart K. Zweiter Jahresbericht des Deutschen Qualitätsbündnisses Sepsis. Ein Projekt des Integrierten Forschungs- und Behandlungszentrum Sepsis und Sepsisfolgen – Center for Sepsis Control and Care am Universitätsklinikum Jena. Jena, April 2018
(28) Dellinger RP, Levy MM, Rohdes A, Annane D et al (2013). Surviving sepsis campaign: International guidelines for management of severe sepsis and septic shock: 2012. Crit Care Med 41:580–637