Die Anlage einer Ernährungssonde ist eine delegierbare ärztliche Tätigkeit. Wenn sie von Pflegenden ausgeführt wird, sind sie für die korrekte Durchführung verantwortlich. Um unerwünschte Ereignisse zu vermeiden, sind das Risiko- assessment und die Lagekontrolle wichtige Voraussetzungen.
Ernährungssonden erfüllen verschiedene therapeutische Zwecke (Panknin 2011). Pflegende stehen bei der Anlage einer Ernährungssonde in einem Zwiespalt. Denn einerseits müssen sie die adäquate Ernährung des Intensivpatienten gewährleisten, andererseits wissen sie um die Risiken, die bei der Anlage bestehen. Zudem kann sie bei Patienten Unwohlsein auslösen (Taylor 2013).
Indikation hinterfragen
In manchen Situationen ist es unklar, ob eine Sonde sofort gelegt werden muss oder ob damit noch gewartet werden kann. Hierbei ist wichtig zu wissen, dass die stundenweise Unterbrechung einer enteralen Ernährung nicht mit erheblichen Nachteilen verbunden ist. In einer aktuellen Metaanalyse (Marik et al. 2015) konnte bezüglich der Infektionsrate, Beatmungsdauer, Verweildauer und Mortalität kein signifikanter Unterschied festgestellt werden. 2 500 Patienten sind bei dieser Studie entweder normokalorisch – das entspricht 75 bis 80 Prozent des tatsächlichen Bedarfs – oder hypokalorisch – 16 bis 59 Prozent des tatsächlichen Bedarfs – ernährt worden.
Eine kurzfristige Unterbrechung über Stunden ist also tolerabel, auch wenn eine Mangelernährung natürlich grundsätzlich vermieden werden sollte. Diese Information ist auch vor dem Hintergrund, dass die Anlage einer Ernährungssonde im Nachtdienst eher zu Komplikationen führen kann (Taylor 2013), wichtig. Die Verzögerung der Gabe von Medikamenten, die über eine Ernährungssonde appliziert werden, muss hingegen im Einzelfall entschieden werden.
Bestehende Schluckstörungen, im Fachjargon Dysphagie genannt, sind ein Aspekt, der bei der Frage, ob eine Ernährungssonde behalten oder wiederholt angelegt werden soll, bedacht werden muss. Hier konkurrieren der Wunsch, die Bedürfnisse der Patienten zu erfüllen und ihnen eine orale Nahrungszufuhr zu ermöglichen, und gegensätzliche Sicherheitsbedenken. Bis zu 83 Prozent der frisch extubierten Patienten weisen Schluckstörungen auf (Macht et al. 2011). Sie sind mit einer erhöhten Pneumonierate, Reintubationen und Mortalität assoziiert, sodass Patienten vor dem Entfernen einer Ernährungssonde auf Schluckstörungen untersucht werden sollten, bevor sie sicher oral belastet werden können.
Risiken beachten
Die Anlage einer Ernährungssonde ist für Intensivpflegende häufig eine Routinetätigkeit. Ernährungssonden sind schnell gelegt, allerdings ist vor allem bei unzureichendem Personalschlüssel für ein ausführliches Risikoassessment keine Zeit. Durchschnittlich tritt bei jeder zehnten Anlage eine Komplikation auf (Stayner et al. 2012). In der Übersichtsarbeit von Prabhakaran et al. (2012) werden folgende unerwünschte Ereignisse angegeben, die bei der Anlage einer Ernährungssonde auftreten können:
- Übelkeit,
- Nasenbluten (1,8–4,7 %),
- Laryngospasmus (5 % bei bronchialer ES-Anlage),
- Insertion in den Thorax (1,3–8 %), dann eher der rechte Bronchus mit folgender Pneumonie, Atelektase, Abszess, bronchiale Perforation, pleurale Penetration,
- Pneumothorax (60 % der iatrogenen Pneumothoraxe durch ES-Anlage),
- Magenulcera (selten),
- Ösophagusperforation (extrem selten),
- intrakraniale Insertion (extrem selten).
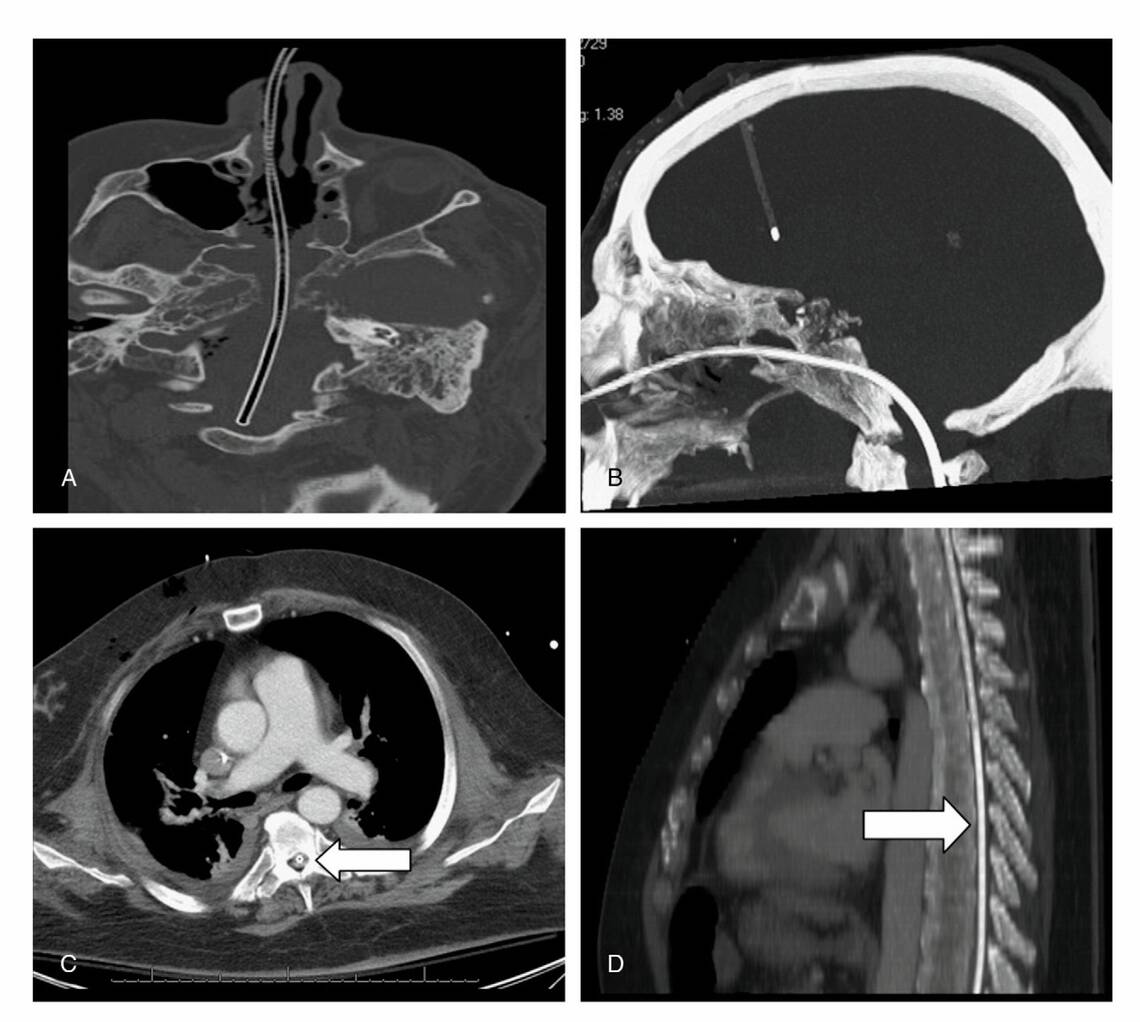
Die Folgen einer intrathorakalen Anlage sind entsprechend pulmonale Blutungen, pleurale Penetration, Pneumothorax mit Empyem und Sepsis. Ein erhöhtes Risiko für Fehlanalgen treten bei Patienten mit endotrachealem Tubus, Bewusstseinsstörung, verminderten Schutzreflexen und bei wiederholten Fehlanlagen auf, vor allem im Nachtdienst und bei geringer Erfahrung der Anwender (Braun et al. 2011). Ösophagusperforationen und craniale Insertionen (Abb. 1) sind selten bis extrem selten (Freij et al. 1997, Hanna et al. 2012).
Lage kontrollieren
Um solche unerwünschten Ereignisse zu vermeiden, kommt der Überprüfung der korrekten Anlage eine besondere Bedeutung zu. In der Praxis werden folgende Verfahren zur Lagekontrolle verwendet:- Ausschluss von Fehllage durch Husten, Abfall der pulsoxymetrisch gemessenen Sauerstoffsättigung (sPO2) während der Anlage,
- Inspektion der Mundhöhle,
- Auskultation mit Stethoskop und 30 bis 50 Milliliter Luftinsertion,
- Beurteilung des Aspirats,
- pH-Wert-Kontrolle des Aspirats,
- Sonografie oder Fluoroskopie,
- Röntgenkontrolle und Beurteilung der Aufnahme,
- Kapnometrie (CO2-Messung),
- Sonstiges (elektromagnetische Kontrolle, Cuff-Manometer).
pH-Wert-Kontrolle ist am sichersten
Als sicherstes Verfahren gilt also die pH-Wert-Kontrolle. Bei unsicheren Ergebnissen sollte zusätzlich eine Röntgenaufnahme gemacht werden (NIH 2009, ENA 2010, Taylor 2013). Taylor (2013) empfiehlt:- Bei wachen, spontan atmenden Patienten ohne vorherige Fehlanlagen einer Ernährungssonde sollte eine pH-Wert-Messung nach Anlage erfolgen. Ein pH von 5 oder weniger erfasst eine gastrale Anlage in 77 bis 90 Prozent der Fälle. Liegt der pH-Wert über 5, kann dies auf eine pulmonale, ösophageale oder intestinale Anlage hinweisen. Bei Zweifel sollte ein elektromagnetisches Verfahren oder eine Röntgenaufnahme durchgeführt werden.
- Bei beatmeten, bewusstseinsgetrübten Patienten oder bei wiederholten Fehlanlagen sollte entweder a) eine Kapnometrie während der Anlage und eine pH-Wert-Kontrolle oder b) ein elektromagnetisches Verfahren durchgeführt werden. Der pH-Wert sollte bei 5 oder darunter liegen. Bei Zweifel sollte ein elektromagnetisches Verfahren oder eine Röntgenaufnahme durchgeführt werden.
Bourgault AM, Heath J, Hooper V, Sole ML, Nesmith EG. Methods used by critical care nurses to verify feeding tube placement in clinical practice. Crit Care Nurse. 2015 Feb; 35(1): e1–7
Boeykens K, Steeman E, Duysburgh I. Reliability of pH measurement and the auscultatory method to confirm the position of a nasogastric tube. Int J Nurs Stud. 2014 Nov; 51 (11): 1427–33
Braun J, Bein T, Wiese CHR, Graf BM, Zausig YA. Ernährungssonden bei kritisch kranken Patienten. Anästhesist 2011, 60: 352–365
Burns SM, Carpenter R, Blevins C, Bragg S, Marshall M, Browne L, Perkins M, Bagby R, Blackstone K, Truwit JD. Detection of inadvertent airway intubation during gastric tube insertion: Capnography versus a colorimetric carbon dioxide detector. Am J Crit Care. 2006 Mar; 15 (2): 188–95
Chau JP, Lo SH, Thompson DR, Fernandez R, Griffiths R. Use of end-tidal carbon dioxide detection to determine correct placement of nasogastric tube: a meta-analysis. Int J Nurs Stud. 2011 Apr; 48 (4): 513–21
Emergency Nurses Association (2010). Gastric Tube Placement Verification. www.ena.org/practice-research/research/CPG/Documents/GastricTubeCPG.pdf, letzter Abruf: 12.12.2015
Freij RM, Mullett STH (1997). Inadvertent intracranial insertion of a nasogastric tube in a non-trauma patient. J Accid Emerg Med. 45–47.
Gerritsen A, van der Poel MJ, de Rooij T, Molenaar IQ, Bergman JJ, Busch OR, Mathus-Vliegen EM, Besselink MG. Systematic review on bedside electromagnetic-guided, endoscopic, and fluoroscopic placement of nasoenteral feeding tubes. Gastrointest Endosc. 2015 Apr;81(4): 836–47
Hanna AS, Grindle CR, Patel AA, Rosen MR, Evans JJ (2012). Inadvertent insertion of nasogastric tube into the brain stem and spinal cord after endoscopic skull base surgery. American Journal of Otolaryngology – Head and Neck Medicine and Surgery 33 (1): 178–180
Macht M, Wimbish T, Clark BJ, Benson AB, Burnham EL, Williams A, Moss M. Postextubation dysphagia is persistent and associated with poor outcomes in survivors of critical illness. Crit Care. 2011; 15 (5): R231
Marik PE, Hooper MH. Normocaloric versus hypocaloric feeding on the outcomes of ICU patients: a systematic review and meta-analysis. Intensive Care Med. 2015 Nov 10
Metheny N, Reed L, Berglund B, Wehrle MA. Visual characteristics of aspirates from feeding tubes as a method for predicting tube location. Nurs Res. 1994 Sep-Oct; 43 (5): 282–7
Metheny NA, Stewart BJ, Mills AC. Blind insertion of feeding tubes in intensive care units: a national survey. Am J Crit Care. 2012 Sep; 21(5): 352–60
National Health Service (2011). Reducing the harm caused by misplaced nasogastric feeding tubes in adults, children and infants. www.nrls.npsa.nhs.uk/resources/?EntryId45=129640, letzter Abruf: 12.12.2015
Neumann MJ, Meyer CT, Dutton JL, Smith R. Hold that x-ray: aspirate pH and auscultation prove enteral tube placement. J Clin Gastroenterol. 1995 Jun; 20(4): 293–5
Panknin HD (2011). Komplikationen im Umgang mit Ernährungssonden. intensiv; 19: 204–207
Prabhakaran S, Doraiswamy VA, Nagaraja V, Cipolla J, Ofurum U, Evans DC, Lindsey DE, Seamon MJ, Kavuturu S, Gerlach AT, Jaik NP, Eiferman DS, Papadimos TJ, Adolph MD, Cook CH, Stawicki SP. Nasoenteric tube complications. Scand J Surg. 2012; 101(3): 147–55.
Seguin P, Le Bouquin V, Aguillon D, Maurice A, Laviolle B, Mallédant Y. Testing nasogastric tube placement: evaluation of three different methods in intensive care unit. Ann Fr Anesth Reanim. 2005 Jun;24(6): 594–9
Smyrnios NA, Lenard R, Rajan S, Newman MS, Baker SP, Thakkar N, Wassef W, Ajmere NK, Irwin RS. Comparison of a self-inflating bulb syringe and a colorimetric CO2 indicator with capnography and radiography to detect the misdirection of naso/orogastric tubes into the airway of critically ill adult patients. Chest. 2015 Jun147(6): 1523–9
Sparks DA, Chase DM, Coughlin LM, Perry E. Pulmonary complications of 9931 narrow-bore nasoenteric tubes during blind placement: a critical review. J Parenter Enteral Nut 2011;35: 625–9
Stayner JL, Bhatnagaer A, McGinn AN, Fang JC. Feeding tube placement: errors and complications. Nutr Clin Prac 27 (6): 738–748
Taylor SJ. Confirming nasogastric feeding tube position versus the need to feed. Intensive and Critical Care Nursing (2013) 29, 59–69
Welch S, Hanlon M, Waits M, Foulks C. Comparison of four bedside indicators used to predict duodenal feeding tube placement with radiography. J Parenter Enteral Nutr 1994; 18: 525–30