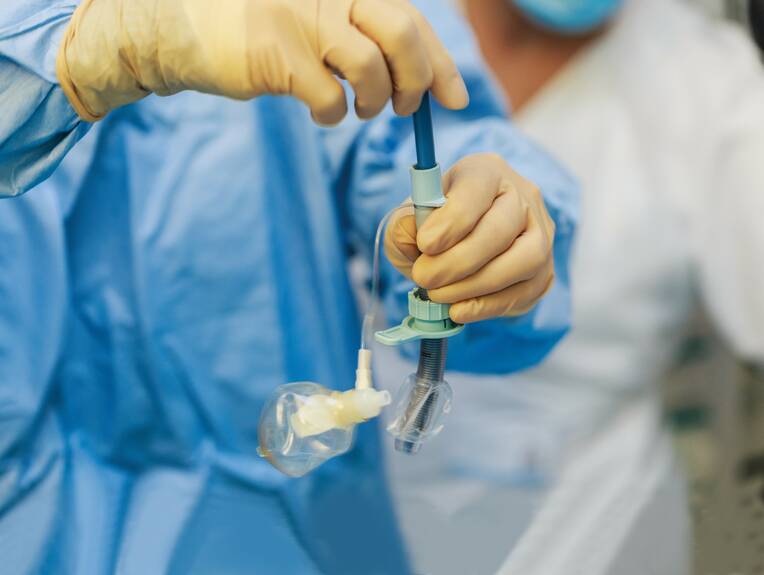
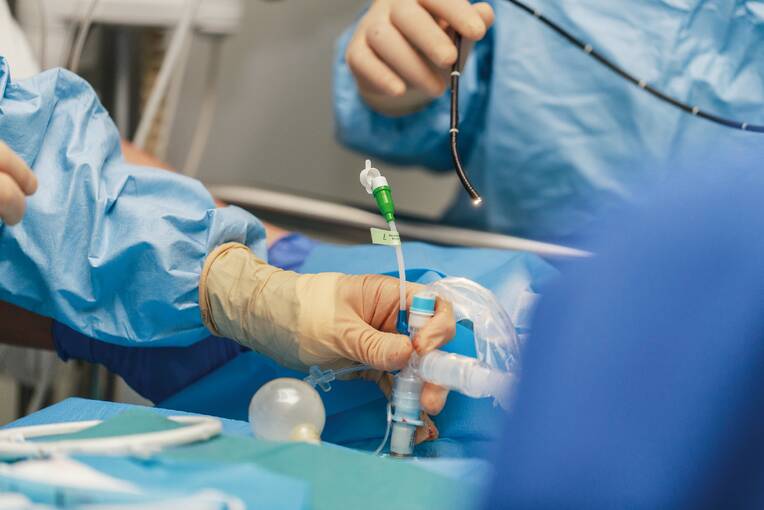
Die perkutane Tracheotomie ist eine mittlerweile weltweit anerkannte Alternative zur chirurgischen Eröffnung der Trachea. Bei den Eingriffen, die bettseitig durchgeführt werden können, kann es jedoch zu schwerwiegenden Komplikationen kommen. Eine sorgfältige Vorbereitung und eine gewissenhafte Durchführung sind daher Grundvoraussetzungen für eine optimale Patientensicherheit.
Die Geschichte der Tracheotomie reicht bis in die Antike zurück. Erste Hinweise finden sich bereits auf zwei ägyptischen Tafeln (1). Ein konkurrierendes Verfahren zur Sicherung der oberen Atemwege ist die Intubation. Auch sie ist seit der Antike bekannt.
Um 1627 entstand mit einer Veröffentlichung des italienischen Mediziners Sanctorius Sanctorius ein Verfahren, das die Wurzel der perkutanen dilatativen Methode darstellt. Zum ersten Mal wurde hier über eine Aufdehnung der Wunde mit dem Einsetzen einer Kanüle berichtet. Sanctorius Sanctorius war der erste, der einen Trokar – eine Hohlnadel mit einem dolchartigen Innenkörper mit dreikantiger Spitze – für die Tracheotomie verwendet hatte (2). Dieser chirurgische Eingriff wurde während der Diphtherie-Epidemien gegen Ende des 19. Jahrhunderts an Tausenden von Kindern praktiziert, die an dieser Krankheit zu ersticken drohten.
Transport in OP-Saal nicht erforderlich
Mit der Entwicklung der Intensivmedizin in den 1960er-Jahren gewann die elektive Tracheotomie langzeitbeatmeter Patienten auf der Intensivstation zunehmend an Bedeutung (3, 4). Die Sicherung der Atemwege und die Vermeidung einer Aspiration sind Ziele der Langzeitbeatmung und der Tracheotomie gleichermaßen (16).
Besonders in den vergangenen 20 Jahren ist es zu einer raschen Entwicklung und Verbreitung vielfältiger dilatativen Methoden gekommen. Hier sind insbesondere die Beschreibungen von Ciaglia, Griggs, Fantoni und Frova maßgeblich.
Die aktuell verfügbaren perkutanen dilatativen Verfahren stehen prinzipiell gleichberechtigt nebeneinander und sind als kommerzielle Sets auf der Intensivstation verfügbar.
Die perkutane Tracheotomie ist mittlerweile im intensivmedizinischen Bereich eine weltweit anerkannte Alternative zur chirurgischen Tracheotomie. Sie ist eine einfache Technik, die bettseitig durchgeführt werden kann (5). Ein Transport in den Operationssaal ist nicht erforderlich.
Dies stellt einen deutlichen Vorteil dar, weil ein Transport kreislaufinstabiler Patienten mit einem erhöhten Risiko einhergeht. Komplikationen wie versehentliche Extubation und Dislokation von invasiven Zugängen und Drainagen fallen somit weg.
Schwierige Beatmungsformen können zudem mit der bettseitigen Tracheotomie am Patientenbettplatz fortgeführt werden. Der Personal-, Material- und Zeitaufwand ist gering. Bei einer Tracheotomie sollte inklusive der Vor- und Nachbereitung mit etwa 60 Minuten gerechnet werden.
Atemwege sichern
Bei einem respiratorischen Notfall bleibt die endotracheale Intubation zunächst die erste Maßnahme. Die Entscheidung zur Tracheotomie erfolgt in der Intensivmedizin erst sekundär, also nach Abwägung der Vor- und Nachteile (9).
Insofern stellen Tracheotomien elektive Eingriffe bei erwarteter Langzeitbeatmung und langfristig fehlender Schutzreflexe dar. Sie dienen der Sicherung der oberen Atemwege und der Durchführung einer differenzierten Beatmungstherapie. Orale, laryngeale und tracheale Komplikationen der Langzeitintubation und des verlängerten Weanings werden vermieden.
Bei längerer Liegedauer des endotrachealen Tubus kommt es durch die mechanische Belastung an Stimmlippe und Knorpel dort zu Ulzerationen bis hin zu Nekrosen und Stimmbandschäden. Trachealstenosen und Tracheomalazie können als Komplikationen entstehen.
Bei der Tracheomalazie kommt es durch entzündliche Veränderungen der Trachealwand mit Perichondritis zu einer Erweichung bis hin zur vollständigen Destruktion der Knorpelspangen. Ein Kollaps der Trachealstruktur während des Einatmens und des Hustens sind die Folgen. Trachealkanülen dagegen sitzen unterhalb des Kehlkopfes, schonen daher dieses Gebiet und Intubationsschäden werden vermieden.
Als weitere Komplikationen der Langzeitintubation gelten eine erschwerte Bronchialtoilette und die Entwicklung einer Sinusitis maxillaris, die nach einer Tracheotomie so nicht mehr auftreten.
Weitere wichtige Gründe für das Anlegen eines Tracheostomas sind die bessere Entwöhnbarkeit vom Respirator, die bessere Toleranz des Atemzugangs und die Vermeidung von Aspiration, die sich bei neurologischen Erkrankungen mit morphologischen Veränderungen des Schluckakts und bei beidseitiger Rekurrensparese ergeben kann.
Ein Endotrachealtubus bietet aufgrund seiner Länge einen erhöhten Atemwegswiderstand gegenüber einer Trachealkanüle. Nach dem operativen Eingriff reduzieren sich der Widerstand und die Atemarbeit durch im Innendurchmesser größere und kürzere Trachealkanülen (6). Die anatomische Totraumreduktion bei einem Tracheostoma hat eine verbesserte alveoläre Ventilation zur Folge.
Kontraindikationen beachten
Es wird zwischen absoluten und relativen Kontraindikationen der perkutanen Dilatationstracheotomie (PDT) unterschieden (8). Absolute Kontraindikationen sind:
- Notfälle jeglicher Ursache,
- schwierige Anatomie bei Adipositas permagna, Tracheomalazie und extremen Kurzhals,
- nicht korrigierbare Gerinnungsstörungen,
- instabile HWS-Fraktur, frische Trachealnaht- und OP-Wunden am Hals,
- laryngoskopisch nicht intubierbarer Patient,
- ARDS beziehungsweise schwerste Gasaustauschstörung,
- Alter unter 16 bis 18 Jahren, weil aufgrund des geringen Trachealquerschnitts und der hohen Elastizität der Trachea eine hohe Gefahr der Verletzung der Trachealhinterwand besteht.
Vor jeder Punktionstracheotomie muss geprüft werden, ob sich die Glottis mithilfe der direkten Laryngoskopie ausreichend visualisieren lässt, um sicherzustellen, dass der Patient im Fall eines Atemwegverlusts jederzeit konventionell reintubiert werden kann.
Von besonderer Bedeutung für Komplikationen sind Arrosionsblutungen großer Gefäße in der Nähe zur Trachea und der Schilddrüse. Vor Beginn der Tracheotomie ist eine sonografische Darstellung dieses Bereichs durch den Operateur hilfreich, um eventuelle Anomalien zu erkennen. Um eine PDT sicher durchführen zu können, muss der Ringknorpel und der Trachealverlauf sicher zu tasten und zu identifizieren sein.
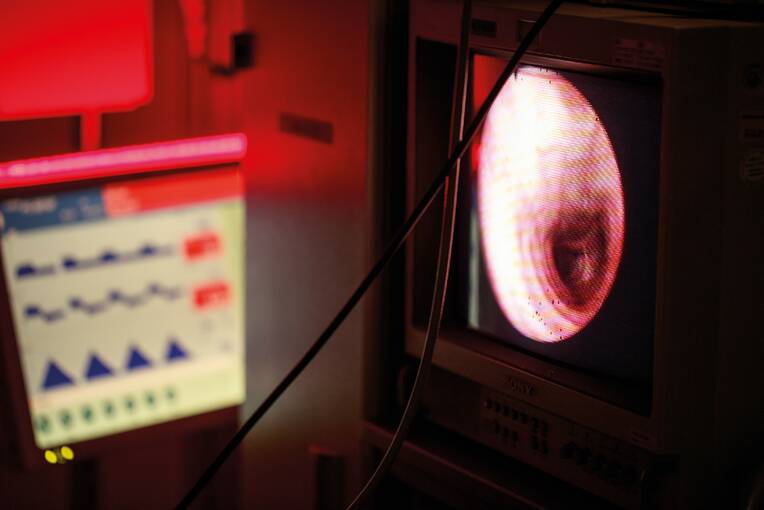
Unabhängig vom Verfahren der Tracheotomie sollte stets eine videoskopische Kontrolle mittels Bronchoskop erfolgen. Damit belaufen sich die Risiken einer paratrachealen Fehlpunktion und die Verletzung der Trachealhinterwand gegen null.
Tracheotomie erleichtert Pflege
Bettseitige Tracheotomie bietet gegenüber der Intubation deutliche Vorteile für pflegerische Tätigkeiten. Trachealkanülen können beispielsweise sicherer fixiert werden. Hierfür eignen sich gepolsterte Kanülentragebänder mit Schaumstoff und hautfreundlichem Material im Nackenbereich für einen idealen Dekubitusschutz und vorzugsweise mit Kletthalterung. Eine Hakenhalterung am Halteband löst sich häufig vom Kanülenschild und erhöht die Gefahr einer Dislokation. Dieser Gesichtspunkt ist insbesondere für die Frühmobilisation und der Mobilität der Patienten im Allgemeinen wichtig, die mit tracheotomierten Patienten erleichtert durchgeführt werden kann.
Nach der Tracheotomie ist ein geringerer Bedarf an Analgetika und Sedativa erforderlich. Eine zunehmende Mimik der Lippen und des Gesichts ist erkennbar. Die Kommunikation gelingt besser, teilweise bis hin zur Sprechmöglichkeit mit dem Patienten.
Weitere pflegerische Vorteile ist die leichter handhabbare Durchführung von Bronchialtoilette und Mundpflege. Die orale Ernährungsaufnahme mit Schlucken bei geblockter oder ungeblockter Kanüle ist nun möglich.
Komplikationen, die sich aufgrund einer Dysphagie ergeben, sollten nicht unterschätzt werden. Tracheotomien führen unabhängig von der Grunderkrankung sehr häufig zu potenziellen lebensbedrohlichen Schluckstörungen mit Aspiration und Pneumonien. Vor einer Oralisierung sollte bei allen, vor allem älteren invasiv langzeitbeatmeten Patienten die Schluckfähigkeit überprüft werden (7).
Früh oder spät tracheotomieren?
Zum optimalen Zeitpunkt einer Tracheotomie gibt es keine eindeutigen wissenschaftlichen Erkenntnisse. Zahlreiche Studien kommen zu dem Schluss, dass so früh wie möglich tracheotomiert werden sollte. Früh heißt hier manchmal schon nach zwei Tagen, manchmal nach sieben Tagen. Nach diesen sieben Tagen gibt es keine genaue Abgrenzung mehr zwischen früher und später Tracheotomie.
Entscheidend ist, die richtigen Patienten auszuwählen – also diejenigen, die mit großer Wahrscheinlichkeit länger – mehr als 21 Tage – intubiert bleiben. Zu dieser Gruppe von Patienten gehören etwa polytraumatisierte Patienten mit Schädel-Hirn-Trauma.
Die Indikationsstellung und das Timing der Tracheotomie hängen weiterhin von der subjektiven Einschätzung und der klinischen Erfahrung des Intensivmediziners ab. Die frühe Tracheotomie kann allerdings zu einer kürzeren Beatmungs- und Intensivbehandlungsdauer führen. Zudem wurden niedrigere Mortalitätsraten beschrieben (11, 12, 13, 14).
Alle Methoden sind sicher
Es stehen mehrere Methoden zur Tracheotomie zu Verfügung. Die verschiedenen perkutanen Verfahren unterscheiden sich in den Methoden der Schaffung eines Zugangs zur Trachea.
- Bei der Punktionstracheotomie nach Ciagla erfolgt die Aufdehnung des Punktionskanals mit abgestuften Dilatatoren.
- Bei der Dilatationstracheotomie nach Griggs erfolgt das Aufspreizen des prätrachealen Gewebes mit einer modifizierten Howard-Kelly-Zange.
- Bei der translaryngealen Tracheotomie nach Fantoni erfolgt die Aufdehnung der Trachea und des prätrachealen Gewebes durch einen retrograden Durchzug der Trachealkanüle. Dies ist das einzige Verfahren zur Anwendung bei Kindern und Jugendlichen.
- Bei der Punktionstracheotomie „Blue Rhino“ nach Ciaglia erfolgt die Aufdehnung des Punktionskanals mit einem Dilatator.
- Bei der Punktionstracheotomie nach Frova erfolgt die Aufdehnung des Punktionskanals mit einer Dilatationsschraube.
- Bei der Punktionstracheotomie „Blue Dolphin“ nach Ciaglia erfolgt die Aufdehnung des Punktionskanals durch einen widerstandsfähigen Ballon mit einem Druck von 11 Atmosphären (atm). Erklärung: Der widerstandsfähige Ballon wird mittels Kontrolle eines Manometers bis 11 atm für etwa 30 bis 40 Sekunden aufgedehnt. Somit entsteht ein zirkuläres sauberes Tracheostoma. Die physikalische Atmosphäre ist eine Einheit des Drucks. 1 atm entspricht 1013 Hektopascal (hPa).
Allen Verfahren gemeinsam ist die Punktion der Trachea. Der Punktionsort befindet sich zwischen dem zweiten und dritten Trachealknorpel. Es wird so in der Regel eine Punktion des translaryngealen Tubus oder seines Cuffs verhindert. Eine Verletzung des Ringknorpels bei der Dilatation wird vermieden. Drucknekrosen wurden nicht beobachtet.
Alle Techniken zur Punktionstracheotomie sind gleichermaßen sicher. Die schweren Komplikationsraten werden mit weniger als einem Prozent beziffert (14). Erwähnenswert sind weiter sehr niedrige Infektionsraten und ein durchgängig geringes Blutungsrisiko. Eine Rückoperation ist nicht notwendig und bessere kosmetische Ergebnisse gegenüber einer chirurgischen Tracheotomie sind zu erreichen.
Zu einer gut geplanten und sicher ablaufenden Tracheotomie ist eine enge Absprache zwischen dem durchführenden Arzt und der verantwortlichen Pflegefachkraft selbstverständlich. Die Lagerung des Patienten erfolgt in Rückenlage ohne Kopfkissen. Ein Polster aus einem Bezug oder Laken wird quer unter beiden Schulterblättern positioniert, damit der Kopf – wie bei einer Strumektomie – etwas überstreckt werden kann und die Trachea besser zu ertasten ist. Zur Fixierung des Kopfs wird dieser in einem festen Kopfring gelagert.
Bei Schädel-Hirn-Trauma mit erhöhtem intrakraniellen Druck ist Vorsicht geboten. Diese Patienten werden in Oberkörperhochlagerung und ohne Kopfreklination tracheotomiert. Der Eingriff wird mit dem ICP-Monitoring ununterbrochen überwacht. Unter dem Oberkörper und Kopf des Patienten sollte eine große Unterlage zum Schutz des Betts liegen. Eine sechsstündige präoperative Nahrungskarenz ist einzuhalten und der restliche Mageninhalt ist kurz vor dem Eingriff nochmals abzusaugen, damit das Aspirationsrisiko weiter vermindert wird.
Die Antikoagulation ist in Absprache mit dem Arzt rechtzeitig zu pausieren. Eine sorgfältige Mundpflege mit antiseptischen Substanzen wie Chlorhexidin und Polyhexanid mit nachgewiesener Wirksamkeit wird empfohlen. Der Cuffdruck und die korrekte Lage des Endotrachealtubus sind zu überprüfen. Die Pflegefachkraft assistiert beim sterilen Anreichen der Materialien und trägt dabei Mundschutz und Untersuchungshandschuhe. Eine Verdunkelung des Patientenzimmers ist zu organisieren, damit das Licht des Bronchoskops durch die Haut des OP-Gebiets gut erkennbar ist.
Während des Eingriffs beobachtet die Pflegefachkraft sämtliche Vitalzeichen, die Beatmungsparameter und die einzelnen Schritte der verschiedenen Verfahren. Komplikationen wie größere Blutungen, Verletzung der Trachealhinterwand, technische Defekte oder ein drohender Verfahrenswechsel sollen so rechtzeitig erkannt werden. Ein Tracheotomie-Set für ein zweites Verfahren sollte immer bereitliegen.
Nach der Tracheotomie
Nach der operativen Intervention sind zahlreiche pflegerische Aspekte zu beachten. Unmittelbar nach dem Eingriff wird der Patient für einige Stunden in der Oberkörperhochlagerung positioniert.
Die Blutgasanalyse zeigt die respiratorische Situation nach dem Eingriff und dient, wenn notwendig, der Korrektur von Beatmungsparameter. Ein Thorax-Röntgen schließt sich an. Die Sedierung wird reduziert, damit der Patient in die Spontanatmung mit Aufwachversuch wechseln kann.
In den ersten 24 Stunden erfolgt ein Verbandwechsel am Tracheostoma nur bei Bedarf. Es genügen anfangs sterile Schlitzkompressen. Die Sichtung des frischen Tracheostoma bezieht sich auf zwei wichtige Aspekte. Zum einen auf ein Auftreten eines Hautemphysems, das auf eine Kanülenfehllage hinweist, zum anderen auf ein Nachbluten am Tracheostoma, als häufigste Komplikation. Sickerblutungen als Erosion von Kapillargefäßen werden oft erst spät bemerkt. Es handelt sich um innere Blutungen. Epinephrin getränkte Kompressen oder ein Hämostyptikum stillen kleinere Blutungen. Mitunter ist eine Umstechung des Tracheostoma bei kleinen arteriellen Blutungen erforderlich. Massive arterielle Blutungen sind zu erkennen an trachealen Brodelgeräuschen, die Aspiration ist blutig. Es handelt sich um einen Notfall; der Patient muss sofort reoperiert werden.
Im weiteren Verlauf reichen tägliche Verbandwechsel mit Schaumverbänden, die aufgrund des Polstereffekts die Wundränder vor der Kanüle schützen. Die Verbände sind nichtklebend, können große Menge an Sekret aufnehmen und sind eine sichere Keimbarriere für MRSA. Metalline Schlitzkompressen sollten wegen ihrer Aluminiumbeschichtung und dem krebserregenden Verdacht nicht mehr eingesetzt werden. Zudem besitzen sie eine sehr geringe Saugkraft, die bei vermehrtem Sekretstau zu einer Infektionsgefahr am Tracheostoma führen kann.
Bei der Durchführung einer speziellen Lagerungstherapie, wie der kompletten Bauchlage um 180 Grad und der inkompletten Bauchlage um 135 Grad ist auf die sichere Fixierung und Freilagerung der Trachealkanüle zu achten. Bei Druck auf die Kanüle kann es zu Verletzungen des Kehlkopfs kommen. Ein Zug an der Kanüle durch das Beatmungssystem ist zu vermeiden. Die Spitze der Trachealkanüle kann dabei an der Trachealwand anliegen und zu Schleimhautschädigungen führen.
Aspekte der Tracheostomapflege
Zur Grundpflege des Patienten gehört von nun an auch die tägliche Tracheostomapflege. Nach der Inspektion wird die Stomaumgebung mit einer Kompresse, die in einer 0,9-prozentigen Kochsalzlösung getränkt wurde, gereinigt und anschließend getrocknet. Eine Wunddesinfektion erfolgt mit einem schleimhautgeeigneten Desinfektionsmittel – zum Beispiel Octenisept – mithilfe steriler Kompressen. Die parastomale Haut ist trocken zu halten. Aufgrund der Entstehung feuchter Kammern finden Salben keine Anwendung. Bei unruhigen Patienten ist die Gefahr einer Dekanülierung gegeben, weswegen zwei Pflegende den Verbandwechsel durchführen sollten.
Am Patientenbettplatz müssen für den Notfall Trachealspreizer und Ersatzkanülen verschiedener Größen unmittelbar griffbereit sein.
Der erste Kanülenwechsel sollte nicht vor dem zehnten postoperativen Tag nach der Tracheotomie durchgeführt werden. Erst ab dem siebten bis zehnten postoperativen Tag ist ein ausreichend bindegewebiges, organisiertes Tracheostoma vorhanden. Bei einem „frischen“ Tracheostoma kommt es zu einem sofortigen Verschieben der prätrachealen Schichten, was auch als Kulissenphänomen bezeichnet wird.
Mangelhafte Fixierung, Manipulation durch den Patienten oder Umlagerungen im Rahmen der Pflege können dazu führen, dass die Kanüle disloziert. Bei einer perkutanen Dilatationstracheotomie kann der Wiedereinsatz schwierig sein. Im Fall einer eingeschränkten Spontanatmung kann es dann schnell zu einer Hypoxie kommen.
Kanülendislokationen bei beatmeten Patienten können zu einem Emphysem und möglicherweise zu einem Spannungspneumothorax führen. Der Patient muss zunächst oral intubiert werden. Das Tracheostoma ist dabei luftdicht zu verschließen. Anschließend erfolgt eine Rekanülierung unter fiberoptischer Kontrolle.
Tracheotomierten Patienten fehlt die transnasale Atmung. Das bedeutet, dass die physiologische Atemlufterwärmung, -befeuchtung und -reinigung fehlt. Infolgedessen ist der Einsatz eines HME-Filters unentbehrlich. Wenn die Patienten pulmonal stabil sind und keine fehlenden Schutzreflexe wie Husten und Schluckreflex haben, ist der Einsatz einer Künstlichen Nase geeignet. Sie dienen der Befeuchtung, Anwärmung und Filterung der Atemluft bei tracheotomierten Patienten. Ein Atemzugvolumen ist bis 1 200 Milliliter, je nach Modell, möglich.
Gleichzeitig ist ein Wechsel zu einem Sprechventil möglich. Das Ventil sollte einen annähernd physiologischen Positiv endexpiratorischen Druck (PEEP) durch den Stimmritzenschluss erzeugen. Der Patient kann dann wieder phonieren und verbal kommunizieren. Die Expiration erfolgt via naturalis.
Bei weiter erfolgreichen Weaning kann für wenige Tage der Einsatz eines Platzhalters sinnvoll sein, der nur der vorderen Trachealwand anliegt. Zur Ein- und Ausatmung werden wieder die oberen Atemwege genutzt. Die tracheobronchiale Absaugung bleibt erhalten und die Belastbarkeit der Atmung vor der Dekanülierung wird erprobt. Eine nicht-invasive Beatmungstherapie (NIV) wird ab diesem Stadium mittels Masken für die Nase-Mund-Partie oder Vollgesichtsmasken durchgeführt.
Hat der Patient über einen längeren Zeitraum eine normale Atemfrequenz, keine Erschöpfungszeichen und eine ausreichende Muskelkraft – Augen öffnen, Kopf heben, Hand drücken – bei vorhandenen Schutzreflexen, steht der Dekanülierung nichts mehr im Wege. Der Hustenstoß sollte kräftig sein, damit es zu keinem Sekretverhalt kommt. Das Tracheostoma wird mit sterilem Verband luftdicht abgedeckt und nach einigen Tagen ist es spontan verschlossen. Nur eine kaum sichtbare und reizlose Narbe bleibt bestehen.
(1) Pahor, L., Ear, Nose and Throat in Ancient Egypt. The Journal of Laryngology and Otology 1992; 106: 773–779
(2) Haller, A.v., Bibliotheca Chirurgica, Bd.1, Basileae 1775, Nachdruck von 1971, Hildesheim: Olms, S. 313
(3) Durst, J., Rohen, J. W. (1991): Chirurgische Operationslehre
(4) Walz, M. K. (2002): Die Tracheostomie. Indikationen, Methoden, Risiken. Der Anaesthesist 51, 123
(5) Sosat, J. (2007): Die geschichtliche Entwicklung der Perkutanen Dilatativen Tracheotomieverfahren im historischen Kontext. ub-ed.ub.uni-greifswald.de/opus/volltexte/2007/404/pdf/Diss_Sosath_Jan.pdf, Abruf: 28.8.2016
(6) Davis K Jr, Branson RD, Porembka D. Respir Care 1994; 39 (6): 611–616
(7) Heidler et al. (2014): Oralisierung langzeitbeatmeter Patienten mit Trachealkanüle. Unterschätzte Gefahr von Dysphagien, Med Klein Intensivmed Notfmed, Springer
(8) Burchardi, H. (2011): Die Intensivmedizin, 11. Auflage, Springer
(9) Bause, H., Prause, A. (1999): Stellenwert und Komplikationen der minimalinvasiven perkutanen Tracheotomieverfahren, Anästhesiol. Intensivmed. Notfallmed. Schmerzther., 34: 659–664
(10) Bause, H., Prause, A. (1999): Alternative Atemwege, Anästhesiol. Intensivmed. Notfallmed. Schmerzther., 33: 501–504
(11) Andriolo, B., Early versus late tracheostomy for critically ill patients, 2015
(12) Meng, L. et al., Early vs late tracheostomy in critically ill patients: a systematic review and meta-analysis, The clinical Respiratory Journal, 2015
(13) Hosokawa, K. et al., Timing of tracheotomy in ICU patients: a systematic review of randomized controlled trials, Critical Care 2015; 19: 424
(14) Huang H, Li Y, Ariani F, Chen X, Lin J., Timing of Tracheostomy in Critically Ill Patients: A Meta-Analysis. PLoS ONE 2015; 9 (3): e92981
(15) Byhan, C. (2008): Intensivmedizin up2date 4: 273–286
(16) Hachenberg, T., Pfeiffer, B. (2000): Die geschichtliche Entwicklung der Intensivmedizin in Deutschland. Der Anaesthesist 49, 441