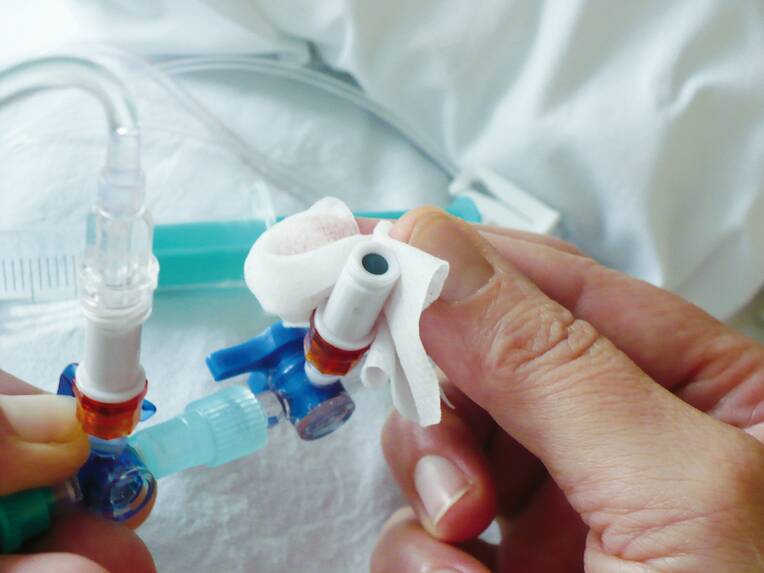
Venöse Zugänge werden traditionell mit Mandrins und Kombistopfen verschlossen. Diese Vorgehensweise ist aus hygienischer Sicht problematisch, weswegen besser sogenannte Membrankonnektoren verwendet werden sollten. Eine aktuelle Studie zeigt jedoch, dass die verschiedenen Konnektortypen unter hygienischen Gesichtspunkten genau geprüft werden sollten, bevor man sich für ein Produkt entscheidet.
Venenverweilkanülen und zentrale Venenkatheter gehören in Akutkrankenhäusern zu den am häufigsten verwendeten Medizinprodukten. Sie dienen der Infusion von Nährlösungen, der Applikation von Antibiotika und der Verabreichung akut erforderlicher Einzelinjektionen. Zwischen den einzelnen Anwendungen werden die Gefäßzugänge vielfach mit Kombistopfen oder Mandrins verschlossen. Erfahrungsgemäß kommt es dabei zum Rückfluss von Blut, weshalb bei diesen Manipulationen Einmalhandschuhe getragen werden müssen. Bei Venenverweilkanülen empfiehlt es sich zudem, eine saugfähige Kompresse unterzulegen.
Eine Alternative, mit der ein Blutrückfluss vermieden werden kann, bieten die sogenannten Membrankonnektoren, die im angloamerikanischen Sprachraum auch als „needleless connectors“, also als nadellose Konnektoren bezeichnet werden. Sie verschließen den Konus von Venenverweilkanülen oder Dreiwegehähne von Venenkathetern absolut rückflussdicht. Die Handhabung kann somit ohne Einmalhandschuhe erfolgen; es genügt die hygienische Händedesinfektion.
Die Membran der nadellosen Konnektoren muss vor dem Ansetzen einer Luer-Spritze durch kreisförmiges Abwischen mit einem alkoholgetränkten Tüchlein wischdesinfiziert werden. In einer aktuellen US-amerikanischen Leitlinie wird empfohlen, dass diese Desinfektion mindestens fünf Sekunden lang dauern sollte (1).
Acht Konnektoren im Test
Ob diese Einwirkzeit ausreicht und ob alle kommerziell erhältlichen Konnektortypen gleich gut desinfizierbar sind, wurde kürzlich in einer praxisnahen Studie überprüft (2). Mit der Untersuchung sollte die Frage geklärt werden, ob die Membrankonnektoren so gut wischdesinfiziert werden können, dass eine nachfolgend angeschlossene Infusion keine Keime mehr ins Blutgefäßsystem des Patienten „mitschleppt“. Untersucht wurden acht im Handel verfügbare Konnektormodelle verschiedener Hersteller (Abb. 1).
Für den Versuchsaufbau wurden die Konnektoren im Labor auf einer sterilen Fläche abgestellt. Die Membran jedes Konnektors wurde mit 1 000 Kolonien eines frisch angezüchteten Staphylococcus-aureus-Keims kontaminiert. In den folgenden sieben Tagen wurden klinische Benutzungen des Membrankonnektors simuliert. Hierzu wurden täglich „Blutabnahmen“ und Zuspritzungen von Kochsalzlösung durchgeführt oder es wurde eine Infusion angeschlossen. Anstelle von Patientenblut wurde für die simulierten Blutabnahmen Pferdeblut durch die Konnektoren aspiriert. Insgesamt wurde jeder Membrankonnektor pro Tag 15-mal betätigt. Über den gesamten siebentägigen Untersuchungszeitraum ergaben sich somit 105 Nutzungen.
Vor jedem Ansetzen einer Luer-Spritze oder einer Infusionsleitung wurden die Konnektoren mit einem Fertigwischtüchlein (Sani-ClothR) abgerieben, das 70-prozentigen Isopropyl-Alkohol enthielt. Das Tüchlein wurde hierzu über eine Dauer von fünf Sekunden dreimal kräftig halbkreisförmig auf der Membranfläche beziehungsweise dem Septum bewegt.
In einer zweiten Serie wurde diese Desinfektionsdauer auf 15 Sekunden ausgedehnt und die Tüchlein wurden 15-mal halbkreisförmig bewegt. Die Spritzen wurden erst angesetzt, wenn die Membran sichtbar abgetrocknet war, was etwa 30 Sekunden dauerte. Die Kontamination der Membranen mit den Versuchskeimen wurde täglich dreimal durchgeführt, um jeweils eine mehrmalige Verunreinigung durch Anfassen oder Kontakt mit kontaminierten Flächen im Rahmen eines hektischen Stationsalltags zu imitieren.
Nach jeder Kochsalzspülung des Konnektors wurde die am patientenseitigen Ende austretende Spüllösung in einem sterilen Gefäß aufgefangen und bei vier Grad Celsius aufbewahrt. Nach jeweils 24 Stunden wurde die angesammelte Lösung auf ihren Gehalt an Staphylococcus-aureus-Keimen untersucht. Als Kontrolle wurden Membrankonnektoren mitgeführt, die entweder nicht mit Staphylococcus-aureus-Keim kontaminiert waren (Negativkontrolle) oder solche, die kontaminiert, aber nicht desinfiziert worden waren (Positivkontrolle).
Unterschiedlich gut desinfizierbar
Die Kontrollen ergaben jeweils einwandfreie Ergebnisse: Die nicht kontaminierten Konnektoren blieben über die gesamte Versuchsdauer steril, während die Lösungen, die aus kontaminierten, aber nicht desinfizierten Konnektoren gesammelt wurden, im Median 218 bis über 1 000 Staphylococcus-aureus-Keime enthielten.
Bei der fünfsekündigen Desinfektion mit Wischtüchlein waren einzelne Konnektortypen bereits am ersten Tag im Innengehäuse kontaminiert. Die Staphylococcus-aureus-Keime sind hier also an den Pseudopatienten weitergegeben worden. Dagegen blieben der Bionector, der CareSite und der MaxPlus Clear über fünf Tage steril; der CareSite und der MaxPlus Clear sogar bis zu sechs beziehungsweise sieben Versuchstage.
Bei längerer Desinfektion über 15 Sekunden zeigte sich der größte Unterschied für den Max- Guard-Konnektor, der nunmehr über die gesamte siebentägige Versuchsdauer steril blieb. Der Bionector schnitt dagegen ab dem vierten Versuchstag deutlich schlechter ab.
Schlussfolgerung der Autoren: Im Handel erhältliche Konnektormodelle zeigten eine unterschiedlich gute Desinfizierbarkeit. Der MaxPlus Clear und der CareSite schnitten bei der von der aktuellen US-amerikanischen Leitlinie empfohlenen Desinfektionsdauer von fünf Sekunden am besten ab, gefolgt vom Bionector. Wurde die Desinfektionsdauer auf 15 Sekunden verlängert, wie in einer Leitlinie aus Großbritannien empfohlen (3), so war der Desinfektionseffekt bei den meisten Konnektormodellen noch nachhaltiger. Die Ursache für den gegenteiligen Effekt beim Bionector blieb ungeklärt.
Kommentar des Autors: Die Studie ist für praktische Anwender auf Normal- und Intensivstationen außerordentlich wichtig. Viele Kliniken verzichten heute auf die Verwendung von Mandrins, die früher regelhaft zum Verschließen von Verweilkanülen genutzt wurden. Sie sind hygienisch außerordentlich problematisch, weil bei ihrer Entfernung meist etwas Blut aus der Verweilkanüle zurückfließt, das durch den neuen Mandrin in der Kanüle fixiert wird. Dieser Blutpfropfen kann zum Ausgangspunkt von Biofilmbildungen und Infektionen werden. Nicht selten führt der Blutpfropfen später auch zu einer Obstruktion der Kanüle. Der Versuch, diese Obstruktion durch Einspritzen von Kochsalz wieder zu beseitigen, kann zu gefährlichen Embolie-Ereignissen führen.
Werden statt der Mandrins die sogenannten Kombistopfen verwendet, verstopfen die Verweilkanülen meist noch schneller. Auf den Dreiwegehähnen von Venenkathetern sind derartige Kombistopfen zwar vielerorts noch Standard. Der darunter liegende Dreiwegehahn kann jedoch schlecht bis überhaupt nicht desinfiziert werden, sodass er oft zur Quelle von Kontaminationen des gesamten Systems wird. Daraus kann sich sehr leicht eine Blutstrominfektion entwickeln.
Die nadellosen Konnektoren stellen eine sehr gute Alternative zum Verschließen von venösen Zugängen dar. Die vorliegende Studie zeigt allerdings, dass man die einzelnen Modelle unter hygienischen Gesichtspunkten genau prüfen sollte, bevor man sich für ein Modell entscheidet. In der Literatur wurde immer wieder über schwere Infektionsserien im Zusammenhang mit bestimmten Modellen berichtet, die möglicherweise mit der Effektivität einer Desinfektion der Membran oder des Septums zusammenhängen (4, 5). Zwei Modelle waren in der vorliegenden Studie bereits bei einer kurzen Wischdesinfektion von nur fünf Sekunden über die gesamte Studiendauer gut desinfizierbar und blieben steril. Andere Modelle ließen deutliche Probleme der Desinfizierbarkeit erkennen. Werden die Konnektoren auf den Infusionssystemen zentraler Venenkatheter verwendet, müssen sie beim Wechsel des Systems – meist nach 72 Stunden – mit verworfen werden.
Die Studie zeigte auch, dass eine Desinfektion der Konnektoren auf keinen Fall unterlassen werden darf. Eine Kontamination mit Hospitalismuserregern ist im realen Betrieb leicht möglich und kann, wie die Studie zeigt, nach mehreren Tagen zu einer massiven Keimbelastung führen.
Bei Einführung derartiger Konnektoren in die Praxis muss daher eine ausführliche Anwendereinweisung erfolgen. Diese sollte für neue Mitarbeiter regelmäßig wiederholt werden.
(1) Marschall J et al. Strategies to prevent central-line associated bloodstream infections in acute care hospitals: 2014 update. Infect Control Hosp Epidemiol 2014; 35: 753–771
(2) Casey A et al. An in vitro comparison of microbial ingress into 8 different needleless iv access devices. J Infusion Nursing 2015; 38: 18–25
(3) Loveday HP et al. Epic 3: National evidence-based guidelines for preventing healthcareassociated infections in NHS hospitals in England. J Hosp Infect 2014; 86 Suppl 1: S1-S70
(4) Maragakis LL et al. Increased catheter-related bloodstream infection rates after the introduction of a new mechanical valve access port. Infect Control Hosp Epidemiol 2006; 27: 67–70
(5) Rupp ME et al. Outbreak of bloodstream infection temporally associated with the use of an intravascular needleless valve. Clin Infect Dis 2007; 44: 1408–1414