Schwere Infektionen aufgrund von Problemkeimen nehmen im Krankenhaus zu. Immunsupprimierte Patienten auf Intensivstationen – oft Sammelbecken für Klinikkeime – sind besonders gefährdet. Pflegenden kommt bei der Infektionsprävention eine wichtige Schlüsselfunktion zu.
Angst vor Seuchen ist seit jeher in der Menschheit tief verwurzelt. Seit Jahrzehnten stehen vor allem Krankenhausinfektionen in der öffentlichen Diskussion. Bereits 1957 titelte die damals neu auf dem deutschen Pressemarkt erschienene „Bild“-Zeitung: „Im Krankenhaus wirst du erst richtig krank“ – eine Überschrift, die in ähnlicher Weise auch in jüngster Vergangenheit genutzt wurde. So griff etwa das Nachrichtenmagazin „Focus“ das Thema Infektionen in der Ausgabe 7/2015 unter dem Slogan „Risiko Krankenhaus – Raus aus der Antibiotikafalle“ auf. Auch „Die Zeit“ thematisierte am 20. November 2014 mit der Überschrift „Die Rache aus dem Stall“ die Problematik der multiresistenten Erreger. In diesem Beitrag wurden unter anderem epidemiologische Daten genannt, für die es aber keine gesicherten Zahlen gibt.
Auch die öffentlich-rechtlichen Medien beteiligen sich an dieser wenig sachlichen Berichterstattung. So sendete etwa die ARD am 14. März 2016 und am 1. August 2016 eine Reportage mit dem Titel „OP gelungen – Patient tot“.
Nicht immer vermeidbar
Beispiele wie diese zeigen: Wenn in den populären Medien über die Gefahr von nosokomialen Infektionen informiert wird, werden lediglich Missstände angeprangert und Lösungsansätze häufig falsch interpretiert.
Vor diesem Hintergrund erstaunt es nicht, dass immer mehr Studien die Angst in der Bevölkerung vor Krankenhausinfektionen belegen. Zum Internationalen Tag der Patientensicherheit 2015 wurde etwa eine Untersuchung des Klinikbetreibers Asklepios zitiert, wonach knapp zwei Drittel der 1 000 Befragten im Falle eines stationären Aufenthalts am meisten eine Infektion mit einem multiresistenten Keim fürchten (1). Eine Befragung unter stationären Krankenhauspatienten im Universitätsklinikum Bonn zeigte indes, dass nur 48 Prozent der Patienten dem Personal hinsichtlich der Einhaltung von Hygienestandards vertrauen. 13 Prozent der Befragten befürchteten „sehr“ und 49 Prozent „etwas“, von einer nosokomialen Infektion betroffen sein zu können (2).
All dies zeigt, dass es dringend geboten ist, sich mit dem Thema Hygiene im Krankenhaus sachlich und auf der Grundlage gesicherter Fakten auseinanderzusetzen. Dies ist erschwert, weil zur Häufigkeit von Krankenhausinfektionen keine gesicherten Daten vorliegen. Man schätzt, dass es in deutschen Kliniken jährlich bis zu 800 000 Infektionen kommt. Nosokomiale Infektionen stellen damit hierzulande die häufigste Infektionskrankheit dar (5, 6, 22, 36). Offizielle Statistiken darüber fehlen weltweit, doch nach Einzelstudien erkranken bis zu 15 Prozent der Krankenhauspatienten an Infektionen, fünf bis acht Prozent davon tödlich. Dies wurde bereits 1978 von der renommierten Berliner Infektiologin Meta Alexander berichtet.
Die Folgen von Krankenhausinfektionen sind immens: Sie führen unter anderem zu einer längeren Liegedauer, einem erhöhten Pflegeaufwand, zusätzlich erforderlicher Diagnostik und Therapeutika sowie erheblichen Mehrkosten. Zudem bewirken sie immer häufiger, dass Bettenkapazitäten aufgrund von Isolierungsanforderungen sinken. Aus nosokomialen Infektionen können schlimmstenfalls schwere systemische Infektionen resultieren, die bis zum Tod des Patienten führen können.
Ein weiteres Problem: Wenn Patienten nach einer schweren akuten Erkrankung die Intensivstation verlassen, bleiben oft Einschränkungen bestehen (4). Beispielsweise kann wegen dauerhafter Schädigung des Atemzentrums oder der Atemmuskulatur eine langfristige Beatmungstherapie über ein Tracheostoma erforderlich sein. In den nachfolgenden Wochen der stabilisierenden Behandlung kommt es dann oft zum Auftreten weiterer Infektionen, die aufgrund der inzwischen erschöpften Abwehrmechanismen nicht mehr überwunden werden. Infektbedingt kommt es in dieser Phase nicht selten zu Todesfällen.
Krankenhausinfektionen treten bevorzugt bei schwerkranken Patienten auf. Jeder zweite Patient, der länger als 24 Stunden auf einer Intensivstation betreut wird, entwickelt im Verlauf der Behandlung eine Infektion (25). Unterschieden werden primär endogene, sekundär endogene und exogene Infektionen.
Primär endogen: Bei primär endogenen Infektionen ist der Erreger zum Zeitpunkt der Aufnahme im Darmtrakt anwesend. Die Infektion entsteht in den ersten Tagen nach Aufnahme. Typische Keime sind Streptococcus pneumoniae, Staphylokokkus aureus und Escherichia coli. Primär endogene Infektionen sind keine typischen Krankenhausinfektionen.
Sekundär endogen: Die Besiedelung des Darmtrakts erfolgt bei sekundär endogenen Infektionen nach der Aufnahme. Die Infektion entsteht üblicherweise ab dem vierten Tag der Krankenhausbehandlung. Typische Keime sind Methicillin-resistente Staphylokokkus aureus und Pseudomonas aeruginosa. Sekundär endogene Infektionen sind typische Infektionen, die auf der Intensivstation entstehen.
Exogen: Bei exogenen Infektionen gibt es keine endogene Besiedelung des Darmtrakts. Die Entstehung erfolgt ab dem vierten Tag. Typische Keime sind Methicillin-resistente Staphylokokkus aureus, Pseudomonas aeruginosa und Enterobacteriaceae. Exogene Infektionen entstehen auf der Intensivstation.
Eine völlige Reduktion von nosokomialen Infektionen ist bei endogenen Ursachen offenbar nicht möglich, wie eine Untersuchung über die Entwicklung nosokomialer Infektionen über einen Zeitraum von 13 Jahren zeigt (26).
Eine weitere Studie zeigt ebenfalls, dass eine Reduktion auf null nicht realistisch ist (27). Insgesamt wurden im Rahmen dieser Untersuchung 2277 Arbeiten gesichtet sowie 204 Volltexte akquiriert und beurteilt. In die quantitative Analyse wurden sieben prospektive Kohortenstudien eingeschlossen, die eine Reduktion von nosokomialen Infektionen bei aseptischen Eingriffen untersuchten. Die Maßnahmen beinhalteten Schulungen, antibiotische Prophylaxe sowie Desinfektions- und Reinigungsmaßnahmen des Operationsgebiets. Postoperative Wundinfektionen konnten durch die genannten Interventionen nur geringfügig und nicht signifikant reduziert werden. Besonders ältere Patienten mit Vorerkrankungen und Immunsuppression sind von einer weiteren steigenden Zunahme von Krankenhausinfektionen mit konsekutiver Sepsis – als schwere systemische Infektion – betroffen.
Schlussfolgerung: Zum beherrschbaren Risiko des Krankenhauses gehören danach nur solche Infektionen, die auf beeinflussbare – also exogene – Faktoren zurückzuführen und nachweisbar im zeitlichen und kausalen Zusammenhang mit dem Krankenhausaufenthalt aufgetreten sind.
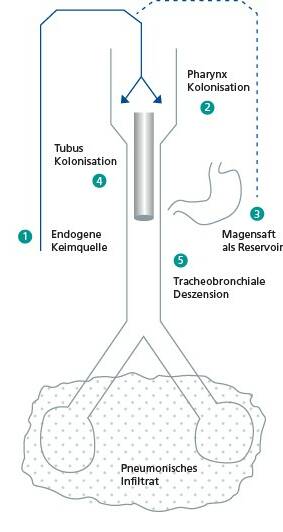
- Die Infektion erfolgt überwiegend endogen. Die Keimbesiedelung hat zum Zeitpunkt der Aufnahme also schon stattgefunden
- Die Kolonisation des Pharynx ist Ausgangsort der Infektion, die sich über tracheobronchiale Deszension ausbreitet
- Eine Magensaftbesiedlung, besonders im antazidifizierten Magensaft, stellt ein wichtiges Keimreservat dar
- Endotrachealtuben können zur Keimbesiedelung der Tubusoberflächen führen. Die Intubation ist in diesem Zusammenhang von erheblicher pathogenetischer Bedeutung, weil der endotracheale Tubus eine Mikroaspiration erleichtert und darüber hinaus die lokale Abwehr schwächt. Häufig isolierte Problemkeime, wie Pseudomonas aeruginosa sezernieren Exopolysaccharide und produzieren mithilfe dieser Substanz einen komplexen Biofilm. Dieser Biofilm ermöglicht den Bakterien die Adhäsion an abiotische Oberflächen und bietet zusätzlich Schutz vor direkter Antibiotikaeinwirkung (Bauer TT. et al. Intensivmed 37: 536–540)
- Respirator-assoziierte Pneumonie = Pneumonisches Infiltrat (durch Infektionserreger verursachte Lungenentzündung)
Quelle: Nach Schuster – modifiziert [10]
Intensivpatienten besonders gefährdet
Neue medizinische und operative Technologien, die mehr Interventionen bei Hochrisikopatienten ermöglichen und die zunehmende Veränderung der Alterspyramide in Deutschland haben zu einem immer kränkeren Patientengut geführt. Davon sind besonders sehr junge sowie auch immer mehr ältere Patienten in den Krankenhäusern betroffen.
Diese speziellen Patienten benötigen häufig eine intensivmedizinische Behandlung. Physiologische Schutzmechanismen verhindern das Eindringen von pathogenen Erregern. Dies setzt eine intakte Körperoberfläche, ausreichende Gewebeperfusion und eine natürliche Bakterienflora voraus.
Eine Infektion setzt immer das Eindringen pathogener Erreger in den Körper voraus. Neben den bereits angeführten Eintrittspforten wie einem Tracheostoma oder einem Venenkatheter bietet der kritisch kranke Patient in der post-akuten Phase oft zahlreiche weitere Eintrittspforten: kutane Defekte oder Wunden, Schleimhautulzerationen, arterielle Zugänge, Nasensonden und Blasenkatheter.
Das Tracheostoma ist ein Paradebeispiel für eine Eintrittspforte, da hier verschiedene Beeinträchtigungen zusammenkommen: der Effekt des Hustenstoßes wird vermindert, Aspirationen kommen leichter zustande, die Tracheotomie hinterlässt eine Haut- und Schleimhautwunde, es bildet sich in kurzer Zeit ein mikrobieller Biofilm auf dem Plastikmaterial der Trachealkanüle. Durch vielfaches Absaugen auf der Intensivstation entstehen Schleimhautschäden in der Trachea und in den proximalen Bronchien, wodurch die natürliche Zilienfunktion gestört wird.
Ein anderes Beispiel für eine Eintrittspforte ist das Dekubitalulcus, das sich bei vielen schwerkranken Patienten auf der Intensivstation infolge von Mikrozirkulationsstörungen entwickelt. Tiefe Dekubitalulcera können massenhaft Erreger beherbergen, etwa auch multiresistente Keime wie Methicillin-resistente Staphylococcus-aureus-Stämme (MRSA).
Aber auch ohne eine solche Besiedlung sind große Dekubitalulcera schädlich für die Infektabwehr, da aus ihnen ein chronischer Proteinverlust erfolgen kann, der das Sepsisrisiko erhöht. Die chronische, durch solche Ulcera unterhaltene Entzündungsreaktion erschöpft das Immunsystem. Nasogastrale Sonden stellen eine Leitschiene für gramnegative Keime aus dem Magen dar, die an ihnen entlang in den Rachenraum emporwandern und über Mikroaspirationen in die Lunge gelangen.
Intensivstation Sammelbecken für Keime
Die Intensivstation ist typischerweise ein Sammelbecken für zahlreiche Krankenhauskeime. Hierzu zählen Staphylococcus aureus, Enterokokken, Clostridium difficile, Pseudomonas aeruginosa und andere Pseudomonas-Arten sowie Stenotrophomonas maltophilia. Oft kommen antibiotika- beziehungsweise antimykotikaresistente Varianten dieser Spezies beim Intensivpatienten vor.
Die Übertragung erfolgt durch horizontale Verbreitung über Hygienefehler, wobei in erster Linie ein unzureichender Gebrauch von Einmalhandschuhen und Überkitteln bei der Versorgung der Patienten zu nennen ist. Aber auch Türgriffe, Bettholme, Stethoskope und andere unbelebte Gegenstände können derartige Erreger beherbergen. Die Übertragung erfolgt dann meist durch die nicht ausreichend desinfizierten Hände. Bei engen räumlichen Verhältnissen auf einer Station kann es auch zu einer aerogenen Übertragung bestimmter Erreger wie Legionellen, das Respiratorische Synzytial-Virus (RSV) oder Adenoviren kommen.
Zu den intakten Abwehrfunktionen eines gesunden Menschen gehören eine funktionierende Hypothalamus-Nebennierenachse, die Mobilisierbarkeit von Zytokinen und Akut-Phase-Proteinen sowie die Aktivierbarkeit des Immunsystems. Die erste Barriere der Abwehr ist die sogenannte natürliche Immunität. Unter diesem Begriff werden unspezifische Reaktionen wie die Rekrutierung neutrophiler Granulozyten, die Mobilisierung von natürlichen Antikörpern und die Antigenverarbeitung durch dendritische Zellen und Makrophagen zusammengefasst. Neuerdings wurde erkannt, dass auch Epithel- und Endothelzellen in dieser ersten Abwehrphase eine wichtige Rolle spielen, indem sie als Reaktion auf eine Schädigung Chemokine, Zytokine und mikrobizid wirkende Peptide oder nicht-peptidische Transmitter freisetzen.
Beim kritisch kranken Patienten sind diese Reaktionsmöglichkeiten oft weitgehend aufgebraucht. Schwerkranke Patienten auf der Intensivstation leiden oft an einer Reihe von Grundkrankheiten, die das Abwehrsystem bereits vor der Krankenhausaufnahme chronisch beanspruchen. Eine chronisch-obstruktive Lungenerkrankung (COLD) geht mit einer Schädigung und einem Funktionsverlust der Tracheal- und Bronchialepithelien einher, ein Diabetes mellitus führt besonders bei schlechter Blutzucker-Einstellung zur Verminderung der Phagozytoseleistung neutrophiler Granulozyten.
Auch das relativ hohe Durchschnittsalter von Intensivpatienten spielt für die natürliche Immunität eine Rolle, da es im fortgeschrittenen Alter zur Immun-Alterung beziehungsweise zur Immunseneszenz kommt. Bei chronischer Niereninsuffizienz wurde experimentell eine Einschränkung der Neutrophilenfunktion, der Komplementaktivierung und der zellulären Immunität nachgewiesen.
Durch die Behandlung auf der Intensivstation werden diese vorbestehenden Defizite weiter verstärkt. Auch eine ausgeglichene parenterale Ernährung führt vermutlich zu einem Mangel an bestimmten Proteinen und Spurenelementen, einer Vitamin-Dysbalance und bei Männern zu einem Testosterondefizit.
Durch den Einsatz von Corticoiden werden neutrophile Granulozyten und Lymphozyten in der Aktivität gehemmt. Intensivpatienten sind darüber hinaus einem kontinuierlichen Stress ausgesetzt. Experimentell wurde nachgewiesen, dass Stress die Zytokinfreisetzung und die natürliche Killer-Zell-Aktivität hemmt.
Dass diese Erschöpfung und Dysbalance des Immunsystems nach einer Intensivbehandlung tatsächlich nachgewiesen werden kann, haben verschiedene Untersuchungen gezeigt. So wurde beispielsweise in der Bronchialspülflüssigkeit von Patienten, die ein akutes Lungenversagen überstanden haben, eine erhöhte Konzentration von TGF-beta, IL-10 und IL1-Ra nachgewiesen (3). Bei diesen Zytokinen beziehungsweise Peptiden handelt es sich um anti-inflammatorische Moleküle, die die zelluläre Immunantwort hemmen.
Daten des nationalen Überwachungssystems für nosokomiale Infektionen der USA, des „National Nosocomial Infections Surveillance System (NNIS)“, belegten an 498.998 ausgewerteten Patienten, dass 83 Prozent der Episoden von Krankenhaus-erworbener Pneumonie mit einer künstlichen Beatmung, 97 Prozent der Harnwegsinfektionen mit einer Blasenkatheterisierung und 87 Prozent der Bakteriämien mit einem zentralvenösen Katheter assoziiert waren (8). Diesen Infektionen gemeinsam ist es, dass sie in direkten Zusammenhang mit einer medizinischen Intervention stehen. Das Risiko einer nosokomialen Ventilator-assoziierten Pneumonie ist bei intubierten Patienten deutlich erhöht und steigt mit zunehmender Beatmungsdauer.
Übersicht: Interventionen zur Vermeidung multiresistenter Erreger (MRE)
Systematische Erfassung des Vorkommens und der Verbreitung (Surveillance)
- Feststellung der krankenhauseigenen MRE-Rate
- Dabei auf Labordaten zurückgreifen
Frühzeitige Erkennung und Verifizierung von MRE
Schulung des Personals
Strikte Einhaltung allgemein anerkannter Hygienemaßnahmen. Besondere Bedeutung hat hier die hygienische Händedesinfektion
Screening
- Patienten, die MRE-Träger waren (z. B. MRSA)
- Kontaktpatienten
- Risikopatienten
Konsequente Isolationsmaßnahmen
- Händedesinfektion bei Patientenkontakt
- Schutzkittel und Handschuhe
- Mund-Nasen-Schutz bei aerosolproduzierenden Tätigkeiten und Besiedlung im Respirationstrakt
- Einzelzimmer
Aufklärung der Besucher über MRE-Status und besonders der hygienischen Händedesinfektion
Herausforderung MRE
Zu den Problemerregern zählen Methicillin-resistente Staphylococcus aureus (MRSA) und gramnegative Erreger mit besonderen Resistenzen. Erschreckend ist hierbei die Verbreitung von 3MRGN und 4MRGN – dies sind multiresistente gramnegative Stäbchen, die gegen drei beziehungsweise vier der häufigen Antibiotikagruppen resistent sind – beziehungsweise panresistenter Keime, die Resistenzen gegen nahezu alle gängigen Antibiotikagruppen aufweisen. Zu den 4MRGN-Erregern zählen Enterobakterien, Pseudomonas aeruginosa und Acinetobacter baumannii, die gegenüber den vier Antibiotikagruppen in der Behandlung von schweren Infektionen, wie den Acylureidopenicilline, Carbapeneme und Fluorchinolone resistent sind (15).
In Deutschland waren 2013 zirka sechs Prozent der nosokomialen Infektionen durch multiresistente Erreger bedingt. Der Anteil der 4MRGN-lnfektionen, die sehr schwer oder nicht mehr antibiotisch behandelbar sind – an allen Infektionen mit multiresistenten Erregerarten –, beträgt demnach zirka fünf Prozent, was zirka 1 500 4MRGN-Infektionen pro Jahr und einem Anteil von 0,3 Prozent aller nosokomialen Infektionen in Deutschland entspricht (16).
Risikofaktoren für multiresistente Erreger sind höheres Alter, vorangegangener Krankenhausaufenthalt, jüngste Antibiotikatherapie, Komorbiditäten, Immunsuppression, Katheter, bestätigter MRE-Nachweis, Kontakt zu MRE-positiven Personen, Diarrhoe, offene Wunden oder Reisen beziehungsweise Herkunft aus einer Region mit hoher MRE-Prävalenz. Besonders davon sind der nahe Osten und Nordafrika betroffen. Das Robert Koch-Institut empfiehlt bei den hier aufgezählten Risikopersonen ein generelles Screening bei Aufnahme in das Krankenhaus.
Abbildung 1 veranschaulicht die erforderlichen präventiven Maßnahmen zur Eindämmung multiresistenter Erreger.
Antibiotika breit einsetzen
Vor jeder Einleitung einer Antibiotikatherapie muss die Verdachtsdiagnose einer bakteriellen Infektion stehen. Klinisches Dilemma bei der Therapie mit Antiinfektiva ist die initiale Antibiotikatherapie nosokomialer Infektionen. Sie erfolgt fast immer ohne Kenntnis des Erregers.
Bei schweren im Krankenhaus erworbenen Infektionen müssen durch die eingesetzten Antibiotika möglichst alle infrage kommenden Erreger erfasst werden. Bei der Auswahl der Antibiotika sollte je nach der Schwere der Infektion, dem potenziellen Erregerspektrum, den Grundkrankheiten der Patienten, der Vorbehandlung mit Antibiotika und der lokalen Resistenzsituation veränderlich vorgegangen werden. Bei der Antibiotikatherapie schwerer Infektionen – wie der Sepsis – sollten breit und schnell wirkende bakterizide Antibiotika parenteral in hoher Dosis eingesetzt werden. Jede antiinfektive Substanz führt früher oder später zum Auftreten von resistenten Mikroorganismen (9, 4, 19).
Zwei Jahre nach Einführung des Penicillins wurden bereits die ersten Staphylokokkus-aureus-Stämme identifiziert, die aufgrund des Erwerbs einer Penicillinase Penicillin-resistent wurden. Um 1948 waren bereits 50 Prozent der Staphylokokken-Isolate Penicillin-resistent. Wird vom Methicillin-resistenten Staphylococcus aureus (MRSA) gesprochen, bedeutet dies eine Unempfindlichkeit des Erregers gegenüber Staphylokokken-wirksamen, penicillinasefesten Penicillinen.
Personalmangel ist Hygieneproblem
Der sich immer mehr abzeichnende Pflegepersonalmangel und die immer älter werdenden Patienten sind zu einer ernsten Herausforderung in den Kliniken geworden. Zu wenig Personal bedeutet immer auch zu wenig Hygiene in der Klinik. Aktuelle Studien belegen einen direkten Zusammenhang zwischen Anzahl der Krankenhaus-erworbenen Infektionen und der personellen Situation in einem Krankenhaus (28, 29, 30, 31).
Hier hat der deutsche Gesetzgeber 2011 mit der Novellierung des Infektionsschutzgesetzes (IfSG) in Paragraf 23 wesentliche Vorgaben erstellt, die der Vermeidung von nosokomialen Infektionen dient. Die dabei ermittelten Daten und eine regelmäßige Rückkopplung an das Personal soll die Aufmerksamkeit aller Beteiligten auf die adäquate Vorgehensweise und die Chancen der Vermeidung der im Krankenhaus erworbenen Infektionen (Surveillance) hinweisen.
Nach Paragraf 1 des IfSG liegt es in der Verantwortung der Häuser, eine angemessene Organisation und Hygiene sicherzustellen. Das bedeutet, dass die Krankenhausleitung für die Etablierung eines umfassenden Hygienestandards zur Gewährleistung der Patientensicherheit Sorge zu tragen hat. Bis zum 31. Dezember 2016 sollte die Krankenhaushygiene in allen Krankenhäusern durch Beschäftigung von Krankenhaus- hygienikern, Hygienefachkräften und Bestellung von hygienebeauftragten Ärzten und Hygienebeauftragten in der Pflege professionalisiert werden. Außerdem müssen die medizinischen Einrichtungen von nun an die klinisch-mikrobiologische und klinisch-pharmazeutische Beratung des ärztlichen Personals regeln und sicherstellen. Ein sogenanntes Antibiotic Stewardship ist zudem einzuführen.
Nach Paragraf 36 müssen auch Krankenhäuser ihre innerbetrieblichen Verfahrensweisen zur Infektionshygiene in Hygieneplänen festlegen. Dabei wird in Paragraf 1 auf die Eigenverantwortung der Träger und Leiter von Gemeinschaftseinrichtungen explizit auch hingewiesen (37).
Ziel ist der gesunde Patient
Resümee: Seitdem es Antibiotika gibt, haben sich nach kürzester Zeit Resistenzen entwickelt. Problematisch sind aber die zunehmenden multiresistenten Erreger, für die es wenige oder gar keine Behandlungsoptionen mehr gibt.
Beim Personal muss daher Verständnis für hygienische und epidemiologische Vorgänge erweckt werden und das Bewusstsein geschärft werden, dass Infektionen im Krankenhaus weitgehend zu verhindern sind. Dazu gehören eine rasche Erkennung von Patienten, bei denen ein Infektionsrisiko ausgehen kann, die umgehende Isolierung und die Einhaltung der Hygieneinterventionen, um eine Transmission von pathogenen- und besonders multiresistenten Problemerregern zu vermeiden.
Pflegende haben hier eine besondere Schlüsselfunktion inne. Ein optimaler Personalschlüssel von ausreichend und gut qualifizierten Beschäftigten in Medizin- und Pflegeberufen in den Krankenhäusern stellt in der Infektionserkennung und Prävention eine Grundvoraussetzung dar. Es muss aber auch darauf hingewiesen werden, dass jeder Patient, der sich einer medizinischen Behandlung unterzieht, das Risiko einer nosokomialen Infektion eingeht. Krankenhausinfektionen sind keineswegs neu – sie sind so alt, wie Kranke hospitalisiert werden.
Die relativ konstante Prävalenz der Krankenhaus-erworbenen Infektionen ist Hinweis dafür, dass es in den vergangenen Jahren nicht zu einem prinzipiellen Anstieg des nosokomialen Infektionsrisikos für Patienten in Deutschland gekommen ist (49). Ziel aller qualitätsorientierenden Maßnahmen im Krankenhaus muss der gesunde Patient sein.
(1) Richter-Kuhlmann, E. Patientensicherheit – Ein Kulturwandel vollzieht sich. Deutsches Ärzteblatt (2015) 112: 39
(2) Stoffels et al. Wissenstand und Einstellung stationärer Patienten zur Krankenhaushygiene. HygMed (2016);41 Suppl. pp 45 DGKH 2016
(3) Armstrong L, Millar AB. Relative production of tumour necrosis factor alpha and interleukin 10 in adult respiratory distress syndrome. Thorax (1997) 52: 442–6
(4) Kalb TH et al. Infection in the chronically critically ill: unique risk profile in a newly defined population. Crit Care Clin (2002) 18: 529–552
(5) Behnke M et al. Nosocomial infection and antibiotic use: a second national prevalence study in Germany. Dtsch Arztebl Int (2013);110: 627–633
(6) Walger P et al. Stellungnahme der DGKH zu Prävalenz, Letalität und Präventionspotenzial nosokomialer Infektionen in Deutschland 2013. Hyg Med (2013) 38: 329–338
(7) Schröder C et al. Epidemiology of healthcare-associated infections in Germany: nearly 20 years of surveillance. Int J Med Microbiol (2015) 305: 799–806
(8) Gerberding JL. Director Hospital Infections Program National Center for Infectious Diseases Centers for Disease Control and Prevention. NNIS SAR December 1999, corrected 3/29/2000
(9) Schuster H-P. Nosokomiale Pneumonien auf Intensivstationen. Atemwegs-Lungenkrankheiten 1988; 14: 80–84
(10) Marusch F et al. Welche Faktoren beeinflussen die postoperative Letalität beim kolorektalen Karzinom. Zentralbl Chir 2002;127: 614–621
(11) Erasmus V et al. Systematic review of studies on compliance with hand hygiene guidelines in hospital care. Infect Control Hosp Epidemiol 2010; 1: 283–294
(12) Richter A. Chirurgische Standards der perioperativen Patientenbehandlung. Chirurg 2012; 83: 343–350
(13) Schelonka RL et al. Sustained reductions in neonatal nosocomial infection rates following acomprehensive infection control intervention. J Perinatol 2006; 26: 176–179
(14) Geffers C et al. Incidence of healthca-re-associated infections in high-risk neonates: results from the German surveillance system for very-low-birthweight infants. J Hosp Infect 2008; 68: 214–21
(15) KRINKO: Hygienemaßnahmen bei Infektionen oder Besiedlung mit multi- resistenten gramnegativen Stäbchen. Bundesgesundheitsbl – Gesundheitsforsch – Gesundheitsschutz 2012; 55: 1311–1354
(16) Wille B. Multiresistente Erreger – Presse und Politik. Krh Hyg Inf Verh 2015; 37: 169–170
(17) Rusek R et al. Clostridium difficile surveillance in London. England. Abstract no. P17.691. J Hosp Infect 2006; 64: (Suppl 1) S103–29
(18) Jurke A et al. Infektionsmeldungen in Nordrhein-Westfalen (Vortrag anlässlich des 11. Ulmer Symposiums Krankhausinfektionen, 28.–30. April 2015
(19) Bobulski GS et al. Clostridium difficile skin contamination in patients with C.-difficile-associated disease. Clin Infect Dis 2008; 46: 447–50
(20) Cairns S et al. The prevalence of health-care associated infection in older people in acute care hospitals. Infect Control Hosp Epidemiol 2011; 32: 763–767
(21) Exner D et al. Krankenhaushygienische Herausforderungen durch multiresistente Erreger in der Chirurgie. Allgemein- und Viszeralchirurgie up2date 2014; 8: 433–448
(22) Passoth N. Wo steht die Krankenhaushygiene 2025? Interview mit Prof. Dr. med. Martin Exner, Bonn. Management & Krankenhaus 2016; 3: Supplement pp3–4
(23) Personelle und organisatorische Voraussetzungen zur Prävention nosokomialer Infektionen. Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention. Bundesgesundheitsbl 2009; 52: 951–962
(24) Sánches Garcia M. SDD bei hoher Prävalenz von MRSA und anderen resistenten Erregern. Journal Anästhesie und Intensivbehandlung 2004; 1: 219–220
(25) Alberti C et al. Systemic inflammatory response and progression to severe sepsis in critically ill infected patients. Am J Respir Crit Care Med 2005; 171: 461–468
(26) Weigert N. Entwicklung nosokomialer Infektionen über 13 Jahre (1998–2010). Dissertation der Medizinischen Fakultät der Friedrich-Schiller-Universität Jena 2013
(27) Tacconelli E et al. Infection risk in sterile operative procedures – a systematic review and meta-analysis. Dtsch Arztebl Int 2016; 113: 271–278
(28) Stone PW et al. Nurse working conditions and patient safety outcomes. Medical Care 2007; 45: 571–578
(29) Hugonnet S et al. The effect of wor-kload on infection risk in critically ill patients. Crit Care Med 2007; 35: 76–81
(30) Stone PW et al. A systematic audit of economic evidence linking nosocomial infections and infection control interventions. Am J Infect Control 2002; 30: 145–152
(31) Needleman J et al. Nurse staffing an inpatient hospital mortality. N Engl J Med 2011; 364: 1037–1045
(32) Pronmost R et al. An intervention to decrease catheter-related bloodstream infections in the ICU. N Engl J Med 2006; 355: 2725–32
(33) Zack JE et al. Effect of an education program aimed at reducing the occurrence of ventilator-associated pneumonia. Crit Care Med 2002; 30: 2407–2412
(34) Gastmeier P. Geffers C. Prevention of catheter-related bloodstream infections. J Hosp Infect 2006; 64: 32365
(35) Murray T et al. Ventilator-associated pneumonia improvement program. AACN Adv Crit Care 2007; 18: 190–9
(36) Gastmeier P et al. Wie viele nosoko-miale Infektionen. Dtsch Med Wochenschr 2010; 135: 91–93
(37) Erlde, H. Infektionsschutzgesetz: Kommentar. 5. Auflage, 2016 ecomed Medizin Landsberg am Lech
(38) Gastmeier P et al. Nosokomiale Infektionen und Infektionen mit multiresistenten Erregern – Häufigkeit und Sterblichkeit. Dtsch Med Wochenschr 2016; 141: 421–426
(39) Rhame F. Sudderth W. Incidence and prevalence as used in the analysis of the occurence of nosocomial infection rates. Am J Epidemiol 1981; 113: 1–11
(40) Peine CKP. Konnatale und Nosokomiale Infektionen bei neonatologischen Intensivpatienten. Dissertation. Fachbereich Humanmedizin. Justus-Liebig-Universität Gießen 1995
(41) Mildner T. De febre puerperale – Eine medizinhistorische Studie um den Hospitalismus im 18. Jahrhundert. Mildner Verlag Traunstein 1950
(42) Müller B. Risikofaktoren und Folgen der primären nosokomialen Sepsis mit multiresistenten gramnegativen Erregern in einem Universitätskrankenhaus. Dissertation der Medizinischen Hochschule Hannover 2011
(43) Diaz Granados, CA et al. Comparison of mortality associated with vancomycin-resistant and vancomycin-susceptible enterococcal bloodstream infections: a meta-analysis. Clin Infect Dis, 2005; 41: 327–33
(44) Diaz Granados, CA, Jernigan, JA. Impact of vancomycin resistance on mortality among patients with neutropenia and enterococcal bloodstream infection. J Infect Dis, 2005; 191; 588–95
(45) Edmond, MB et al. Nosocomial bloodstream infections in United States hospitals: a three-year analysis. Clin Infect Dis, 1999; 29: 239–44
(46) Cosgrove SE et al. Health and economic outcomes of the emergence of third-generation cephalosporin resistance in Enterobacter species. Arch Intern Med, 2002; 162: 185–90
(47) Schwaber MJ et al. Clinical and economic impact of bacteremia with extended-spectrum-beta-lactamase-producing Enterobacteriaceae. Antimicrobial Agents and Chemotherapy 2006 50; 1257–1262
(48) Kampf WD. Die Wirkung von Antibiotikaeinsatz auf Krankenhausinfektionen. Die Schwester Der Pfleger (1982) 21: 705–707
(49) Gastmeier P, Piening B. Deutsche Daten der ersten europäischen Prävalenzerhebung zum Vorkommen nosokomialer Infektionen und zur Antibiotikaanwendung. In: GERMAP 2012 – Antibiotika-Resistenz und -Verbrauch. Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation mbH, Rheinbach 2014